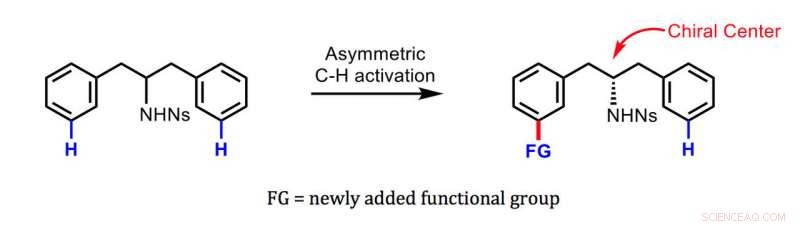
Den nya metoden utvecklad av Yu och kollegor. Kredit:Jin-Quan Yu/Scripps Research
Kemister vid Scripps Research har tagit itu med en av de mest formidabla utmaningarna inom syntetisk kemi genom att uppfinna en metod för "enantioselektiv fjärr-meta-CH-aktivering, " som möjliggör tillverkning av kirala molekyler som tidigare var svåra eller omöjliga att syntetisera.
Metoden, rapporterade idag i Natur , kommer sannolikt att användas i stor utsträckning för tillverkning av potentiella läkemedel och andra kemiska produkter.
"Denna nya metod borde göra det möjligt för oss att utforska ett stort "kemiskt utrymme" som i huvudsak hade varit förbjudet, " säger Jin-Quan Yu, Ph.D., senior utredare och Frank och Bertha Hupp professor i kemi vid Scripps Research.
Kirala molekyler är asymmetriska, med formerna "höger hand" och "vänster hand". Ofta har bara en av dessa former (kallade enantiomerer) den önskade biologiska eller kemiska aktiviteten, medan den andra är inert eller till och med har oönskade biverkningar - och de flesta vanliga reaktioner ger en oren, 50:50 mix av båda.
Det finns metoder för att omvandla en symmetrisk molekyl till en kiral och erhålla rena kvantiteter av en enantiomer snarare än den andra. Dock, dessa metoder involverar typiskt fästningen av ett reaktivt kluster av atomer som kallas en funktionell grupp till startmolekylen vid den punkt som blir centrum för asymmetri:det så kallade kirala centret. Den nya metoden fäster en ny funktionell grupp relativt långt från det kirala centret - en bedrift som tidigare endast uppnåtts av enzymer i levande celler. Eftersom det kirala centret vanligtvis innehåller en annan funktionell grupp, den resulterande kirala molekylen slutar med två funktionella grupper med stor spridning, potentiellt ge unik och potent bioaktivitet.
"De kirala molekylerna vi kan göra med den här metoden kan designas för att interagera med vitt åtskilda bindningsställen på ett målprotein, till exempel, " säger Yu.
Nyckeln till den nya metoden är en specialdesignad hjälpmolekyl, en "övergående kiral mediator, " baserat på den organiska föreningen norbornen. Det möjliggör det avgörande steget att fästa den nya funktionella gruppen asymmetriskt till en initialt symmetrisk utgångsförening - långt från det kirala centret på den molekylära ryggraden men, ändå, vilket ger nästan 100 procent rena kvantiteter av den önskade enantiomeren.
Yus team demonstrerade tekniken genom att använda den för "fjärrkiral induktion" av bensylaminer och fenyletylaminer, breda klasser av molekyler som utgör basen för många moderna läkemedel såväl som många biologiskt aktiva föreningar i växt- och djurceller. De resulterande kirala molekylerna omfattade typiskt mer än 95 procent av den önskade enantiomeren och mindre än 5 procent av den oönskade enantiomeren.
Yu och hans grupp undersöker för närvarande sätt att vidga omfattningen av denna strategi till andra klasser av startmolekyler. De använder också sin nya metod för att skapa stora bibliotek med tidigare otillgängliga föreningar, som kan screenas för att upptäcka potentiella nya läkemedel.