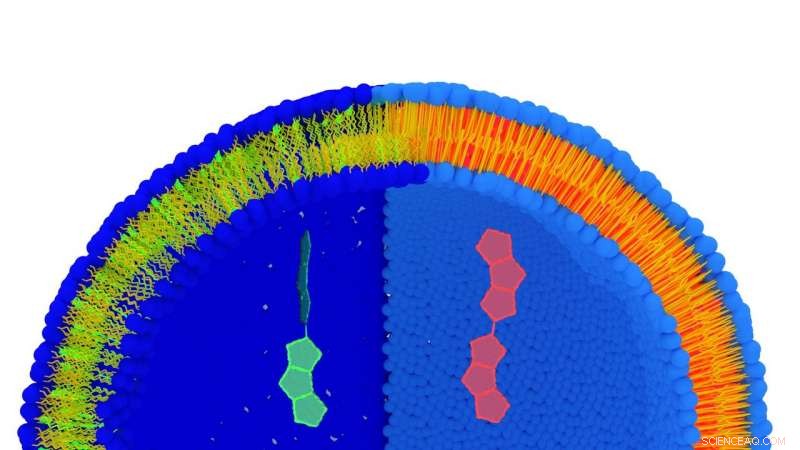
Konstnärens syn på ett lipidmembran märkt med FliptR-molekylen. Lipiderna är blå (hydrofil del) och gula (hydrofob del). När lipider sträcks ut (vänster del) har molekylen en kort livslängd (grön), medan när lipiderna är mer kompakta, dess livslängd är lång (röd). Båda konformationerna visas i stor skala i mitten av bilden. Kredit:© UNIGE
Volymen av celler kan variera dramatiskt. På samma sätt som en uppblåsande ballong, volymökningen av växande celler trycker på plasmamembranet – lipidhöljet som omger cellen. Detta "turgor" tryck ökar spänningen i membranet, som, om den lämnas okorrigerad, kommer i slutändan att få cellen att spricka. För att förhindra att detta händer, celler har utvecklat mekanismer för att övervaka spänningen i deras plasmamembran. När spänningen är för hög, celler svarar genom att öka mängden lipid i membranet. Omvänt, när spänningen är för låg, celler tar bort lipid från membranet för att "dra åt" det. Hur celler lyckas känna av spänning och utlösa den lämpliga biologiska responsen har förblivit ett mysterium. Det har varit svårt att lösa på grund av brist på verktyg för att studera membranspänningar i levande celler. För att ta itu med detta problem, forskare från universitetet i Genève (UNIGE) och National Centre for Competence in Research Chemical Biology (NCCR) har samarbetat för att skapa en fluorescerande molekyl för att mäta spänningen i plasmamembranet hos levande celler. Med detta nya verktyg, de kunde sedan upptäcka hur celler anpassar sin yta till sin volym. Dessa resultat, publiceras i Naturkemi och Naturens cellbiologi , bana väg för många applikationer, inklusive vid upptäckt av cancerceller som vanligtvis uppvisar avvikande hög membranspänning.
När volymen av en cell ökar, spänningen som utövas på dess membran ökar, orsakar aktivering av TORC2 – ett komplex av proteiner som skapar varningssignaler i cellen. "Cellmembranet består av lipider organiserade i ett semipermeabelt dubbelskikt, " förklarar Aurélien Roux, professor vid institutionen för biokemi vid UNIGEs naturvetenskapliga fakultet och medlem av NCCR. "Denna yta är flytande, tillåter stor anpassningsförmåga av membranet till förändringar i form och volym av cellen. Som vilken yta som helst, den kan sträckas och utrymmet mellan lipiderna ökar då. När detta utrymme blir för stort och membranet riskerar att gå sönder, ett protein, heter Slm1, aktiverar TORC2 för att producera signaler som driver cellen att producera nya lipider och i sin tur minskar spänningen i cellmembranet." Men hur kunde forskarna mäta spänningen som behövs för att utlösa denna process?
För att utvärdera spänningen i cellmembranet, det är nödvändigt att kunna mäta utrymmet mellan lipiderna som utgör detta membran. Stefan Matile, professor vid institutionen för organisk kemi vid UNIGEs naturvetenskapliga fakultet och medlem av NCCR, har skapat en "sondmolekyl" som heter FliptR (Fluorescent Lipid Tension Reporter), som integreras spontant mellan lipiderna i plasmamembranet. "Vi har utvecklat en fluorescerande molekyl med två små "fenor" som definierar en viss vinkel mellan dem, han förklarar. Denna vinkel varierar beroende på trycket som utövas på FliptR, som ändrar dess fluorescens." Genom att dra fördel av denna skillnad i molekylens fluorescensegenskaper, gruppen av professor Roux kunde mäta utrymmet mellan lipiderna och därmed spänningen i ett membran.
FliptR är ett värdefullt nytt verktyg för att mäta spänningen i plasmamembranet i levande celler. "Vi vet att cancerceller har högre membranspänning än normala celler. Vi hoppas att denna fluorescerande molekyl en dag kommer att hjälpa till att upptäcka dem lättare, säger Stefan Matile.
Och när det gäller att minska spänningen i cellen?
När spänningen i plasmamembranet ökar, TORC2 aktiveras och detta utlöser produktionen av lipider för att sänka spänningen tillbaka till basala värden. Men vad händer när spänningen i membranet är för låg och måste ökas? "Vi trodde först att det skedde genom samma mekanism som körde baklänges, men historien visade sig vara mycket mer intressant, " säger Robbie Loewith, professor vid institutionen för molekylärbiologi vid UNIGE-naturvetenskapliga fakulteten och även medlem i NCCR. Verkligen, initial forskning visade att TORC2-aktivatorn Slm1 – involverad i att känna av hög membranspänning – överraskande nog inte spelar någon roll i svaret på för lite spänning. "Å andra sidan, vi observerade att en viss lipid som finns i plasmamembranet, kallas PIP2, är sensorn för låg membranspänning."
När membranspänningen minskar, PIP2, tidigare blandat med andra lipider, självsegregerar för att bilda PIP2 "öar" i ett hav av kvarvarande lipider i membranet, i en process som inte liknar den spontana separationen (höjningen) av grädde i färsk mjölk. Eftersom ett av proteinerna i TORC2 binder PIP2, TORC2 omdistribuerar också till dessa PIP2-öar. En gång uppslukad av dessa holmar, TORC2 inaktiveras. "Lipiderna i cellmembranet bryts ned naturligt, och TORC2-aktivitet är nödvändig för att ersätta dem" förklarar Robbie Loewith. Men när TORC2 hämmas inom PIP2-öarna, de nedbrutna lipiderna ersätts inte längre, vilket resulterar i en ökning av spänningen i plasmamembranet. Om denna omkalibrering är blockerad, celler kan inte justera spänningen i sitt plasmamembran och dör.
Ett kemiskt mätverktyg för att hjälpa forskning inom biologi
Tack vare spänningsmätningstekniken utvecklad av Stefan Matile och Aurélien Roux, teamen av professorerna Roux och Loewith kunde utföra sina experiment på jästsvampar och mäta spänningsvariationerna i plasmamembranet. Membranspänning är en mycket viktig parameter att kontrollera i alla cellulära processer där membran är involverade, såsom motilitet, endocytos (processen genom vilken cellen matar sig själv), eller celldelning, och särskilt när det gäller cancerutveckling. Forskarna fokuserar nu på att kontrollera om mekanismen som observeras i jäst är densamma i mänskliga celler, med den långsiktiga idén att utveckla läkemedel som kan reglera TORC2, eller till och med att förhindra utvecklingen av vissa cancerformer.