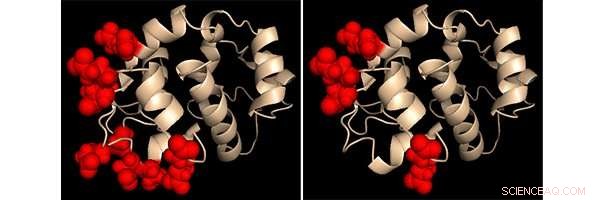
Proteinkemiker skildrar den kalciumavkännande regionen i två konstruerade STIM1-proteinvarianter. De platser som ändrades markeras i varje fall som röda sfärer. Beteendet hos dessa två konstruerade proteiner gav viktig insikt i hur STIM1 upptäcker förändringar i kalciumnivåer Kredit:Dr Patrick Hogan, La Jolla Institute for Immunology
Alla däggdjursceller behöver en klar tillförsel av kalciumjoner för att utföra funktioner som är så olika som neurotransmission, muskelsammandragning, hormonfrisättning, eller immunsvar. Så grundläggande är detta krav att celler skyddar sig mot katastrofer genom att lagra kalcium i ett nätverk av intracellulära cisterner som kallas endoplasmatisk retikulum, eller ER. Sedan, som celler förlorar kalcium som en del av sin dagliga rutin, kanaler öppnas i cellens membran så att kalciuminflödet utifrån kan fylla ER-reserverna igen och bibehålla kalciumdrivna cellulära funktioner.
Två studier nyligen publicerade av La Jolla Institute for Immunology (LJI) utredare Patrick Hogan, Ph.D., och Aparna Gudlur, Ph.D. - ett papper som visas tidigt i år Cellrapporter och den andra i oktober 31, 2018, frågan om Naturkommunikation —Rapportera hur ett kalciumavkännande protein som kallas STIM1 signalerar att det är dags att initiera kalciumhämtning och sedan vidarebefordrar det meddelandet till sin partner, kalciumkanalen ORAI. Detta arbete ger grunden för nya sätt att manipulera avvikande kalciumsignalering i immunsystemet, särskilt i samband med autoimmun eller inflammatorisk sjukdom.
"Vi har vetat i ett decennium att STIM1 -proteinet rörde sig mot plasmamembranet för att öppna ORAI -kanaler när ER -kalciumnivåerna sjunker, säger Hogan, professor i avdelningen för signalering och genuttryck. "Vårt senaste arbete visar hur STIM -maskineriet fungerar på molekylär nivå. Att förstå dessa mekanismer är avgörande, eftersom kalcium är viktigt för ett stort antal immunsvar. "
De Cellrapporter papper avslöjar hur STIM1 -protein förlängs när det växlar från vilande till aktiverat tillstånd när kalciumreserverna sjunker. STIM1 är ett transmembranprotein som spänner över ER-väggen:ena änden petar in en kalciumavkännande oljestickliknande svans inuti reservatet; i vila, kalciumfylldt tillstånd, den andra armen sticker ut från akuten men förblir stoppad mot ER -väggen, ur kontakt med vilande ORA1 -kanaler som prickar cellmembranet.
Gruppen definierade vad som händer när kalciumnivåerna sjunker genom att konstruera och testa beteendet hos genetiskt modifierade STIM1-proteiner i odlade celler. Analys visade att kalciumförlust från sensorns svans orsakade att membranspannande områden av par av STIM1-proteiner drog ihop inuti ER-väggen, vilket fick de yttre armarna att sträcka sig mot cellmembranet. Den formändringen förde STIM1 tillräckligt nära ORAI -kanaler för att nå ut och öppna dem, så att kalcium kan flöda tillbaka till cellerna.
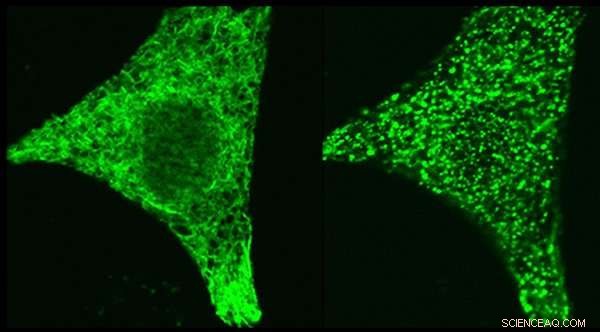
Mikroskopbilder av regleringsproteinet STIM1- märkt genetiskt med en grön fluorescerande tagg- i samma cell före stimulering (vänster panel) och efter stimulering (höger panel). STIM1 omplacerar, när cellen stimuleras, till platser där den kan koppla kalciumkanalen ORAI1. Mekanismen som initierar denna STIM1 -rörelse var i fokus för de två studierna. Upphovsman:Dr Aparna Gudlur, La Jolla Institute for Immunology
"Det första dokumentet visade hur STIM1 kommunicerar med ett kanalprotein i plasmamembranet genom en strukturell förändring, "säger Hogan." Vår senaste tidning tar den processen ett steg tillbaka i tiden och avslöjar hur kalciumförlust inuti akuten initierar den förändringen. "
Enkelt uttryckt, det nyare dokumentet fokuserar på hur STIM1 kalciumkännande mätstickan fungerar. Tidigare, proteinkemister fann att kalcium inuti ER binder till ett strukturmotiv i STIM1-svansen som kallas en "EF-hand" och föreslog att när handen var tom, STIM1 aktiverad ORAI. Gudlur, en instruktör i Hogan -labbet och den nya tidningens första författare, förklarar att det inte är så enkelt. "Vi rapporterar nu att flera kalcium binder inte bara till EF-handen utan till andra platser i STIM1 ER-domänen, och att sajterna är beroende av varandra, "säger hon." Det reviderar konceptet om hur STIM1 aktiveras. "
Inte bara det, men enligt Hogan hade den rådande tron varit att kalciumdissociation gör att STIM1:s oljestickliknande region inuti akuten utvecklas dramatiskt och antar en kaotisk struktur, en störning som anses nödvändig för ORAI -aktivering. "Vi visar nu att när kalcium är lågt på ER -området utvecklas inte denna region utan får istället en ny men stabil struktur som gynnar interaktion med ORAI -kanalen, "säger han." Det är viktigt eftersom det betyder att interaktion kan riktas av hämmare. "
Faktiskt, läkemedelsföretag har redan försökt utveckla läkemedel för att blockera ORAI-kalciumkanaler som medel för att stoppa kalciumberoende immunsvar vid autoimmun sjukdom eller vid inflammatoriska tillstånd som akut pankreatit. Vissa ORAI-blockerande läkemedel är för närvarande i fas I och II kliniska prövningar och verkar hittills giftfria. Men deras terapeutiska potential är fortfarande okänd.
Gudlur, som hade en ledande roll i båda studierna, spekulerar i att utveckla direkta ORAI/STIM1 -blockerare som terapier bara kan vara ett första steg, eftersom båda proteinerna är gemensamma för många celltyper. "Inriktning på ORAI -kanaler som ett sätt att blockera överskott av kalciumsignalering endast i vissa celler kan kräva större specificitet, "säger hon." Vårt arbete är ett första steg för att identifiera cellspecifika faktorer som kan modulera ORAI/STIM1-aktivitet. När vi väl hittar dem, läkemedelsskärmar som riktar sig till dessa faktorer skulle krävas. "
Hogan håller med om att upptäckten av droger bygger på en grund för utforskning. "Människor som bedriver grundforskning måste undersöka grundläggande cellulära processer, " han säger, noterade att mer än 20 år gick mellan upptäckten av immunkontrollpunktsproteinet CTLA4 och FDA -godkännande av immunkontrollblockad som behandling för melanom. (Obs! Fyra dagar efter den här intervjun tilldelades "upptäckarna" som heter Hogan Nobelpriset 2018 i fysiologi och medicin). "Om du inte pysslar med grunderna i en cell kommer du aldrig att hoppa framåt. Vi vet inte alltid var terapierna kommer att komma ifrån."