OCTN:En liten transportfamilj med stor relevans för mänsklig patofysiologi, Drug Discovery and Diagnostics Credit:Cesare Indiveri
I februari 2019 -numret av SLAS Discovery , en granskning av forskare från University of Calabria (Italien) undersöker ULT, en liten men spännande grupp transportörer som öppnar nya gränser inom forskning om läkemedelsdesign för att förbättra läkemedelsleverans och förutsäga läkemedelsinteraktioner.
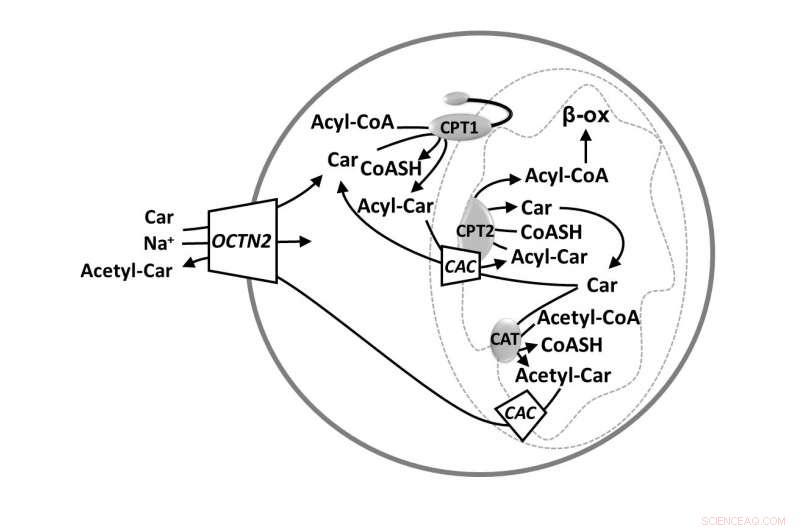
OCTN förmedlar flödet av fysiologiska organiska katjoner genom cellmembranet. Bland de tre medlemmarna i underfamiljen, OCTN1 och 2 finns hos människor, medan OCTN3 gick förlorad under evolutionen. OCTN2 har en väletablerad roll för att upprätthålla homeostas av karnitin, en viktig kofaktor för att producera energi från fettsyraomsättningen. Vissa ärftliga defekter av OCTN2 orsakar den primära karnitinbristen, en svår muskelpatologi som kan lindras genom att administrera karnitin som ett läkemedel. Anmärkningsvärda brister som efterliknar sjukdomsfunktionerna kan orsakas som biverkningar av att vissa läkemedel stör karnitinabsorptionen eller av en strikt vegetarisk kost under graviditet eller spädbarn.
Den patofysiologiska rollen för OCTN2 bekräftas också av dess närvaro i exosomer, nanovesiklar som släpps ut i den extracellulära miljön som är involverad i cell -till -cell -kommunikation. Intressant, OCTN1 -funktionen förblir relativt oklar. Faktiskt, ablation av dess gen orsakar tydligen inga problem hos djur. Dock, vissa mutationer av OCTN1 hos människor är associerade med inflammatoriska sjukdomar som Crohns sjukdom.
Studier med de senaste metodologiska metoderna belyser en länk mellan OCTN1 och inflammation, vilket tyder på att molekyler med antiinflammatoriska eller antioxidantegenskaper kan vara OCTN1-ligander. I denna ram, ergotionin, en svampmetabolit och acetylkolin har föreslagits. Den senare är en välkänd neurotransmittor som också spelar en roll vid inflammation via ett icke-neuronalt kolinergt system. Både OCTN1 och OCTN2 visar en sidofunktion i interaktion med katjoniska läkemedel. Dessa nya fynd öppnar nya gränser inom forskning om läkemedelsdesign för att förbättra läkemedelsleverans och förutsäga läkemedelsinteraktioner.