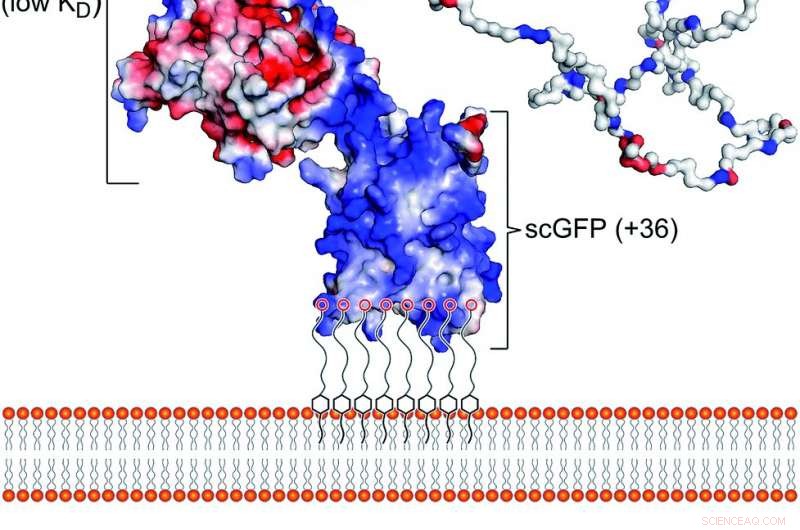
Fig. 1 Den konstgjorda plasmamembranbindande konstruktionen. (a) Schematisk visning av interaktionen mellan den polymert ytaktiva substansen konjugerade överladdade fusion [CshA_scGFP] [S] konstruktionen med dubbelskiktet i det cytoplasmatiska membranet. Strukturen visar ytladdningspotentialen, markerar den höga positiva laddningen (blå) på den överladdade GFP -domänen och den negativa laddningen (röd) på den globala CshA -domänen, samt "catch" och "clamp" -domänerna för CshA. (b) Strukturen av den anjoniska polymerens ytaktiva glykolsyraetoxylat 4-nonylfenyleter (S), som elektrostatiskt komplexar med den överladdade GFP -gruppen. Kredit:Kemisk vetenskap, öppen åtkomst:https://pubs.rsc.org/en/content/articlelanding/2019/sc/c9sc02650a#!divAbstract
I en värld först, forskare har hittat ett nytt sätt att styra stamceller till hjärtvävnad. Resultaten, ledd av forskare vid University of Bristol och publicerad i Kemisk vetenskap , kan radikalt förbättra behandlingen för hjärt -kärlsjukdom, vilket orsakar mer än en fjärdedel av alla dödsfall i Storbritannien.
Hittills, försök med stamceller, som tas och odlas från patienten eller givaren och injiceras i patientens hjärta för att regenerera skadad vävnad, har gett lovande resultat.
Dock, medan dessa nästa generations cellterapier är i horisonten, betydande utmaningar i samband med fördelningen av stamcellerna har kvarstått. Högt blodflöde i hjärtat i kombination med olika vävnadssänkor, "som cirkulerande celler kommer i kontakt med, betyder att majoriteten av stamcellerna hamnar i lungorna och mjälten.
Nu, forskare från Bristols skola för cellulär och molekylär medicin har hittat ett sätt att övervinna detta genom att modifiera stamceller med ett speciellt protein så att de "hem" till hjärtvävnad.
Dr Adam Perriman, studiens huvudförfattare, docent i biomaterial, UKRI Future Leaders Fellow och grundare av cellterapiteknikföretaget CytoSeek, förklarade:"Med regenerativa cellterapier, där du försöker behandla någon efter en hjärtattack, cellerna går sällan dit du vill att de ska gå. Vårt mål är att använda denna teknik för att omarbeta cellmembranet, så att när de injiceras, de kommer att innehålla specifika vävnader efter vårt val.
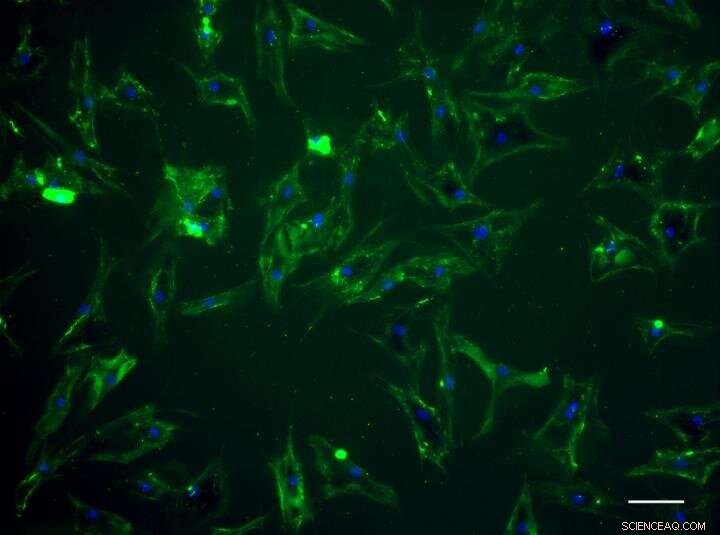
Mänskliga mesenkymala stjälkar uppvisar grön fluorescens efter att de "målats" av designerproteinet. Kredit:University of Bristol
"Vi vet att vissa bakterieceller innehåller egenskaper som gör det möjligt för dem att upptäcka och" hem "för sjuk vävnad. Till exempel, den orala bakterien som finns i våra munnar kan ibland orsaka halsfluss. Om det kommer in i blodströmmen kan det "hem" för skadad vävnad i hjärtat som orsakar infektiös endokardit. Vårt mål var att replikera bakteriecellernas hemförmåga och tillämpa den på stamceller. "
Teamet utvecklade tekniken genom att titta på hur bakterieceller använder ett protein som kallas ett adhesin för att ”hem” till hjärtvävnad. Med hjälp av denna teori, forskarna kunde producera en artificiell cellmembranbindande version av adhesinet som kunde ”målas” på utsidan av stamcellerna. I en djurmodell, laget kunde visa att denna nya cellmodifieringsteknik fungerade genom att styra stamceller till hjärtat i en mus.
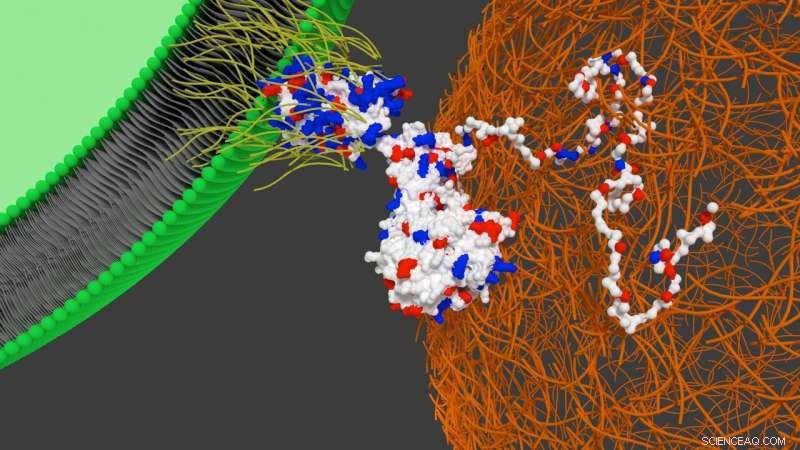
Schematisk bild av interaktionen mellan designerproteinet på stamcellens yta och hjärtfibronektin. Kredit:University of Bristol
Dr Perriman tillade:"Våra fynd visar att infektiösa bakteriers hjärthomegenskaper kan överföras till mänskliga stamceller. vi visar i en musmodell att designeradhesinproteinet spontant sätter in i plasmamembranet på stamcellerna utan cytotoxitet, och dirigerar sedan de modifierade cellerna till hjärtat efter transplantation. Så vitt vi vet, detta är första gången som inriktningsegenskaperna hos infektiösa bakterier har överförts till däggdjursceller.
"Denna nya teknik har en enorm potential för de sju miljoner människor som för närvarande lever med hjärtsjukdomar i Storbritannien."