Upphovsman:A.James Clark School of Engineering, University of Maryland
Forskare vid University of Maryland (UMD) och National Institute of Standards and Technology (NIST) har upptäckt ett sätt att upptäcka den molekylära mekanismen genom vilken 5HT3A, en serotoninreceptor belägen vid neuronsynapsen, är aktiverad. Att ha en molekylär modell av denna aktivering gör det möjligt att testa läkemedelshämmare med hjälp av datormodeller istället för traditionella experiment, potentiellt minska kostnaden och tiden för screening av nya läkemedel.
Studien som leds av Jeffery Klauda, professor i kemisk och biomolekylär teknik (ChBE) vid University of Maryland (UMD), publicerades i Förfaranden från National Academy of Sciences ( PNAS ) i dag. Nicholas Guros, en forskarassistent från ChBE, fungerade som första författare till studien och rådgavs av Arvind Balijepalli, maskiningenjör på NIST.
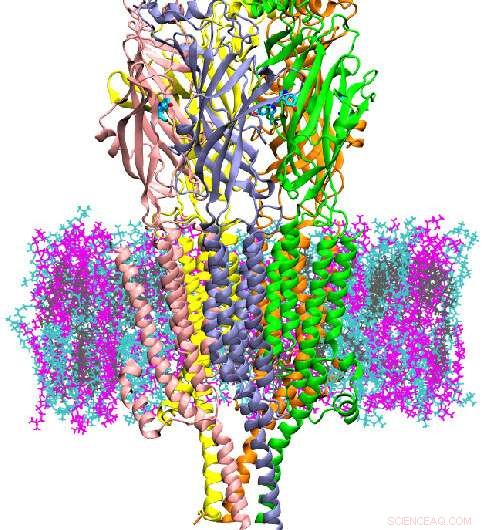
5HT3A är en typ av protein som kallas en jonkanal, inblandad i depression, ångest och målsatt för att minska illamående som orsakas av kemoterapi. Det reglerar flödet av joner vid den postsynaptiska klyftan av neuroner. Författarna utförde datasimuleringar av 5HT3A i upp till 20 mikrosekunder - mycket längre än tidigare simuleringar som utförts för
"Om du tänker på molekylär dynamik (MD) som ett molekylärt mikroskop, detta betyder att vi kan observera aktiveringsmekanismen för x10 längre än tidigare, "sa Guros." Nya beräkningsmöjligheter kan ge kraft att observera molekylär aktivering av komplexa proteiner vid betydligt större tidsskalor. Ju längre denna tidsperiod, desto bättre validering vi kan få av experimentella resultat för att visa att MD -modeller är en robust metod för att studera protein och testa läkemedel. "
Aktivering och desensibilisering av proteiner som 5HT3A sker över millisekunder, så när det är närmare den sanna tidsramen, forskare är fortfarande något bakom att observera hela transportcykeln för proteinet. Den här studien, dock, kunde ge insikt om effekterna av serotoninbindning på att utveckla ett preaktivt tillstånd av 5HT3A och hur membranlipids mångfald påverkar proteinstruktur och funktion.
Mycket simuleringsutrymme att utforska med dessa modeller återstår, och det har bara blivit möjligt under de senaste åren med framsteg i beräkningskraft. Specifikt, denna studie utfördes med hjälp av en bidragsbaserad fördelning på Anton2-superdatorn som underhålls av Pittsburgh Supercomuting Center (PSC) och sponsras av DE Shaw-forskning. Traditionella högpresterande datorresurser skulle inte kunna nå tidsskalorna för denna studie.
När datorhastigheten och kraften ökar i framtiden, gruppen hoppas kunna studera effekterna av läkemedel, såsom granisetron eller ondansetron, i ett försök att exakt modellera deras effekter på proteinet och undersöka andra riktade terapier.