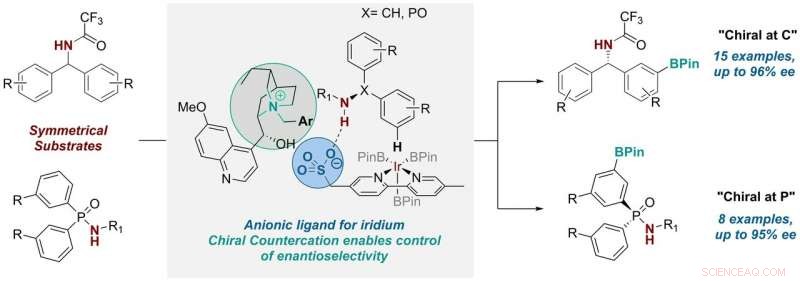
Kredit:University of Cambridge
Forskare här har kommit fram till en strategi för att göra en övergångsmetallkatalyserad kemisk reaktion enantioselektiv genom användning av en kiral katjon. Arbetet utfördes i Dr Robert Phipps forskargrupp.
Tidigare, Robert säger, medan kirala katjoner har använts i stor utsträckning som organokatalysatorer, Att föra dem in i kemiska reaktioner katalyserade av övergångsmetaller för att kontrollera reaktionens enantioselektivitet har varit mycket sällsyntare. Nu, efter två års hårt arbete "och mycket lagarbete, " de har lyckats med det.
Deras arbete, publiceras i Vetenskap , är "i huvudsak ett bevis på att du kan göra detta, och att det kan göras på en utmanande reaktionstyp som har visat sig vara tuff med befintliga metoder, " han säger.
Phipps-gruppen utvecklar metoder för syntes av små molekyler, såsom droger. De senaste åren, de har ägnat betydande ansträngningar åt att utveckla katalysatorer som kan kontrollera positionsselektiviteten i kemiska reaktioner – dvs. kontrollerar exakt vid vilken punkt på molekylen den kemiska reaktionen äger rum. De har gjort detta genom att utveckla ligander för övergångsmetallkatalysatorer som förankrar katalysatorn till en viss position på molekylen.
Och de har letat efter sätt att förfina liganderna ytterligare, så att de kan göra dem inte bara positionellt selektiva utan också enantioselektiva. Enantiomerer är spegelbilder - som en vänster och en höger - av en molekyl. Att kunna välja vilken av de två enantiomererna av molekylen de producerar, och därför vilken typ av "handedness" den har, är nyckeln.
För medan en enantiomer av molekylen kan ge den önskade terapeutiska effekten, den andra enantiomeren kan antingen inte ge någon effekt alls, eller kan ge oönskade biverkningar. Dessutom, chiraliteten, eller 'händighet, " av enantiomeren kan vara avgörande för att säkerställa precision i hur den interagerar inom ett biologiskt system.
"Naturen själv uppvisar kiralitet på flera sätt. Proteiner bildas av aminosyrabyggstenar som finns naturligt som en enantiomer, dvs de är enhands. Plus DNA har spiralformad kiralitet, " förklarar Robert. "Så som syntetiska kemister, det är verkligen viktigt att vi kan göra små molekyler som enstaka enantiomerer. När vi ska sätta in en liten molekyl i ett biologiskt system där vi hoppas att den ska ha, till exempel, en terapeutisk effekt, den "vänstra" enantiomeren kan passa in helt annorlunda jämfört med den "högra" enantiomeren."
Tre år sedan, gruppen utvecklade en ligand för övergångsmetallkatalysatorer som kontrollerade positionsselektiviteten i en CH-aktiveringsreaktion – en användbar reaktion som används flitigt inom läkemedelsindustrin och som vanligtvis uppnås med hjälp av övergångsmetallkatalys. De gjorde detta genom att ta en vanlig bipyridinligandställning och fästa en anjonisk sulfonatgrupp till den.
Efter att ha fäst denna anjoniska (eller negativt laddade) grupp till ställningen, de behövde sedan en positivt laddad komponent för att balansera den. I deras tidigare arbete, forskarna använde en vanlig katjon (tetrabutylammonium) för denna roll, vilket ursprungligen bara var för att ge saltets löslighet i organiska lösningsmedel. Men de insåg att "vi hade en möjlighet att ta in en kiral katjon här som potentiellt skulle kunna vara involverad i reaktionens övergångstillstånd och utöva ett visst inflytande på den, " förklarar Robert. Så de gav sig i kast med att undersöka om detta var möjligt.
Ph.D. student Georgi Genov arbetade först med idén, vilket i slutändan involverade ytterligare två Ph.D. studenter, James Douthwaite och David Gibson, och en postdoktor, Antti Lahdenperä. De ersatte den akirala tetrabutylammoniumkatjonen med en kiral katjon som härrör från det naturligt förekommande anti-malariakininet. Och genom att göra det, de fann att de kunde kontrollera inte bara den positionella selektiviteten utan också enantioselektiviteten i reaktionen, som ersätter en C-H-bindning på en aromatisk ring med en mångsidig C-B-bindning.
Georgi säger:"Optimeringsprocessen för denna transformation var ganska involverad. efter att ha upptäckt de rätta katjon- och reaktionsförhållandena, vi observerade att systemet var anmärkningsvärt allmänt, vilket gjorde det möjligt för oss att använda två mycket olika substratklasser - en där det nya stereocentret är vid en kolatom, och en där den är på fosfor. Det senare är mycket spännande eftersom syntesen av kirala och fosforföreningar är mer utmanande."
Hittills, det har funnits mycket väletablerade sätt att göra enantioselektiva reaktioner med övergångsmetaller - men de förlitar sig normalt på att introducera någon form av kiralitet direkt i ligandställningen som är fäst vid metallen och "det kan finnas nackdelar med detta tillvägagångssätt som betyder att det inte kommer att fungera i vissa situationer, " säger Robert.
"Vi vet att dessa kirala katjoner, av den typ vi använder, är verkligen privilegierade eftersom de har använts i andra typer av asymmetrisk katalys. Men de har knappt använts alls med övergångsmetaller. Så om vi potentiellt kunde förena dessa privilegierade kirala katjoner med reaktiva övergångsmetaller, då kanske vi har ett nytt och helt annorlunda sätt att tänka på att göra asymmetrisk övergångsmetallkatalys."
Han tillägger:"Vi är glada att titta på att rulla ut detta till andra riktigt användbara övergångsmetallkatalyserade reaktioner där det finns utmaningar att utföra dem enantioselektivt. Specifikt, vi skulle vilja se om vi kan möjliggöra enantioselektiva reaktioner som inte har varit möjliga tidigare, använder denna strategi."