Upphovsman:University of California, Los Angeles
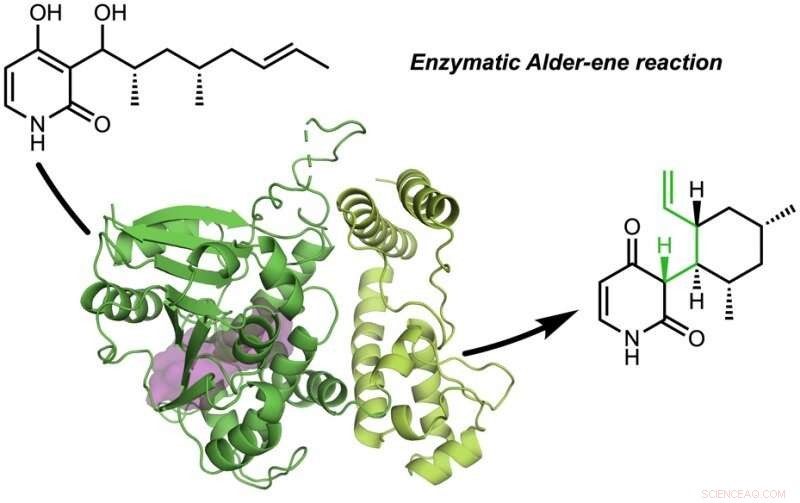
The Tang, Garg, och Houks forskargrupper har upptäckt naturens naturliga proteinkatalysatorer (enzymer) som katalyserar Alder-en-reaktionen.
Alla grupper ingår i UCLA Institutionen för kemi och biokemi. Professor Yi Tang är kansliprofessor vid UCLA -avdelningen för kemisk och biomolekylär teknik och har också ett gemensamt utnämning vid Institutionen för bioingenjör. Professor Ken Houk innehar Saul Winstein Distinguished Research Chair i organisk kemi och professor Neil Garg innehar Kenneth N. Trueblood Endowed Chair i kemi och biokemi och fungerar som avdelningsordförande.
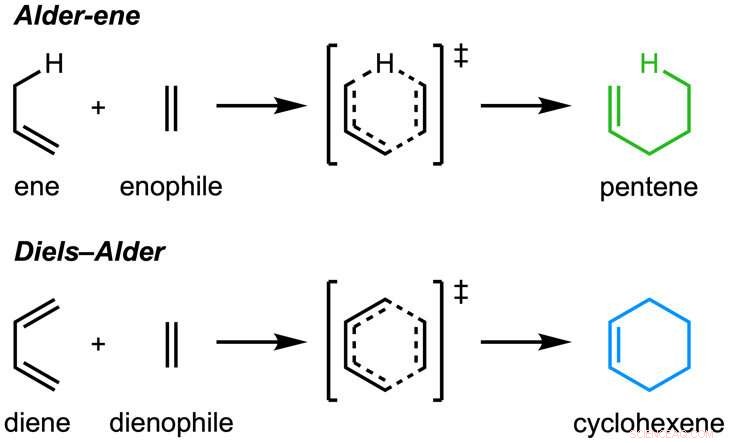
Pappret, "En enzymatisk Alder-en-reaktion" publicerades i Natur . Alder-en-reaktionen upptäcktes 1943, men har hittills endast använts för kemisk syntes i laboratoriet. Alder-en-reaktionen är ett exempel på en pericyklisk reaktion och en analog av den allmänt kända Diels-Alder-reaktionen. Tidigare, Tang och Houk identifierade en ny klass av enzymer - pericyklaserna - för deras förmåga att påskynda pericykliska reaktioner i primär och sekundär metabolism.
I ett samarbete med Jiahai Zhou från Shanghai Institute of Organic Chemistry, Tang-Garg-Houk-grupperna rapporterade strukturerna och mekanismerna för två grupper av enzymer som katalyserar en stereoselektiv uttorkning och samtidig pericyklisk reaktion, visas nedan, där de små symbolerna som PdxI indikerar naturliga enzymer (proteinkatalysatorer) upptäckta av Tang -gruppen. En grupp enzymer katalyserar en Alder-en-reaktion, och den andra katalyserar hetero-Diels – Alder-reaktioner.
Upphovsman:University of California, Los Angeles

Upphovsman:University of California, Los Angeles
Papperet beskriver den divergerande syntesen av pyridoxatin och asperpyridon A. Från och med alkoholsubstratet, enzymerna underlättar en uttorkning för att bilda en reaktiv kinonmetidmellanprodukt från vilken pyridoxatin och asperpyridon A-skelett kan bildas genom Alder-en eller Diels-Alder-reaktion. Masao Ohashi i Tang -gruppen, och Cooper Jamieson i Houk- och Tang -grupperna arbetade tillsammans för att identifiera de faktorer i enzymerna som styr vilken reaktion som uppstår. Beräkningsprognoser styrde experimentella modifieringar som förändrade enzymerna för att katalysera den andra reaktionen. Denna typ av proteinteknik lovar att påverka laboratoriesyntesen av relaterade naturprodukter i framtiden.
Upphovsman:University of California, Los Angeles
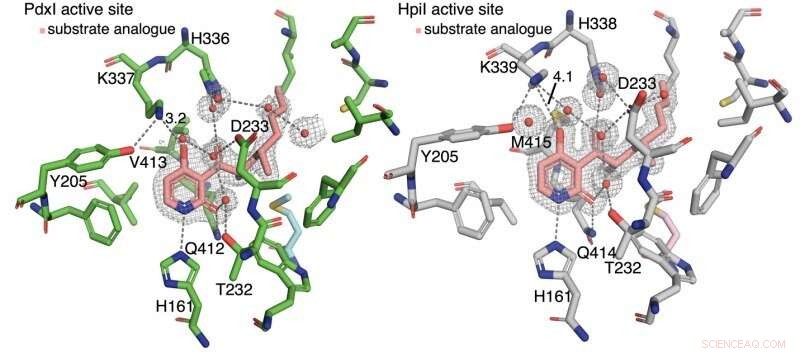
Författarna upptäckte att vätebindning till pyridon C4 styr reaktionstypen. I enzymerna PdxI, AdxI, och MdxI, en lysinrest (K337) vätebindningar till C4. Detta minskar nukleofiliciteten hos syret och ogynns hetero-Diels-Alder-reaktionen. PdxI, AdxI, och MdxI använder denna strategi för att selektivt bilda pyridoxatinskelettet. Enzymer EpiI, UpiI, och HpiI blockerar denna vätebindning från att uppstå med en flexibel metioninrest (M415) och underlättar därigenom bildandet av asperpyridon A -skelettet. Denna subtila geometriska skillnad på de aktiva platserna gör en ganska stor elektronisk förändring i substratet och styr den enzymatiska pericykliska reaktionen.