Kredit:Nagoya Institute of Technology
Många av våra mediciner och andra bioaktiva läkemedel är baserade på kemiska strukturer som kallas enantiomerer – molekyler som är spegelbilder av varandra och som inte går att lägga över varandra. Noterbara bland dem är kiral N, N-acetaler som ingår i diuretika som bendroflumetiazid och tiabutazid, används för att behandla högt blodtryck och ödem. Eftersom en enantiomer och dess spegelbildsversion ofta har olika biologiska aktiviteter, med bara en av dem som har farmakologisk användbarhet, en enantioselektiv eller asymmetrisk syntes som ger den önskade enantiomeren i större mängder är mycket önskvärd.
När det gäller N, N-acetaler, flera studier har visat deras enantioselektiva beredning från aldehyder, aldiminer, eller enaminer. Dock, i alla dessa fall, deras reaktionspartner har begränsats till aldehyd eller iminer. Medan ketoner har använts, med fall av framgångsrik enantioselektiv N, N-acetal syntes, deras användning – i allmänhet – anses inte vara effektiv.
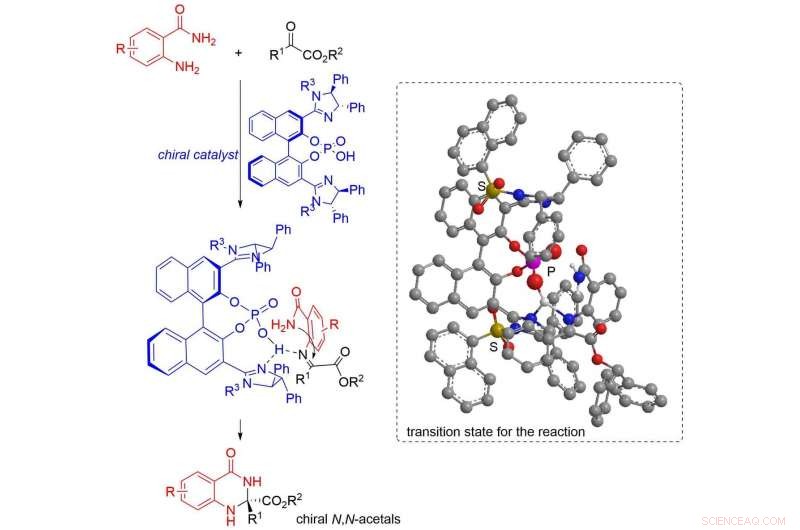
I en nyligen publicerad studie publicerad i Avancerad syntes och katalys , forskare från Nagoya Institute of Technology (NITech) och Osaka University i Japan undersökte denna situation med en enantioselektiv syntes av kiralt N, N-acetaler från α-dikarbonylföreningar - föreningar med två karbonyl(keton)grupper på α-kolet - i närvaro av kirala imidazolin-fosforsyrakatalysatorer, och erhållna utbyten så höga som 99% med en maximal enantiopurity på 96%.
"Vår studie presenterar den första mycket stereoselektiva bildningen av kiralt N, N-acetaler från α-ketoestrar med en originalkatalysator som också kan användas för andra stereoselektiva syntetiska reaktioner, " säger professor Shuichi Nakamura från NITech, som ledde studien.
Forskarna började med att undersöka reaktionen mellan 2-aminobensamid och olika α-ketoestrar i närvaro av olika katalysatorer. α-ketoestrarna skilde sig från varandra i karaktären av den funktionella gruppen kopplad till α-kolet, medan de valda katalysatorerna var bis(imidazolin)-fosforsyra med olika substituenter bundna till kvävet i imidazolinringen, mono-imidazolin-fosforsyra, och två kommersiella kirala fosforsyror. Bland dessa olika kombinationer, forskare fann det bästa utbytet (99 %) och enantiorenhet (92 %) i fallet med α-ketoester med benshydrylgrupp och en bis(imidazolin)-fosforsyrakatalysator med 1-naftalensulfonylgrupp.
Forskare undersökte därefter reaktionen av olika aminobensamider (som bär antingen en elektrondonerande metylgrupp eller elektronbortdragande fluor, klor, och bromgrupper) med olika a-ketoestrar (innehållande samma benshydrylgrupp men olika funktionella grupper istället för en tidigare fenylgrupp) som håller samma bis(imidazolin)-fosforsyrakatalysator med 1-naftalensulfonylgrupp. Alla kombinationerna visade bra utbyte (77-95%) tillsammans med hög enantioselektivitet (82-96%).
Dessutom, teamet tittade på den enantioselektiva syntesen av N, N-acetaler via reaktionen av N-bensyl isatin (en cyklisk α-ketoamid), bensil (en acyklisk diketon), och bensaldehyd med 2-aminobensamid för samma katalysator. Alla tre reaktionerna gav produkter med hög enantiopenhet (91-93%).
Teamet föreslog också en möjlig mekanism för N, N-acetalbildningsreaktion motsvarande det bästa utbytet (99 %), involverar en ketiminintermediär med en amidgrupp som hjälper till att undvika sterisk repulsion mellan fenylgruppen på imidazolin, möjliggör bildning av en (R)-isomer med hög enantiorenhet.
Även om mekanismen fortfarande är spekulativ och kräver ytterligare undersökning, forskare är entusiastiska över de potentiella konsekvenserna av experimentresultaten. "Vår nya metod kommer att möjliggöra syntes av läkemedelskandidater som för närvarande är svåra att syntetisera, och kan till och med potentiellt bidra till att skapa och förse människor med nya och bättre läkemedel i framtiden, " avslutar Prof. Nakamura.
Nu, det är några lovande konsekvenser att se fram emot!