Bild:Harder Group
Kemister vid Friedrich-Alexander-Universitetet Erlangen-Nürnberg har publicerat ett genombrott inom magnesiumkemin i tidskriften Natur .
Magnesium (Mg) är en jordrik tidig huvudgruppsmetall med låg elektronegativitet som lätt förlorar sina valenselektroner. I kombination med andra element, det förekommer naturligt bara i sin mest stabila form som den positivt laddade Mg 2+ katjon. Mg 2+ katjon finns i olika mineraler men även i klorofyll, pigmentet som gör växter gröna. Magnesium i det onormala oxidationstillståndet +I detekterades först i interstellära moln, men nyligen, första komplexen med Mg + har isolerats.
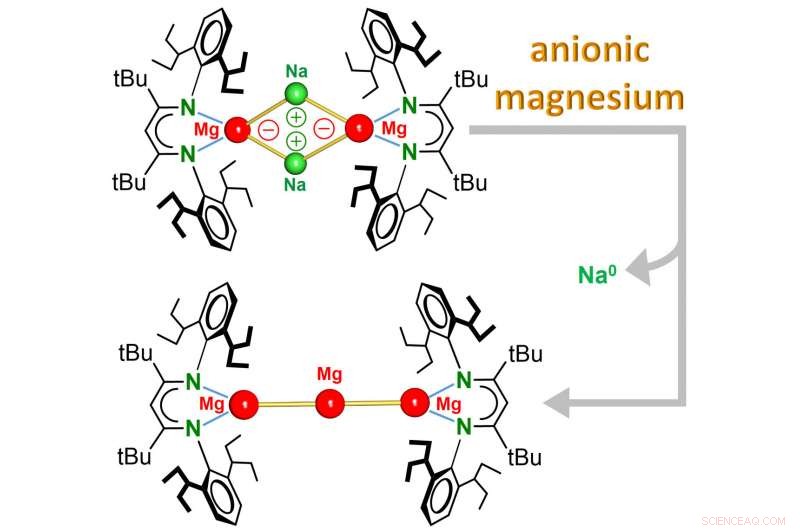
Teamet kring Prof. Sjoerd Harder (ordförande för oorganisk och metallorganisk kemi) rapporterar nu upptäckten av den första Mg 0 komplex där metallen har ett oxidationstillstånd på noll och till och med är negativt laddad. Dessa komplex, som innehåller unik magnesium-natriumbindning (Mg-Na), reagerar helt annorlunda än vanliga Mg 2+ föreningar. Medan elektronfattigt Mg 2+ katjoner kan ta emot elektroner, det elektronrika anjoniska Mg 0 centrum reagerar genom att donera elektroner.
Komplexet är lösligt i vanliga organiska lösningsmedel och är ett extremt starkt reduktionsmedel:Lätt uppvärmning ledde till omedelbar reduktion av Na
+
katjoner till Na
0
, en metall som normalt har en stark tendens att oxidera till Na
+
katjoner. Under denna termiska nedbrytning, en ny typ av komplex bildas där tre Mg-atomer ansluter som pärlor i en kedja. Denna Mg
3
kluster reagerar som atomärt Mg
0
och kan ses som den minsta biten av Mg-metall, som är lösligt i organiska lösningsmedel. Denna nya klass av anjoniska Mg-komplex vänder Mg-kemin helt upp och ner. Ytterligare ovanlig reaktivitet hos denna lösliga, extremt stark, reduktionsmedel kan förväntas.