
Funktionalisering av eterbindningar. (A) Småmolekylära läkemedel som innehåller cykliska eterdelar. Ph, fenyl; Ac, acetyl; Bz, bensoyl; glu, glukos. (B) övergångsmetallkatalyserad C -O -klyvning via oxidativ tillsats. R, alkyl; M, övergångsmetall; FG, funktionell grupp; B2pin2, bis (pinacolato) diboron. (C) karbeninsättning i aktiverade etrar. (D) Cykliska boronatderivat som läkemedelskandidater eller tvärbindare för biomedicinska material. (E) Detta arbete:en Ni-katalyserad direkt borinsättning via en klyvning-sedan-rebound-väg. Kredit:Vetenskap, 10.1126/science.abg5526
Kol-syre (C-O) bindningen i alkyletrar kan klyvas med milda metoder för att förenkla kemiska synteser genom att utarbeta robusta, lätt tillgängliga prekursorer. I en ny rapport nu Vetenskap , Hairong Lyu och ett forskargrupp i kemi vid University of Chicago och University of Pittsburgh, USA detaljerade hur dibromoboraner reagerade med alkyletrar i närvaro av en nickel (Ni) katalysator och zinkreduktant för att sätta in bor i C-O-bindningen. Den efterföljande reaktiviteten påverkade syre-till-kväve-substitutionen för att effektivisera beredningen av bioaktiva föreningar i större utsträckning. Med hjälp av mekanistiska studier, laget avslöjade en klyvning-sedan-rebound-väg via zink/nickel-tandemkatalys.
Etergrupper
Etergrupper finns vanligen i råvaror och finkemikalier; till exempel, cykliska etrar förekommer i en rad biologiskt viktiga molekyler inklusive läkemedel, jordbrukskemikalier och naturprodukter. Ethers fungerar också som effektiva strukturella länkar för att skydda grupper i organisk syntes på grund av deras höga kemiska stabilitet mot syror, baser, reduktanter och oxidanter. En mild metod som direkt redigerar en del genom att ersätta syret eller sätta in en mellanliggande atom i C-O-bindningen kan bekvämt introducera en ny funktionell grupp i en befintlig byggnadsställning i ett strategiskt viktigt steg. Kemister kan använda robusta etrar som surrogater för mer känsliga kemiska grupper som kan installeras senare. Lyu et al. inspirerades av de senaste framstegen inom borylenkemi för att funktionalisera eterbindningar genom att sätta in en aktiv borylenart.
Klyvning av alkyleterbindningar
Konventionellt, alkyleterbindningar kan klyvas under hårda och starkt sura förhållanden. För att fastställa en praktisk metod i detta arbete, Lyu et al. försökte undvika starka reduktanter, dyra katalysatorer och forcerade reaktionsbetingelser. Studien började därför med 2, 3-dihydrobenzofuran som modell etersubstat och dibromomesitylborane (MesBBr 2 ) som borreagens. Den skrymmande gruppen förhindrade dimerisering av reducerade borarter för att förbättra stabiliteten av den borinsättande produkten för isolering. Den kombinerade nickelkatalysatorn och zinkpulvret var mest effektiva. Teamet erhöll slutligen den önskade borinsättningsprodukten 2H-bensoxaborin (märkt 3a) med 90% utbyte i toluenlösning vid 60 grader Celsius. Reaktionsvägen var helt annorlunda; de använde ett luftstabilt tetraedriskt Ni (II) -komplex förkortat (Cat 1-molekyl) och bekräftade dess struktur med hjälp av röntgenkristallografi för att belysa dess överlägsenhet gentemot andra Ni-förkatalysatorer eller andra metaller. I frånvaro av Cat1, de noterade mindre än 1 procent utbyte av 2H-bensoxaborin och en ringöppnande alkylbromidmellanprodukt (förkortad som 4a) för att bildas med högt utbyte. Andra nickelkomplex gav också önskad produkt, fast i mycket lägre avkastning. Lyu et al. noterade liknande effektivitet med användning av en in situ -genererad nickelkatalysator (förkortad som L1). Med tanke på nickelkatalysatorens kritiska roll, laget undersökte också andra kvävebaserade ligander. Monodentatliganderna agerade bättre än bidentatligander (märkta L1 till L7 och jämfört med L8 till L12). Till exempel, 3-metylpyridin (L5) uppvisade något lägre reaktivitet, medan de flesta andra monopyridiner (L2, L3, L4 och L6) samt oxazolin (förkortat L7) var jämförelsevis mindre effektiva. De använde också zinkpulver som en väsentlig katalysator och noterade utvecklingen av borinsättningsreaktionen vid en låg reaktionshastighet vid rumstemperatur.
Nickelkatalyserad borylering av cykliska etrar. (A) Syntes av oxaborinaner via direkt borylering av femmedlemmade cykliska etrar. Mig, metyl; Ar, aryl. (B) Syntes av oxaborepans via direkt borylering av sexmedlemmade cykliska etrar. Ts, tosyl. (C) Syntes av oxaborolaner och azaborolidin via direkt borylering av cyklooxabutaner och azetidin. (D) Syntes av oxazaborolidin via direkt borylering av 4-fenyl-morfolin. (E) Syntes av borsyror via direkt borylering av linjära etrar. Reaktioner utfördes med 0,2 mmol eter, 0,24 mmol MesBBr2, 0,01 mmol Cat 1, och 1 mmol zinkpulver i 0,5 ml toluen vid 60 ° C under kväve i 24 timmar. Isolerade utbyten efter silikagelkromatografi ges; siffrorna inom parentes är nukleära magnetiska resonansutbyten före rening. *Reaktionen utfördes vid 80 ° C. † Reaktionen utfördes vid 100 ° C. ‡ 0,2 mmol MesBBr2 användes. §Reaktionen utfördes vid 130 ° C. ¶Ni (PMe3) 2Cl2 (0,01 mmol) användes som katalysator, och reaktionen kördes vid 130 ° C i 18 timmar. Reaktionstiden var 36 timmar. Kredit:Vetenskap, 10.1126/science.abg5526 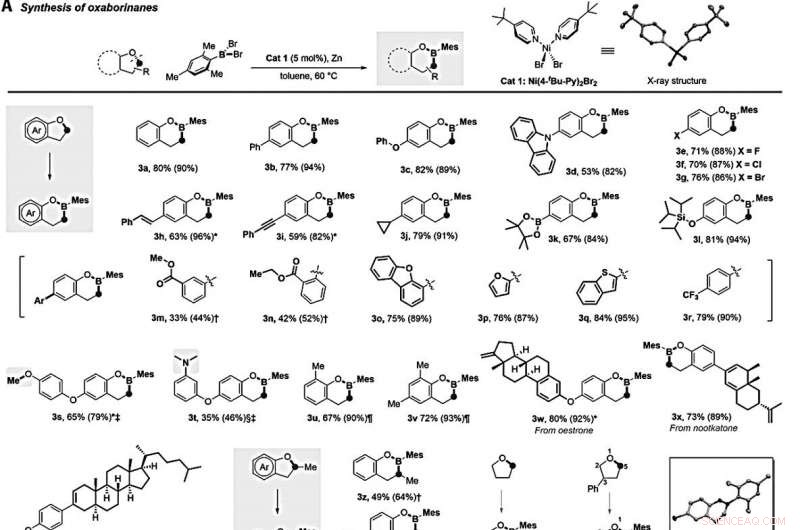
Lyu et al. undersökte eteromfånget för borinsättningsreaktionen. Till exempel, ett intervall av substituerade 2, 3-dihydrobensofuraner reagerade med MesBBr 2 (dibromomesitylborane) smidigt för att bilda de önskade borinsättningsprodukterna med bra till utmärkt utbyte. Till exempel, substrat som innehåller halogener inklusive fluor (F), klor (Cl) och brom (Br) genomgick nickelkatalyserade tvärkopplingar för att bilda 2H-bensoxaboriner (märkta 3e till 3g) med mer än 70 procent utbyte. Bland ett otal molekyler som sålunda bildats, laget noterade toleransen för både pinakolboronat- och silyletergrupper under denna reaktion. Ytterligare kontrollexperiment visar hur primär alkylklorid är fullt kompatibel, medan primär alkylbromid var delvis kompatibel under reaktionsbetingelser. Dessutom, den primära alkylfluoriden tolererades inte på grund av dess starka bor-fluorid-interaktioner. Lyu et al. därefter härledde komplexa substrat från terpen naturliga produkter som smidigt genomgick borinsättningsreaktionen och levererade önskade produkter i tre gånger eller högre. Dessutom, tetrahydrofuran gav också den förväntade mono-bor-införingsprodukten (märkt som 3ab) i 69 procent utbyte. När laget använde den osymmetriska 3-fenyl-tetrahydrofuran som kopplingspartner, borinsättningen skedde regioselektivt i det mindre skrymmande läget för att indikera påverkan av sterika.
Borinsättning i mer komplexa molekyler.
Lyu et al. genomförde dessutom borinsättning i mer ansträngda oxetaner, också, för att tillhandahålla en post till fem-lediga oxaborolaner (märkta 3ai till 3aj). Den komprometterade selektiviteten resulterade i linjära sidoprodukter. Från syntetisk praktik, teamet visade hur B-Mes (bor-mesityl) -bindningen lätt kunde genomgå en-potthydrolys via tillsats av vatten i metanol för att ge motsvarande hydroxylboronatprodukter som är mer stabila i luften. Forskarna funktionaliserade cykliska boronater från lätt tillgängliga 2, 3-dihydrobensofuraner i ett steg för att utveckla analoger av ett godkänt svampdödande läkemedel som kallas tavaborol och crisaborole, ett godkänt läkemedel för att behandla dermatit.
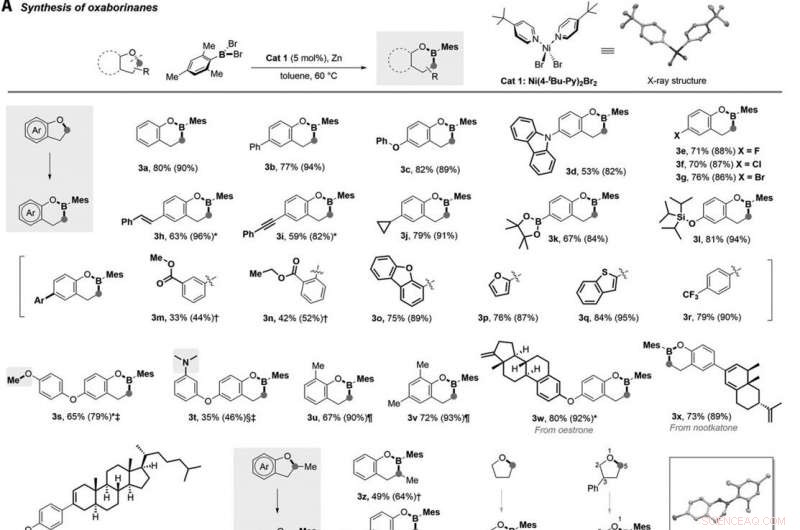
Syntetisk utarbetning. (A) Snabb åtkomst till cykliska boronater via hydrolys med en kruka. Boronatprodukterna (5a till 5c) är väsentligen mer stabila mot luft och fukt. (B) Ytterligare funktionalisering av boryleringsprodukten genom derivatisering av C -B -bindningen. Bn, bensyl. (C) O-till-N-redigering för åtkomst till pyrrolidiner och piperidiner från tetrahydrofuraner och tetrahydropyraner, respektive. (D) Tre tillvägagångssätt för expansion av en kolring av cykliska etrar. DIAD, diisopropylazodikarboxylat. (E) Strömlinjeformad syntes av det antihypertensiva läkemedlet nebivolol. För detaljerade reaktionsprotokoll. Kredit:Vetenskap, 10.1126/science.abg5526
Andra reaktioner
Bordelen i införingsprodukterna kan också bekvämt omvandlas till olika andra funktionella grupper. Till exempel, laget kunde behandla råprodukten (3a) 2H-bensoxaborin, med väteperoxid för att erhålla 1, 2-tyrosol (6a) i utmärkt utbyte. Suzuki-Miyaura-kopplingen av 3a-molekylen med brombensen effektivt bildad o-fenetylfenol (märkt som 7a). Metoden möjliggjorde också effektiva expansionsreaktioner med en kolring och gav bor-retentiv ringexpansion. Under experimenten, alkylgruppens beskaffenhet i kopplingsreaktionen och nickelkatalysatorns roll var avgörande för att förstå de efterföljande stegen för bildning av kolbor.
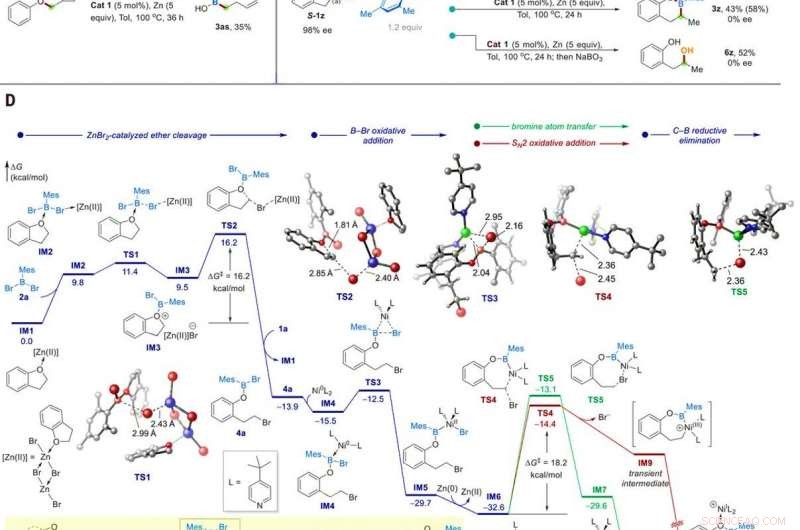
Mekaniska studier. (A) Identifiering av reaktionsmellanprodukten. (B) Radikal-klocka experiment. (C) Kontrollförsök med ett 98% ee -substrat. (D) Beräknad energiprofil för den katalytiska boryleringen av eter la. Beräkningar utfördes vid M06/SDD-6311+G (d, p)/SMD (toluen) // B3LYP-D3/SDD-6-31G (d) teoretisk nivå. Insats visar föreslagen Zn/Ni -tandemkatalys. Kredit:Vetenskap, 10.1126/science.abg5526
Syn
På det här sättet, Hairong Lyu och kollegor demonstrerade en metod för borinsättning i alkyleterbindningar under katalys av nickel och zink. Eftersom etrar är lättillgängliga och robusta substat, borinsättningsmetoden kan också effektivisera syntesen av komplexa målmolekyler genom att minimera de funktionella gruppmanipulationerna eller genom att skydda gruppanvändningar. Det distinkta reaktionsläget som avslöjas av de mekanistiska studierna kan ha konsekvenser för Lewis syra/övergångsmetall -tandemkatalysreaktioner som ligger utanför detta arbete.
© 2021 Science X Network