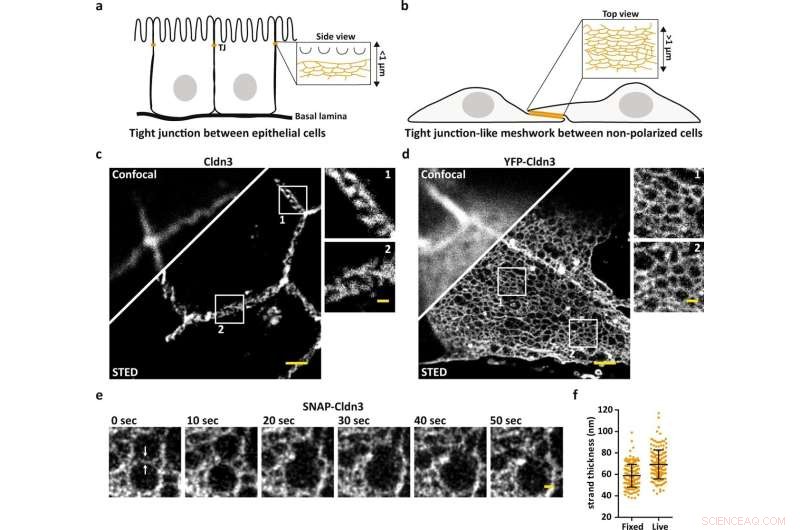
STED-mikroskopi avslöjar organisationen av TJ meshworks i nanoskala. ett schema som illustrerar den endogena TJ vid den mest apikala cell-till-cell-kontakten i epitelceller. b Schema som illustrerar TJ-liknande nätverk bildat i plana överlappande områden av claudin-transfekterade opolariserade celler. c, d Representativ konfokal och STED-bild av en endogen bildad TJ märkt för Cldn3 (2nd-Atto647N) mellan epitelceller från vävnad från mus duodenum (c) och TJ-liknande nätverk bildat av överuttryckt YFP-Cldn3 (α-GFP-NB- Atto647N) mellan två COS-7-celler (d). e Representativ enfärgad STED-tidsserie (1 ram/10 s) av ett TJ-liknande nät i en överlappande region av levande COS-7-celler som uttrycker SNAP-Cldn3 (BG-JF646). Vita pilar indikerar det initiala strängbrottet följt av sammansmältningen av två mindre maskor till ett större nät. En Gaussisk oskärpa med en sigma på 20 nm applicerades. f Full-wide-half-maximum (FWHM) mätning av TJ-strängar av SNAP-Cldn3 (BG-JF646) i fixerade och levande COS-7-celler. Data representerar medelvärdet ± SD. Varje datapunkt representerar en linjeprofil av totalt 160 linjeprofiler från 8 oberoende TJ-liknande nätverk (n = 160). Den totala FWHM resulterade i 59 ± 11 nm för fasta och i 69 ± 14 nm för levande prover. Alla representativa bilder härrör från 3 oberoende experiment. Skalstaplar, 1 µm (c, d) och 200 nm (förstoringar i c, d och e). Kredit:Nature Communications (2022). DOI:10.1038/s41467-022-32533-4
De förseglar epitelceller och tillåter under vissa förhållanden passage av joner och vatten:Täta förbindelser bildar en paracellulär barriär i vävnader och deras dysfunktion är förknippad med sjukdomar. Även om deras molekylära komponenter har varit kända sedan 1990-talet, är det inte uppenbart hur de 26 proteinerna som kallas claudiner är organiserade.
Forskare från Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP) har nu fått djupa insikter i strukturen hos tight junctions, med hjälp av STED-mikroskopi (super-resolution stimulated emission depletion). Det är första gången som den grundläggande mekanismen bakom alla epitelial barriäregenskaper har beskrivits.
Tight junctions (TJ) är normalt utmärkta för att möjliggöra passage av nödvändiga joner eller molekyler, samtidigt som de bildar en tät barriär för att förhindra att oönskade bakterier och deras toxiner kommer in i kroppen. Dessa paracellulära barriärer, som samtidigt kan vara selektiva jon- och vattenkanaler, finns varhelst epitelceller eller endotelceller möts, d.v.s. där olika vävnader är anslutna till varandra eller när ett organs lumen behöver tätas från blodomloppet.
Förekomsten av tight junctions upptäcktes för cirka 60 år sedan, och deras huvudsakliga molekylära komponenter har varit kända i 30 år:26 membranproteiner som kallas claudiner. Beroende på cellen är claudins organiserade i olika konstellationer för att bilda semipermeabla nätverk upp till flera hundra nanometer breda. Vanligtvis kommer flera claudiner samman, men vissa barriärer består av bara ett eller två strukturella proteiner.
Men frågan är, hur är claudins organiserade för att skapa olika barriäregenskaper beroende på vilken cell eller vävnad det gäller? Och i vilken utsträckning är claudins beroende av varandra i processen? Fram till nu har dessa frågor förblivit obesvarade eftersom det var omöjligt att se igenom strukturen av trådar, som bara är cirka tio nanometer tjocka. Nu har forskare från FMP lyckats göra just det med STED-mikroskopi.
"Den här typen av superupplösningsmikroskopi och ett utmärkt team av cellbiologer, datavetare och fysiologer har hjälpt oss att kasta ljus över den molekylära arkitekturen hos tight junctions", säger Dr. Martin Lehmann, chef för Cellular Imaging Group sist författare till studien. "Vi har nu för första gången kunnat beskriva mekanismen bakom de viktigaste epitelbarriäregenskaperna."
Användning av STED för att lösa enskilda meshworks
Normalt är upplösningen för fluorescensmikroskop begränsad till cirka 250 nanometer. Med STED-mikroskopi är 50 nanometer eller mindre möjliga. Detta gav bokstavligen forskarna större insikt.
"Med standard fluorescensmikroskopi skulle vi aldrig ha penetrerat den täta organisationen av den täta korsningen, men STED har gjort det möjligt för oss att lösa de individuella maskorna i nätverket. Som ett resultat kan vi nu bestämma den exakta positionen för proteiner, som samt att se om claudins blandas eller separeras, och hur de segregerar", säger Hannes Gonschior, studiens första författare, som genomförde sin doktorsexamen. avhandling om ämnet vid FMP. "Denna organisation i nanoskala var tidigare okänd."
Först utfördes studierna på cellnivå och sedan i tarm- och njurvävnad hos möss. Slående bilder återgav de fluorescerande märkta proteinerna i olika färger, som visar var vilka proteiner finns och hur de kedjar samman för att bilda en färgglad dragkedja.
Tre resultat från studien, nu publicerade i Nature Communications , är särskilt anmärkningsvärda:
Skapande av modell för läkemedelsupptäckt
Det faktum att FMP-forskare för första gången har kunnat bestämma organisationen av tight junctions i nanoskala är en stor framgång för grundforskningen. Men medicinen kan också dra nytta av genombrottet. Detta beror på att mutationer i claudins spelar en roll i ett antal ärftliga sjukdomar, den mest uppenbara är HELIX-syndromet – ett sällsynt tillstånd som orsakar minskad svettproduktion.
En mutation i claudin 10b är boven som orsakar hypohidros och defekter i tår- och spottkörteln, samt försämrad kalcium- och magnesiumreglering i njurarna. Teamet av forskare hade också experimenterat med denna sjukdomsmutant.
"Vår forskning är fortfarande långt ifrån att ha klinisk relevans," sade biofysikern Martin Lehmann, som bedömde sina resultat. "Men nu förstår vi åtminstone hur dessa nätverk är uppbyggda. Detta är det första steget som gör att vi kan söka efter små molekyler som öppnar eller stänger dessa barriärer."
Cellbiolog Hannes Gonschior tillade att de "har hittat en förenklad modell för läkemedelsupptäckt och mer allmänt bedrivit forskning om paracellulär passage av joner. Det är mycket troligt att våra fynd kommer att göra det möjligt för oss att förstå tidigare oförklarade kliniska fenotyper och symtom - med en defekt i en av dessa speciella paracellulära barriärer." + Utforska vidare