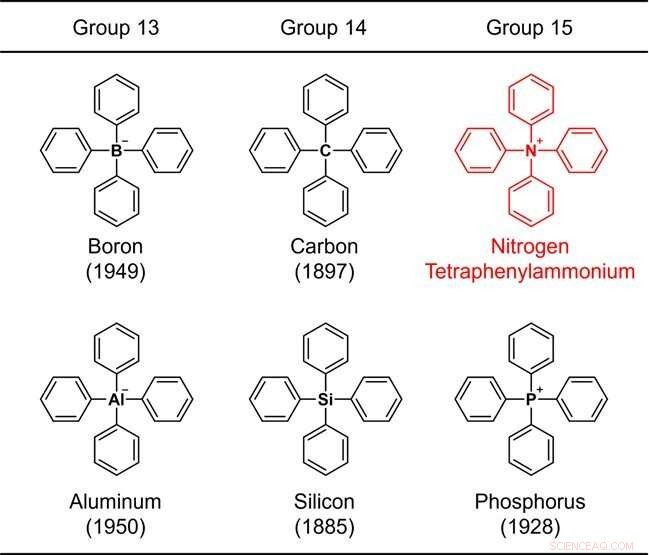
Figur 1. Strukturer av tetrafenylsubstituerade grundämnen tillhörande grupperna 13–15. Siffran inom parentes indikerar syntesåret. Kredit:Kanazawa University
Tetrafenylammonium, med alla fyra vätena av ammonium (NH4 + ) ersatt med bensenringar, har varken upptäckts i naturen eller syntetiserats kemiskt, vilket ifrågasätter om det skulle kunna existera. Här lyckades vi syntetisera tetrafenylammonium för första gången, vilket visar dess stabila existens. Den syntetiska strategin som används i denna studie, radikal koppling, kan vara tillämpbar på syntesen av olika besläktade ammonium med hög strukturell nyhet. Studien publiceras i Nature Communications .
Eftersom bensenringen är en representativ beståndsdel av organiska föreningar anses en struktur som endast består av ett gemensamt element plus bensenringen vara ett av de mest grundläggande kemiska skeletten. På grund av deras betydelse har den kemiska syntesen av sådana molekyler studerats sedan den tidiga tiden av organisk kemi. Till exempel, strukturen i vilken fyra bensenringar är bundna till ett representativt element (bor, kol, aluminium, kisel eller fosfor) av grupperna 13 till 15 i det periodiska systemet (Fig. 1) syntetiserades för mer än 70 år sedan, och den äldsta syntetiska rapporten går tillbaka 137 år.
Dessa skelett kallas gemensamt för "tetrafenyl", vilket betyder att strukturen innehåller 4 bensenringar. När det centrala grundämnet är kväve, ammonium, NH4 + , betraktas som moderjonen. En sådan förening kallas tetrafenylammonium. Denna förening, i själva verket en jon, har en mycket enkel kemisk struktur som även en nybörjare inom organisk kemi lätt kan föreställa sig.
Ändå har det visat sig vara mycket svårt att på konstgjord väg skapa denna struktur och inga syntetiska rapporter med tydlig strukturidentifiering har publicerats. Dessutom, eftersom det inte har upptäckts i naturen, har det inte varit klart förrän nu om tetrafenylammonium överhuvudtaget kan existera. Det har dykt upp publikationer som antar dess existens och endast nämner dess användning utan att beskriva dess syntes eller förvärvsmetod. Sammansatta databaser innehåller endast den kemiska strukturen. Således kallas denna jon ibland som om den redan vore känd. Men i verkligheten har ingen faktiskt observerat det, vilket gör tetrafenylammonium till en "fantomjon."
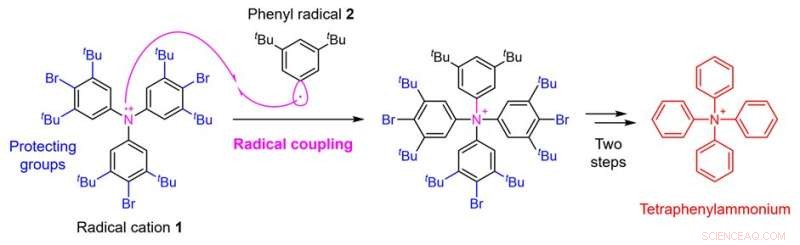
Figur 2. Tetrafenylammoniumsyntesstrategi med användning av radikalkoppling. Kredit:Kanazawa University
I denna studie har ett forskarlag vid fakulteten för farmaceutiska vetenskaper, Kanazawa University möjliggjort syntesen av tetrafenylammonium genom att etablera en ny syntetisk strategi. Den kritiska punkten i syntesen av tetrafenylammonium är tillägget av den fjärde fenylgruppen till kväveatomen som redan har tre fenylgrupper fästa. Det ansågs vara svårt att uppnå denna syntes med konventionella tekniker. I den aktuella studien använde forskargruppen därför en teknik som kallas radikalkoppling och använde en strategi för att reagera radikalkatjonen 1 framställd från ett trifenylaminderivat med fenylradikalen 2 (Fig. 2).
Som ett resultat, trots att utbytet var så lågt som 0,1 %, lyckades forskargruppen utföra den önskade kemiska omvandlingen. I sådana radikalkopplingar bildar högreaktiva radikaler bindningar med varandra, vilket har fördelen att möjliggöra bindningsbildning som inte kunde uppnås med andra metoder. Å andra sidan har det nackdelen att det är svårt att kontrollera selektiviteten eftersom reaktiviteten är för hög, vilket leder till olika sidoreaktioner.
Därför, i denna syntes, för att så mycket som möjligt undertrycka sidoreaktionen av bindningsbildning på kolet av radikal katjon 1, utformade forskargruppen också införandet av skyddsgrupper) som orsakar steriskt hinder. Slutligen genomfördes totalt fem steg av kemisk omvandling av ett känt trifenylaminderivat, utgångsmaterialet för syntesen, genom införandet av skyddsgrupperna, radikalkoppling och efterföljande avlägsnande av skyddsgrupperna, vilket ledde till tetrafenylammonium.

Figur 3. Röntgenkristallstruktur av tetrafenylammonium. Kredit:Kanazawa University
Baserat på data erhållna från olika instrumentella analyser bekräftades strukturen av tetrafenylammonium. röntgenkristallografi) visade att bindningslängden mellan kväveatomen och fenylgruppens kolatom som finns i denna jon endast är 1,529 Å (fig. 3).
Eftersom denna bindningslängd är kortare än för en tetrafenylstruktur som innehåller ett annat grundämne (bor, kol, aluminium, kisel eller fosfor), är det uppenbart att kväveatomen i tetrafenylammonium är i en mer rumsligt hindrad miljö än andra grundämnen. Detta tredimensionella hinder anses vara en av de faktorer som gör det svårt att konstruera detta skelett. Vidare visade våra resultat också att tetrafenylammonium har en hög stabilitet för att motstå starkt sura och basiska förhållanden.
Föreliggande studie har visat att tetrafenylammonium faktiskt existerar och kan syntetiseras kemiskt. Om storskalig syntes av denna jon och dess derivat realiseras i framtiden kan den potentiellt användas inom olika forskningsområden som en organisk katjon med hög kemisk stabilitet. Dessutom kan den radikala kopplingsstrategin som används i denna studie vara tillämpbar på syntesen av andra besläktade ammonium som inte har kunnat göras hittills. + Utforska vidare