Forskare har upptäckt sätt att omvandla inhibitorliknande cancerläkemedel till små molekyler som kallas nedbrytare, som hjälper till att förstöra cancerfrämjande proteiner i celler.
Forskarna valde ut molekyler som är kända för att hämma vissa proteiner – stoppa deras funktion – och modifierade dem på olika sätt för att omvandla dem till proteinnedbrytare, som bryter ner proteinet.
Andra forskare kan nu replikera detta nya tillvägagångssätt för att utveckla och optimera en rad proteinnedbrytare. På lång sikt kan detta hjälpa till att göra befintliga cancerbehandlingar mer effektiva och skapa nya behandlingar för att inrikta sig på olika proteiner som är involverade i cancer, inklusive proteiner som tidigare kan ha ansetts vara "odugliga."
Forskningen, som leddes av forskare vid Institute of Cancer Research, London, publiceras i ACS Chemical Biology .
Forskare över hela världen har undersökt riktad proteinnedbrytning som ett sätt att eliminera specifika proteiner som är kända för att spela en roll i utvecklingen eller progressionen av cancer. Celler bryter naturligt ner skadade eller onödiga proteiner, och det är möjligt att kapa denna process genom att introducera rätt läkemedelsmolekyler så att cellerna förstör cancerproteiner.
ICR har förbundit sig att undersöka riktad proteinnedbrytning som ett sätt att upptäcka nya cancerbehandlingar. År 2022 gjorde en stor filantropisk donation det möjligt att öppna ett nytt Center for Protein Degradation inom ICR:s Center for Cancer Drug Discovery.
Forskare har redan nått viss framgång med proteolysinriktade chimärer (PROTAC). Dessa binder till både proteinet av intresse och ett enzym som kallas E3 ubiquitinligas för att föra de två nära varandra. Enzymet märker sedan proteinet med ubiquitin, vilket markerar att det förstörs av cellen.
Den relativt höga molekylvikten hos PROTAC begränsar dock deras användning, eftersom de inte löser sig bra i vatten och kan kämpa för att komma in i celler i en tillräckligt hög koncentration för att vara effektiva. Omvänt, om koncentrationen blir för hög, binder PROTAC:erna till endast en av de två föreningarna – enzymet eller målproteinet – snarare än båda, vilket innebär att proteinnedbrytningen är ofullständig.
En nyare upptäckt har varit användningen av monovalenta nedbrytare, ofta kallade molekylära lim. Dessa fungerar på liknande sätt som PROTAC, men de modifierar kemiskt ytan på antingen enzymet eller målproteinet så att de två kan binda direkt. Dessa föreningar övervinner begränsningarna hos PROTAC eftersom de är mindre och fortfarande effektiva vid högre koncentrationer.
Ett molekylärt limläkemedel, upptäckt efter ett forskningsprogram vid ICR, befinner sig redan i kliniska prövningar i tidig fas.
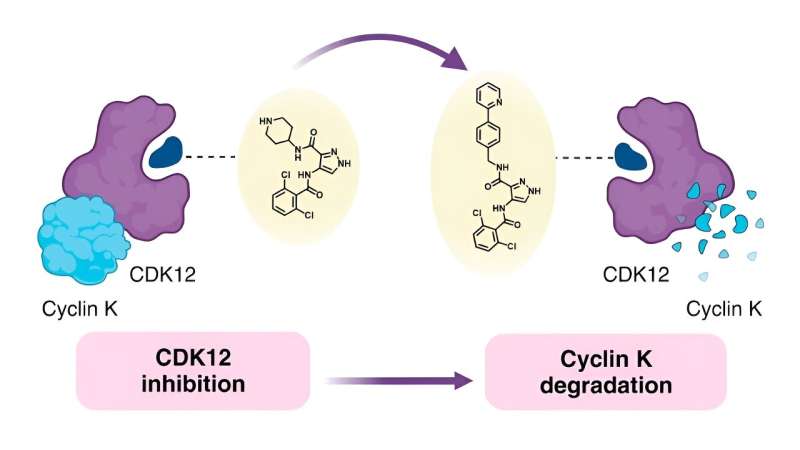
Eftersom de ville förstå kopplingen mellan den kemiska strukturen hos molekylära lim och hur de beter sig – känd som struktur-aktivitetsrelationen (SAR) – bestämde forskarna bakom den aktuella studien att använda en känd monovalent nedbrytare kallad CR8 som utgångspunkt. CR8 hämmar alla cyklinberoende kinaser (CDK), som har flera roller i tumörutveckling, men det bryter också ned proteinet cyklin K, vilket främjar cancersignalvägar.
Tidigare forskning har visat att CR8 binder till CDK12 och en E3-ligaskomponent som kallas skadat DNA-bindande protein 1 (DDB1). Detta gör att cellen kan bryta ner cyklin K bundet till CDK12.
Beväpnade med denna information försökte teamet ersätta pyridinet i CR8 med ett brett utbud av substitut. De försökte först använda enkla grupper, inklusive fluor, metyl och hydroxi, innan de gick vidare till mer komplexa formationer för att avgöra hur dessa förändringar påverkade nedbrytningsförmågan.
I den andra delen av studien tillämpade forskarna sin ökade förståelse av nedbrytande SAR på andra CDK-hämmare för att avgöra om deras resultat var överförbara. De fann att molekylära komponenter som inducerade proteinnedbrytning kunde användas för att omvandla flera olika inhibitorer till nedbrytare. De identifierade också vissa substitut som ledde till förbättrad nedbrytning.
Första författare Katie Thomas, en Ph.D. student vid avdelningen för cancerterapi vid ICR, sa:"Det var förvånande att se att ett så brett spektrum av grupper kunde användas för att inducera cyklin K-nedbrytning. Detta betyder att interaktionsgränssnittet mellan degrader bound-CDK12 och DDB1 inte måste vara perfekt optimerad för att nedbrytning ska inträffa. Detta är lovande för framtiden att använda monovalenta lim som terapeutiska metoder – det kommer att hjälpa oss att utveckla molekyler från upptäckt till optimering."
Proteinkinashämmare har använts i cancerbehandling i mer än två decennier. De verkar genom att blockera verkan av proteinkinaser, enzymer som kontrollerar proteinernas funktion och kan leda till oreglerad celltillväxt om de blir muterade.
Även om dessa behandlingar kan fungera bra finns det en risk att cancern blir resistent mot dem. Detta beror på att inhibitorer blockerar cancerrelaterade proteiner snarare än att förstöra dem, och tumörcellerna kan ibland återaktivera dem.
Dessutom, när vissa proteinkinaser blockeras av inhibitorer, kompenserar cellen genom att använda andra kinaser för att utföra samma åtgärder.
Att bli av med proteinerna helt genom proteinnedbrytning tar bort dessa risker.
Denna studie fungerar som en utgångspunkt för andra forskare som vill designa molekylära lim, identifiera lovande proteinmål för nedbrytning och utveckla nya molekyler som kan fungera som nedbrytningsterapier.
Thomas sa:"Vi antar att andra hämmare av små molekyler skulle kunna omvandlas till nedbrytare genom tillägg av vissa grupper. Vårt team undersöker för närvarande om vissa grupper kan kopplas till andra typer av kinashämmare för att förvandla dem till monovalenta nedbrytare. Arbetet är också pågår för att avgöra om dessa föreningar kan bryta ned andra proteiner."
I teorin, när forskare har fått en full förståelse för nedbrytare SAR, kommer det att vara möjligt att ta bort en rad cancerfrämjande proteiner från olika typer av cancer. Detta tillvägagångssätt kan därför öppna dörren till nya effektiva cancerbehandlingar.
Motsvarande författare Dr. Benjamin Bellenie, Senior Staff Scientist vid avdelningen för cancerterapi vid ICR, sa:"Denna studie har avsevärt förbättrat vår förståelse kring utformningen av monovalenta nedbrytare. Vi har fokuserat specifikt på cyklin K-nedbrytare och behöver träna om vi kan replikera detta tillvägagångssätt för nya mål. Vi tror dock att vår forskning kan möjliggöra framtida läkemedelsupptäckter."
Mer information: Katie L. Thomas et al, Degradation by Design:New Cyclin K Degraders from Old CDK Inhibitors, ACS Chemical Biology (2024). DOI:10.1021/acschembio.3c00616
Journalinformation: ACS Chemical Biology
Tillhandahålls av Institute of Cancer Research