Först nyligen började en ny era inom medicinen med de första RNA-vaccinerna. Dessa aktiva substanser är modifierade RNA som utlöser immunsvar från det mänskliga immunsystemet. Ett annat tillvägagångssätt inom RNA-medicin riktar sig mot kroppens eget RNA och dess proteinmodulatorer med specifikt skräddarsydda aktiva substanser.
Forskare kring Peng Wu, forskargruppsledare vid Chemical Genomics Center vid Max Planck Institute of Molecular Physiology i Dortmund, har nu utvecklat de första småmolekylära hämmarna mot det RNA-modifierande enzymet METTL16. Metyltransferaset är ansvarigt för regleringen av olika RNA och är ett lovande anti-cancermål.
De nya rönen lägger grunden för en omfattande undersökning av rollen av METTL16 i hälsa och sjukdom och är ett steg närmare utvecklingen av terapeutiska medel riktade mot sådana RNA-modifierare. Forskningen är publicerad i tidskriften JACS Au .
RNA har länge endast betraktats som en passiv budbärare i cellen, producerad genom DNA-transkription för att överföra genetisk information till proteinfabrikerna, ribosomerna. Det har dock visat sig att RNA gör mycket mer än så. Förutom det kodande DNA som just beskrivits, finns det också icke-kodande DNA som kontrollerar många cellulära processer genom att reglera aktiviteten hos gener på många nivåer. Inte mindre än ett dussin RNA-klasser har identifierats. RNAi används till exempel av cellen för att bryta ned särskilda RNA-mål för att tysta gener, när det gäller att bekämpa främmande virus-DNA.
RNA interagerar med en uppsjö av biomolekyler, inte bara andra RNA eller DNA utan även proteiner och metaboliter. De resulterande regulatoriska komplexen kontrollerar olika vitala cellulära processer och fel kan orsaka sjukdomar. RNA:s öde bestäms av kemiska modifieringar som påverkar dess stabilitet, struktur och interaktioner och därmed dess öde.
Mer än 170 distinkta RNA-modifieringar har beskrivits hittills. Den vanligaste är metyleringen på N6-positionen av RNA-nukleotiden adenosin (m6A). Det gör att cellen snabbt kan reagera på miljöförändringar genom att initiera lämpliga cellulära svar, såsom delning, differentiering eller migration.
Det är därför RNA-metylering måste kontrolleras noggrant, tas om hand av en uppsättning proteiner:"skribenter" sätter in, "läsare" känner igen och "suddare" tar bort metylgruppen.
Avvikande RNA-metylering har associerats med cancer och andra mänskliga sjukdomar, vilket gör "författare" till ett attraktivt terapeutiskt mål. Endast en handfull RNA m6A-skrivare har hittills identifierats. Och endast för en av dem, METTL3, har potenta hämmare rapporterats. Dessa molekyler hindrar skrivaren från att absorbera bläcket, biomolekylen S-adenosylmetionin (SAM).
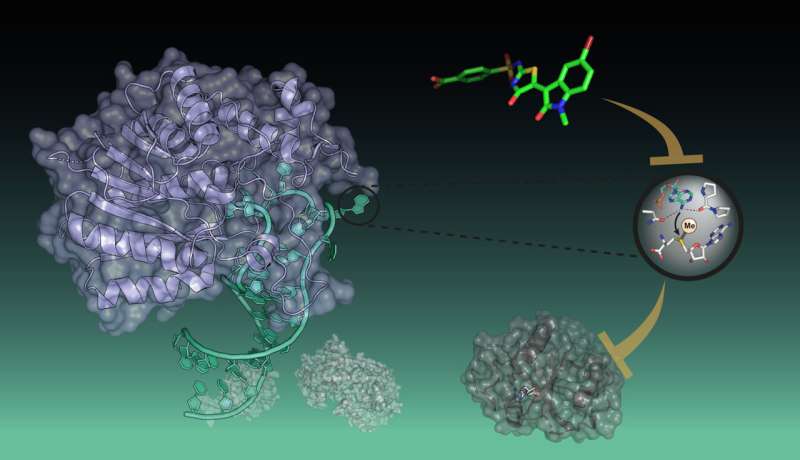
Gruppen Peng Wu har nu identifierat den första hämmaren av författaren METTL16. Men i motsats till de tidigare nämnda hämmarna visade den ett annat verkningssätt:det förhindrar interaktionen av METTL16 med RNA. Forskarna kunde identifiera denna nya typ av hämmare genom att utveckla en analys som utvärderade störningen mellan METTL16 och ett fluorofor-märkt mRNA-substrat.
"Vissa cancerceller har förhöjda skribentnivåer och är också mer sårbara för minskning av SAM-nivåer, vilket gör dem till lovande anticancermål. De exakta biologiska konsekvenserna av METTL16:s bindning till RNA-substrat är dock ännu inte klart fastställda. Med vårt arbete ligger vi fast. grunden för en bättre undersökning av rollen av METTL16 i sjukdom och hälsa, men också för utvecklingen av nya RNA-inriktade terapier, säger Peng Wu.
Mer information: Yang Liu et al, Aminotiazolon-hämmare stör protein-RNA-interaktionen av METTL16 och modulerar m6A RNA-modifieringen, JACS Au (2024). DOI:10.1021/jacsau.3c00832
Tillhandahålls av Max Planck Society