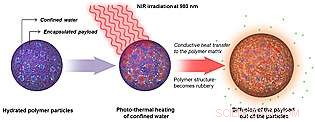
I denna schematiska representation, en hydratiserad polymer nanopartikel utsätts för nära-infrarött ljus. NIR värmer upp vattenfickor inuti nanopartikeln, vilket gör att polymeren mjuknar och tillåter inkapslade molekyler att diffundera in i den omgivande miljön. Kredit:UC San Diego School of Medicine
Forskare från University of California, San Diego Skaggs School of Pharmacy and Pharmaceutical Sciences, i samarbete med materialvetare, ingenjörer och neurobiologer, har upptäckt en ny mekanism för att använda ljus för att aktivera läkemedelslevererande nanopartiklar och andra riktade terapeutiska ämnen inuti kroppen.
Denna upptäckt representerar en stor innovation, sa Adah Almutairi, PhD, docent och chef för det gemensamma UC San Diego-KACST Center of Excellence in Nanomedicine. Tills nu, Hon sa, endast en handfull strategier som använder ljusutlöst frisättning från nanopartiklar har rapporterats.
Mekanismen, beskrivs i den 1 april, 2014 online nummer av ACS Nano , använder nära-infrarött (NIR) ljus från en lågeffektlaser för att värma upp vattenfickor instängda i icke-fotokänsliga polymera nanopartiklar infunderade med läkemedel. Vattenfickorna absorberar ljusenergin som värme, som mjukar upp den inkapslande polymeren och gör att läkemedlet kan frisättas i den omgivande vävnaden. Processen kan upprepas flera gånger, med exakt kontroll av mängden och spridningen av läkemedlet.
"En viktig fördel med denna mekanism är att den bör vara kompatibel med nästan alla polymerer, även de som är kommersiellt tillgängliga, sade Mathieu Viger, en postdoktor vid Almutairis laboratorium och medförfattare till studien. "Vi har observerat fångst av vatten i partiklar som består av alla biologiskt nedbrytbara polymerer som vi hittills har testat."
Metoden, noterade Viger, skulle således lätt kunna adopteras av många biologiska laboratorier.
Den kombinerade användningen av hydratiserade polymerer och nära-infrarött ljus verkar lösa en mängd tekniska och hälsobarriärer som har hindrat tidigare, liknande tillvägagångssätt. Tidigare ansträngningar att använda NIR-utlöst release har inte utnyttjats i stor utsträckning eftersom de krävde speciella designerpolymerer, dyra kraftfulla lasrar och/eller saminkapsling av oorganiska partiklar vars säkerhet i kroppen fortfarande är tveksam.
Den nya metoden som beskrivs av Almutairi och kollegor på avdelningarna för maskin- och flygteknik, Neurovetenskap, och kemi och biokemi vid UC San Diego använder NIR vid en vibrationsvåglängd som stimuleras för att excitera vattenmolekyler, som absorberar den optiska energin och omvandlar den till värme. NIR kan penetrera biologiska vävnader till större djup än synligt eller ultraviolett ljus.
Medförfattare Wangzhong Sheng, en doktorand vid institutionen för maskin- och rymdteknik, förklarade uppvärmningens selektivitet genom att jämföra det fångade vattnet i partiklar med ett glas vatten och det omgivande vattnet i lösningen eller vävnaden med ett badkar. Den mindre mängden vatten värms upp mycket snabbare på grund av den enorma volymskillnaden.
En uppenbar användning av metoden, sa Almutairi, är ljusutlöst läkemedelstillförsel, men med mer forskning, hon förväntar sig att den nya metoden kan ge en mängd olika industriella, medicinska och vetenskapliga tillämpningar, inklusive "alla tekniska tillämpningar som kräver att kemin kontrolleras i tid och rum, till exempel i katalys eller självreparerande material eller ljusaktiverade solskyddsmedel eller bekämpningsmedelsdosering."