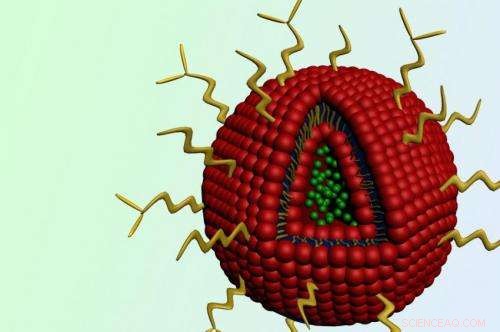
Nanopartikeln innehåller cancerläkemedlet doxorubicin (gröna sfärer) i sin kärna. Erlotinib är inbäddat i det röda yttre skalet. Fäst på ytan är kedjor av polyetylenglykol (PEG), i gult. Upphovsman:Stephen Morton
MIT -forskare har tagit fram en ny cancerbehandling som förstör tumörceller genom att först avväpna deras försvar, sedan slå dem med en dödlig dos av DNA -skada.
I studier med möss, forskargruppen visade att denna en-två slag, som bygger på en nanopartikel som bär två läkemedel och släpper ut dem vid olika tidpunkter, krymper dramatiskt lung- och brösttumörer. MIT -teamet, ledd av Michael Yaffe, David H. Koch professor i vetenskap, och Paula Hammond, David H. Koch professor i teknik, beskriv fynden i den 8 maj onlineutgåvan av Vetenskapssignalering .
"Jag tror att det är en föregångare till vad nanomedicin kan göra för oss i framtiden, säger Hammond, som är medlem i MIT:s Koch Institute for Integrative Cancer Research. "Vi går från den enklaste modellen av nanopartikeln - bara att få in läkemedlet där och rikta det - till att ha smarta nanopartiklar som levererar läkemedelskombinationer på det sätt som du verkligen behöver angripa tumören."
Läkare ger rutinmässigt cancerpatienter två eller flera olika kemoterapimedicin i hopp om att en mångsidig attack kommer att bli mer framgångsrik än ett enda läkemedel. Även om många studier har identifierat läkemedel som fungerar bra tillsammans, ett papper från 2012 från Yaffes labb var det första som visade att tidpunkten för läkemedelsadministration dramatiskt kan påverka resultatet.
I den studien, Yaffe och tidigare MIT postdoc Michael Lee fann att de kunde försvaga cancerceller genom att administrera drogen erlotinib, som stänger av en av de vägar som främjar okontrollerad tumörtillväxt. Dessa förbehandlade tumörceller var mycket mer mottagliga för behandling med ett DNA-skadligt läkemedel som kallas doxorubicin än celler som gav de två läkemedlen samtidigt.
"Det är som att koppla om en krets, "säger Yaffe, som också är medlem i Koch Institute. "När du ger det första läkemedlet, trådarnas anslutningar växlas så att det andra läkemedlet fungerar på ett mycket mer effektivt sätt. "
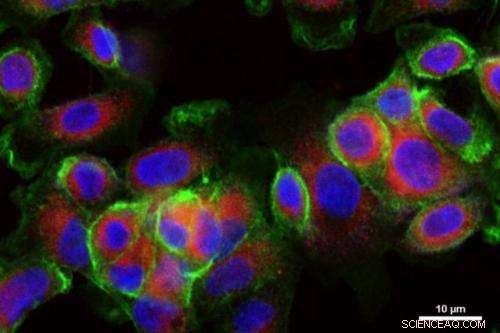
Läkemedelsleverans nanopartiklar (färgade röda) tas upp av cancerceller som odlas i laboratoriet. Upphovsman:Stephen Morton
Erlotinib, som riktar sig mot ett protein som kallas epidermal tillväxtfaktor (EGF) -receptorn, finns på tumörcellytor, har godkänts av Food and Drug Administration för att behandla bukspottskörtelcancer och vissa typer av lungcancer. Doxorubicin används för att behandla många cancerformer, inklusive leukemi, lymfom, och urinblåsa, bröst, lunga, och äggstockstumörer.
Försvagning av dessa läkemedel visade sig vara särskilt kraftfull mot en typ av bröstcancercell som kallas trippelnegativ, som inte har överaktiv östrogen, progesteron, eller HER2 -receptorer. Trippelnegativa tumörer, som står för cirka 16 procent av fallen av bröstcancer, är mycket mer aggressiva än andra typer och tenderar att slå till yngre kvinnor.
Det var ett spännande fynd, Säger Yaffe. "Problemet var, " han lägger till, "hur översätter man det till något man faktiskt kan ge en cancerpatient?"
Från laboratorieresultat till läkemedelsleverans
För att närma sig detta problem, Yaffe gick ihop med Hammond, en kemiingenjör som tidigare har designat flera typer av nanopartiklar som kan bära två läkemedel samtidigt. För detta projekt, Hammond och hennes doktorand, Stephen Morton, skapade dussintals kandidatpartiklar. Den mest effektiva var en typ av partikel som kallas liposomer - sfäriska droppar omgiven av ett fett yttre skal.
MIT -teamet utformade sina liposomer för att bära doxorubicin inuti partikelkärnan, med erlotinib inbäddat i det yttre lagret. Partiklarna är belagda med en polymer som kallas PEG, som skyddar dem från att brytas ner i kroppen eller filtreras bort från levern och njurarna. En annan tagg, folat, hjälper till att rikta partiklarna till tumörceller, som uttrycker stora mängder folatreceptorer.
När partiklarna når en tumör och tas upp av celler, partiklarna börjar brytas ner. Erlotinib, bärs i det yttre skalet, släpps först, men frisättningen av doxorubicin fördröjs och det tar längre tid att sippra in i celler, ger erlotinib tid att försvaga cellernas försvar. "Det är en fördröjning på någonstans mellan fyra och 24 timmar mellan när erlotinib når sin effektivitet och doxorubicin når sin effektivitet, "Säger Yaffe.
Forskarna testade partiklarna i möss implanterade med två typer av humana tumörer:trippel-negativa brösttumörer och icke-småcelliga lungtumörer. Båda typerna krympt betydligt. Vidare, genom att förpacka de två läkemedlen i liposomen nanopartiklar gjorde de mycket mer effektiva än de traditionella formerna av läkemedlen, även när dessa droger gavs i en tidsförskjuten ordning.
Som ett nästa steg före möjliga kliniska prövningar på mänskliga patienter, forskarna testar nu partiklarna i möss som är genetiskt programmerade att utveckla tumörer på egen hand, istället för att ha implanterade mänskliga tumörceller i dem.
Forskarna tror att tidsförskjuten leverans också kan förbättra andra typer av kemoterapi. De har tagit fram flera kombinationer som involverar cisplatin, ett vanligt använt DNA-skadligt läkemedel, och arbetar med andra kombinationer för att behandla prostata, huvud och nacke, och äggstockscancer. På samma gång, Hammonds laboratorium arbetar med mer komplexa nanopartiklar som möjliggör mer exakt laddning av läkemedlen och finjustering av deras förskjutna frisättning.
"With a nanoparticle delivery platform that allows us to control the relative rates of release and the relative amounts of loading, we can put these systems together in a smart way that allows them to be as effective as possible, " Hammond says.