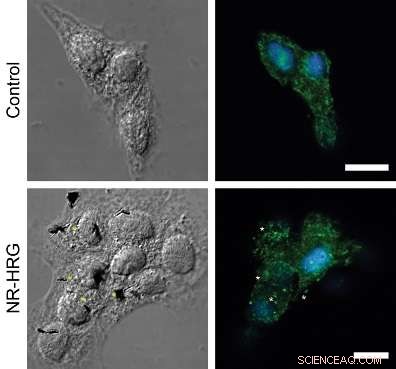
Figur:ErbB2 -receptorkluster vid HRG -nanorodbindning till MCF7 -celler. Konfokala mikroskop som visar en dorsal sektion av riktade (nedre panelen) och icke-riktade (överpanelen) MCF7-celler. ErbB2 -receptorer (gröna) immunfärgades utan att permeabilisera plasmamembranet. Kärnor färgades med Hoechst 33342 (blå). Stjärnor indikerar exempel på ErbB2 -receptorkluster som ligger i närheten av nanoroder.
UCD -forskare har framgångsrikt manipulerat nanopartiklar för att rikta in sig på två mänskliga bröstcancercellinjer som ett verktyg för cancerdiagnos och behandling.
Beläggning av nanopartiklar med olika ämnen gör att deras interaktion med celler kan ställas in på ett visst sätt. Till exempel, att använda en optiskt aktiv partikel som guld (Au) ger utmärkt kontrast i nära infraröd (NIR) avbildning och, vid uppvärmning, kan faktiskt förstöra den omgivande vävnaden. Detta kallas fototermisk ablationsterapi. Magnetiskt aktiva partiklar som järn (Fe) kan möjliggöra fysioterapier genom att generera värme när de utsätts för alternerande magnetfält som orsakar celldöd (magnetisk hypertermi).
UCD -teamet under ledning av Conway Fellows, Professor Gil Lee vid School of Chemistry and Chemical Biology och professor Walter Kolch i systembiologi Irland, syntetiserade nanoroder med ett långt järnsegment belagt med polyetylenglykol och en kort guldspets belagd med ett enda lager av proteinet, heregulin (HRG).
HRG är en tillväxtfaktor som binder till och aktiverar ErbB -familjen av proteinreceptorer. ErbB2 är överuttryckt i vissa bröstcancer och kopplat till dålig prognos. Dock, ErbB2 -överuttryck leder till ökad känslighet för vissa läkemedel. Teamet tror att Fe-Au-funktionaliserade nanoroder som används tillsammans med dessa läkemedel kan vara användbara vid cancerbehandling.
Efter att ha karaktäriserat och justerat interaktionen mellan nanoroderna och cellerna, forskargruppen bedömde hur cellerna reagerar på mekanisk stimulering. Att göra detta, de integrerade en elektromagnetisk pincett med ett optiskt mikroskop och använde ett nytt mikrofluidiskt chip för att övervaka interaktionen mellan enskilda nanoroder med två mänskliga bröstcancercellinjer som uttrycker ErbB -familjen av receptorer i olika takt. När HRG-nanoroderna binder till cancerceller som uttrycker ErbB, de sparkar igång en kaskad av signalhändelser som leder till celldöd.
"Med magnetpincett för att sträcka celler, vi kunde ytterligare aktivera cellsignaleringsvägar för att utlösa celldöd. Detta var ännu mer effektivt för att orsaka cancercellsdöd än magnetisk hypertermi, det andra terapeutiska tillvägagångssättet vi bedömde ", förklarade Dr Devrim Kilinc, första författare och forskare i Lee -gruppen.
"Resultaten är en positiv indikation för nanoskala -inriktning och lokal manipulation av cancerceller med en specifik receptorprofil."