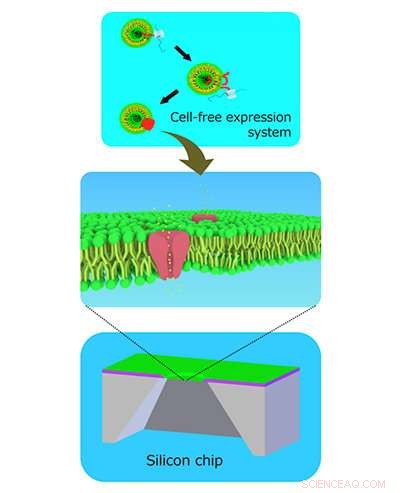
Cellfria jonkanaler inbäddade i tvåskiktslipidmembran bildade i kiselchips. Kredit:Ayumi Hirano-Iwata
Forskare från Tohoku University har förbättrat för närvarande tillgängliga metoder för att screena läkemedel för hjärtrelaterade biverkningar.
Metoden går ut på att tillverka ett litet hål i ett kiselchip över vilket lipidmembran, liknande de som omger celler, uppmuntras att växa. En jonkanal syntetiseras sedan separat och slås in i membranet under centrifugering.
Jonkanaler är porer gjorda av proteiner som finns i vissa cellmembran, som i hjärtmuskelceller. De öppnar och stänger för att låta joner passera igenom, skapa en elektrisk signal. Vissa läkemedel har biverkningar genom att de verkar på dessa jonkanaler. Antihistamin astemizol, till exempel, som nu har dragits tillbaka från den amerikanska marknaden, kan stänga av en kaliumjonkanal som är involverad i att reglera hjärtslag. Att ta det kan leda till oregelbunden hjärtklappning.
Forskare har undersökt sätt att screena läkemedel för biverkningar på jonkanaler. För närvarande tillgängliga metoder är ofullkomliga. I en metod, stamceller är riktade att omvandlas till hjärtmuskelceller som har den specifika typen av jonkanal som är inriktad på drogtester. Den här metoden, dock, är tråkigt och kan ta upp till 90 dagars förberedelse. Övrig, mindre tidskrävande metoder innebär att man sätter in jonkanaler i artificiellt formade lipidmembran som täcker ett litet hål som gjorts i ett chip i mikro- eller nanostorlek. Men nuvarande metoder leder till bildandet av instabila membran, minska deras effektivitet under experiment.
Professor Ayumi Hirano-Iwata vid Tohoku Universitys Advanced Institute of Materials Research och hennes team tillverkade tre kiselchips med olika formade hål och jämförde deras förmåga att vara värd för jonkanal-innehållande lipidmembran.
Varje chip var gjord av ett tjockt lager av kisel täckt av ett tunt lager av kiselnitrid, följt av ett tunt lager kiseloxid. I en rad steg, den centrala delen av chipet etsades bort för att skapa ett litet hål. Hålets form varierade mycket lite beroende på vilken typ av syra som användes för att lösa upp materialet. Teamet fann att hålet som gav mest stabilitet för lipidmembran att bilda över det hade en gradvis avsmalnande kant. En större andel membran förblev fästa vid den avsmalnande kanten under centrifugering (45 procent) och när små krafter applicerades på dem (75 procent), jämfört med de som är fästa vid de två andra hålen (från 0 procent till 20 procent).
Teamet lade till en cellfri syntetiserad hjärtmuskeljonkanal, kallas hERG, till membranen genom centrifugering. De lyckades detektera elektriska strömmar från kanalerna och blockera strömmarna genom att administrera läkemedlet astemizol, som har en välkänd negativ effekt på hERG-kanalerna i hjärtat.
Deras tillvägagångssätt har potentialen "att fungera som en ny screeningplattform för att bedöma de potentiella riskerna för läkemedelsbiverkningar som verkar på patienters hERG-kanaler, " avslutar forskarna i sin studie publicerad i tidskriften Vetenskapliga rapporter .