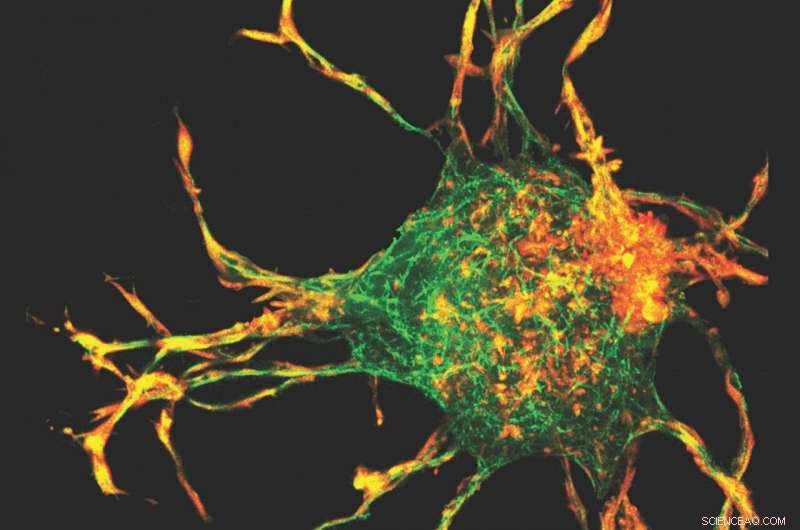
Forskare använde en 3D-kartläggningsteknik - första gången den har applicerats på kollagen - tillsammans med en beräkningsmodell för att beräkna 3D-belastningen och stressfälten som skapas av utsprång från cellerna. Kredit:Artighetsbild
När vi får ett sår på huden, cellerna i våra kroppar mobiliserar snabbt för att reparera det. Även om det har varit känt hur celler läker sår och hur ärr bildas, ett team ledd av forskare från Washington University i St. Louis har för första gången bestämt hur processen börjar, som kan ge ny insikt om sårläkning, fibros och cancermetastaser.
Laget, ledd av Delaram Shakiba, en postdoktor från NSF Science and Technology Center for Engineering Mechanobiology (CEMB) vid McKelvey School of Engineering, upptäckte hur fibroblaster, eller vanliga celler i bindväv, interagerar med den extracellulära matrisen, som ger strukturellt stöd såväl som biokemiska och biomekaniska signaler till celler. Teamet upptäckte en rekursiv process som pågår mellan cellerna och deras miljö samt strukturer i cellerna som tidigare var okända.
Resultaten av forskningen publicerades i ACS Nano den 28 juli. Seniorförfattare på tidningen är Guy Genin, Harold och Kathleen Faught professor i maskinteknik vid McKelvey School of Engineering, och Elliot Elson, professor emeritus i biokemi och molekylär biofysik vid Medicinska institutionen.
"Kliniska ansträngningar för att förhindra progression av fibrokontraktila sjukdomar, såsom ärrbildning och fibros, har i stort sett misslyckats, delvis för att mekanismerna som celler använder för att interagera med proteinfibrerna runt dem är oklara, "Shakiba sa. "Vi fann att fibroblaster använder helt olika mekanismer i de tidiga - och jag tror de mest behandlingsbara - stadierna av dessa interaktioner, och att deras reaktioner på droger därför kan vara motsatsen till vad de skulle vara i de senare stadierna."
Genin, vem är meddirektör för CEMB, sade att processen har hindrat mekanobiologiforskare under en tid.
"Forskare inom mekanobiologin trodde att celler drog in kollagen från den extracellulära matrisen genom att nå ut med långa utsprång, tar tag i den och drar tillbaka den, ", sa Genin. "Vi upptäckte att så inte var fallet. En cell måste först pressa sig ut genom kollagen, då istället för att ta tag i det skjuter i princip små hårstrån, eller filopodia, ut ur sidorna av armarna, drar in kollagen på det sättet, drar sig sedan tillbaka."
Nu när de förstår denna process, Genin sa, de kan styra formen som en cell tar.
"Med våra kollegor på CEMB vid University of Pennsylvania, vi kunde validera några matematiska modeller för att gå igenom ingenjörsprocessen, och vi har nu de grundläggande reglerna som celler följer, ", sa han. "Vi kan nu börja designa specifika stimuli för att styra en cell att bete sig på ett visst sätt i att bygga en vävnadskonstruerad struktur."
Forskarna lärde sig att de kunde kontrollera cellformen på två sätt:För det första, genom att kontrollera gränserna runt det, och för det andra, genom att hämma eller uppreglera särskilda proteiner som är involverade i remodelleringen av kollagenet.
Fibroblaster drar ihop kanterna på ett sår, får den att dra ihop sig eller sluta sig. Kollagen i cellerna omformar sedan den extracellulära matrisen för att helt stänga såret. Det är här mekanobiologin kommer in i bilden.
"Det finns en balans mellan spänning och kompression inuti en cell som nyligen har exponerats för fibrösa proteiner, " sade Genin. "Det finns spänning i aktinkablar, och genom att leka med den balansen, vi kan få dessa utsprång att växa extremt långa, " Sa Genin. "Vi kan stoppa ombyggnaden från att inträffa eller så kan vi öka den."
Teamet använde en 3-D-kartläggningsteknik - första gången den har applicerats på kollagen - tillsammans med en beräkningsmodell för att beräkna 3D-spänningen och stressfälten som skapas av utsprången från cellerna. När cellerna ackumulerade kollagen, spänningsdriven ombyggnad och anpassning av kollagenfibrer ledde till bildandet av kollagenkanaler. Detta kräver samverkande interaktioner mellan celler, genom vilka celler kan interagera mekaniskt.
"Nya metoder för mikroskopi, vävnadsteknik och biomekanisk modellering förbättrar avsevärt vår förståelse av mekanismerna genom vilka celler modifierar och reparerar vävnaderna de befolkar, ", sade Elson. "Fibrösa cellulära strukturer genererar och styr krafter som komprimerar och omorienterar deras extracellulära fibrösa miljö. Detta väcker nya frågor om de molekylära mekanismerna för dessa funktioner och hur celler reglerar krafterna de utövar och hur de styr omfattningen av matrisdeformation."
"Sårläkning är ett bra exempel på hur dessa processer är viktiga på ett fysiologiskt sätt, ", sa Genin. "Vi kommer att kunna komma med insikter i hur man tränar celler att inte överdrivet komprimera kollagenet runt dem."