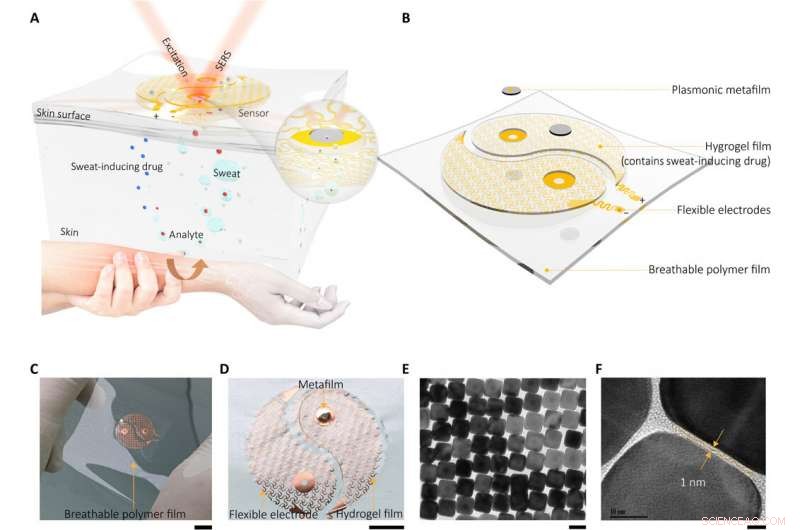
Plasmoniskt metamaterial-integrerad bärbar SERS-avkänningsenhet. (A) Schematisk ritning som visar enhetens arbetsprincip och design, (B) som bestod av två huvudkomponenter (svettextraktionskomponent och SERS-avkänningskomponent) och utformades för att se ut som en yin-yang-symbol. Den infällda figuren framhäver nyckelavkänningsgränssnittet nära metafilmen. (C) Optisk bild av enheten och (D) förstorad optisk bild av svettextraktionskomponenten. Ett tunt hydrogelskikt laddat med molekyler (acetylkolinklorid) som stimulerar svettkörtelsekretioner är monterat på spiralfraktalmesh-elektroden. Observera att för att markera kontrasten för utställningen, endast en av elektroderna var monterad med hydrogelskiktet och den plasmoniska metafilmen. Fotokredit:Yingli Wang, Zhejiang universitet. (E och F) Högupplösta transmissionselektronmikroskopbilder (TEM) av SERS-avkänningskomponenten monterad i mitten av elektroden, vilket är den plasmoniska metafilmen som bildas av en ordnad silvernanokub (NC) supergitter. Skala staplar, 1 cm (C), 5 mm (D), 50 nm (E), och 5 nm (F). Kredit:Science Advances, doi:10.1126/sciadv.abe4553
Bärbar avkänningsteknik är en viktig länk i personlig medicin, där forskare måste spåra flera analyter inuti kroppen samtidigt, för att få en fullständig bild av människors hälsa. I en ny rapport om Vetenskapens framsteg , Yingli Wang och ett team av forskare inom biosystem, ingenjörs- och informationsvetenskap vid University of Cambridge och Zhejiang University i Storbritannien och Kina, presenterade en bärbar plasmonisk-elektronisk sensor med "universell" molekylär igenkänningsförmåga. Teamet introducerade flexibla plasmoniska metasytor med ytförstärkt Raman-spridning (SERS) aktivitet som den grundläggande avkänningskomponenten. Systemet innehöll en flexibel svettextraktionsprocess för att noninvasivt extrahera och fingeravtrycksanalyter inuti kroppen baserat på deras unika Raman-spridningsspektra. Som proof of concept, de övervakade framgångsrikt varierande spårläkemedelsmängder inuti kroppen för att få en individuell läkemedelsmetabolisk profil. Sensorn överbryggade gapet i bärbar avkänningsteknik för att ge en universell, känslig molekylär spårningsprocess för att bedöma människors hälsa.
Bärbar sensorteknik
Wang et al. presenterade en bärbar plasmonisk elektronisk integrerad avkänningsplattform med en nästan "universell" igenkänningsförmåga. Bärbar avkänning ger en länk till framtiden för personlig medicin, men sådana sensorer måste övervinna en fundamental oöverensstämmelse mellan en styv och mjuk elastisk yta för att laminera in i biogränssnitt som huden, öga, nerv och tand för att sömlöst bedöma människors hälsa. Enheterna gör det möjligt för forskare att kontinuerligt bedöma vitala tecken inklusive hjärtfrekvens och kroppstemperatur, svett och fysiska aktiviteter. Trots framgången med fysiska bärbara sensorer, Icke-invasiva molekylspårningstekniker som ger insikt i människokroppens dynamik på molekylär nivå återstår att realisera. Dessa förmågor är avgörande för personlig precisionsmedicin. I det här fallet, Wang et al. syftade till att utveckla en ny strategi med universell målspecificitet istället för att ha ett enda mål för att samtidigt spåra flera mål. Teamet utvecklade en ny plattform med hjälp av en flexibel ytförstärkt Raman-spektroskopi (SERS)-aktiv plasmonisk metayta för att fungera som nyckelavkänningskomponenten och ett flexibelt elektroniskt system för att automatiskt extrahera svett och analyter från kroppen.
Karakterisering av enhetens SERS-avkänningskomponent. (A) Schematisk illustration som visar SERS-avkänningsprincipen för NC-metafilmen. Analyterna i den extraherade svetten drogs till EM-hotspot i NC-metafilm från botten, som kan detekteras in situ med SERS-teknik från baksidans metafilm (bakåt excitation och samling). (B) FDTD-simulering av den lokala elektriska fältförbättringen för EM-hotspot i NC-metaytan. (C) SERS-spektra av NC-metafilmen nedsänkt i sondmolekyllösningen (CV) med olika koncentrationer (i genomsnitt 20 slumpmässigt utvalda platser för varje koncentration med en 1-sekunds insamlingstid och med ett 10× objektiv och laserstyrka på 0,33 mW). (D) Raman-intensitetskarta (~1621 cm−1) av NC-metafilmen efter behandling med Raman-sonden (CV, 10-5 M). (E) Jämförelse av SERS-svaren (~1621 cm−1) till olika CV-lösningar med hjälp av insamlingsmetoder bakåt och framåt. (F) SERS-spektra av mänskliga svettprover som innehåller olika läkemedel (0,2 M lidokain, 10−3 M kokain, och 10−5 M metotrexat) och det tomma svettprovet (med 10× eller 50× objektiv och laser med effekt 0,15 till 0,66 mW, med inhämtningstider på 6 till 30 s). Kredit:Science Advances, doi:10.1126/sciadv.abe4553 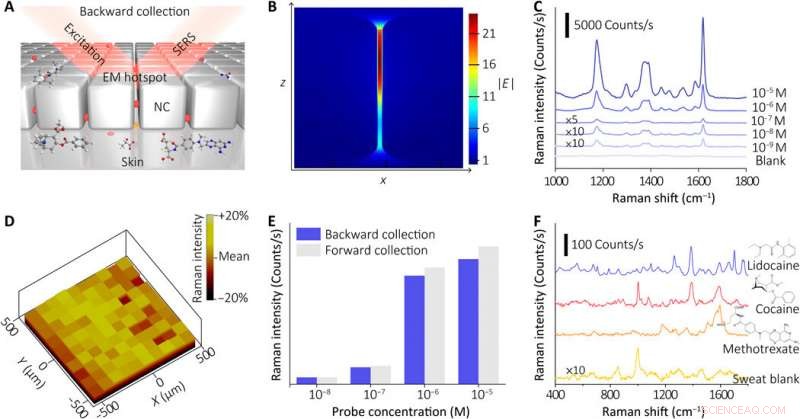
Teamet tog fingeravtryck av det unika SERS-spektrumet med hjälp av den bärbara sensorn. Som ett bevis på konceptet, de upptäckte variationen av läkemedelskoncentrationer i människokroppen för att erhålla en individs läkemedelsmetaboliska profil. Den integrerade bärbara sensorn överbryggade det befintliga gapet i personlig diagnos för realtidsspårning av viktiga biokemiska föreningar. Forskarna använde avkänningsplattformen för att övervaka fysiologiska signaler eller läkemedelskoncentrationer i människokroppen för att få fram en individs läkemedelsmetaboliska profil. Använd sedan den integrerade bärbara sensorn, de övervakade fysiologiska signaler eller läkemedelskoncentrationer i ett återkopplat läkemedelsleveranssystem med sluten slinga.
Den plasmoniska metamaterial-integrerade bärbara avkänningsanordningen innehöll två huvudkomponenter inklusive ett tunt lager av hydrogel laddat med molekyler för att stimulera svettkörtelsekretioner. Teamet fäste dessa konstruktioner till två spiralfraktalmesh-elektroder för att fungera som svettextraktionskomponenten. Wang et al. använde jontoforesprocessen (transdermal läkemedelstillförsel) för denna extraktion; används allmänt som en icke-invasiv svettprovtagningsmetod i enheter för diagnostiska och terapeutiska ändamål. De bildade en plasmonisk metafilm med hjälp av ett beställt silver nanokub supergitter för att fungera som avkänningskomponenten monterad i experimentuppställningen. De starka elektromagnetiska fälten lokaliserade i nanokuben gav upphov till SERS-effekten (ytförstärkt Raman-spridning) för att detektera molekyler som närmar sig metafilmytan. De placerade de två komponenterna på en tunn polymerfilm med ultralåg modul för att bilda en tunn, andningsbart och fysiskt tufft stöd för icke-irriterande hudvidhäftning. Med hjälp av elektroderna, teamet applicerade en mild elektrisk ström för att leverera acetylkolinklorid i hydrogelskiktet till sekretoriska svettkörtlar för snabb, lokaliserad svettgenerering.
Mekaniska egenskaper hos enheten. (A) Optiska bilder av sensorn under deformation. (B) FEM-töjningsfördelningsanalys av skyddsringområdet på den töjbara elektroden under olika förvrängningar, indikerar att skyddsringen kan isolera stora deformationer till den mjuka elastomeren, på så sätt undviker potentiellt destruktiva plastpåfrestningar på SERS-avkänningskomponenten. (C) SERS-svar hos sensorn under olika deformationer. (D) SERS-sensorns egenskaper efter det cykliska sträcktestet. (E) Motståndsförändringar i elektroden under olika deformationer. (F) Motståndsförändringar i elektroden efter det cykliska sträcktestet. (G) Fotografier av sensorn monterad på mänsklig hud och (H) under olika förhållanden. Fotokredit:Xiangjiang Liu, Zhejiang universitet. Skala staplar, 1 mm (B) och 1 cm (G och H). Felstaplar definieras som ±SD. Kredit:Science Advances, doi:10.1126/sciadv.abe4553 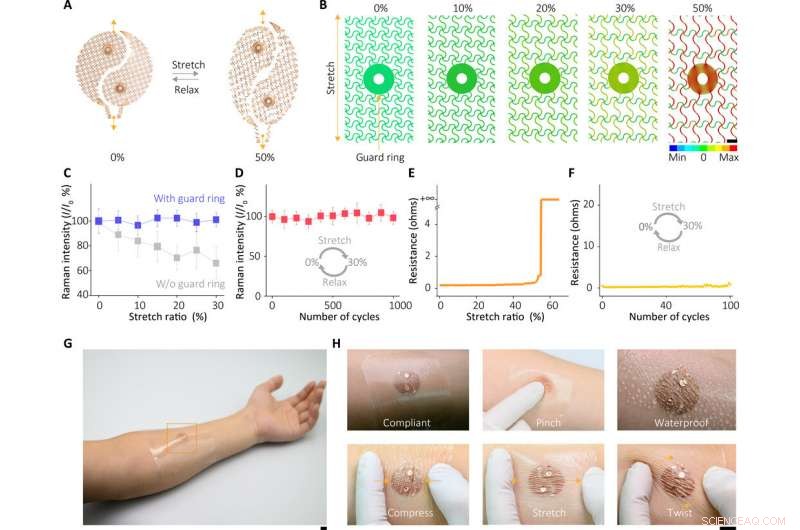
Sensorn för den bärbara enheten berodde på SERS-effekten som genererades av den beställda silvernanokubens supergittermetafilm, baserat på vilket teamet upptäckte målet av intresse för extraherad svett. I början, de satte ihop ett enda lager av den slutna packade nanokubmatrisen vid vätske/luft-gränsytan och transformerade sedan konstruktionen till en tunn flexibel polymerbärare. Forskarna verifierade sedan den genomsnittliga gapstorleken mellan nanokuberna med hjälp av högupplösta transmissionselektronmikroskopbilder (TEM) och utförde numeriska simuleringar med finit-difference time domän (FDTD). Den mekaniska följsamheten och hudkontakten hos metafilmen möjliggjorde högtrohetsmätningar. Teamet utvecklade sedan SERS-filmen och överförde den till en hydrogel laddad med ett agonistmedel fäst vid fraktala mesh-elektroder. De använde en ultratunn spiraldesign för att öka toleransen hos det svettframkallande systemet mot mekaniska deformationer och åstadkom detta genom att utveckla ett "sammankopplat ön" designsteg för att bilda en spröd SERS-film med ett mjukt och elastiskt elektroniskt system. Teamet bekräftade elektronikens hållbarhet efter 100 testcykler, utan någon observerbar signalförsämring för att perfekt uppfylla de uppgifter som krävs av en bärbar sensor.
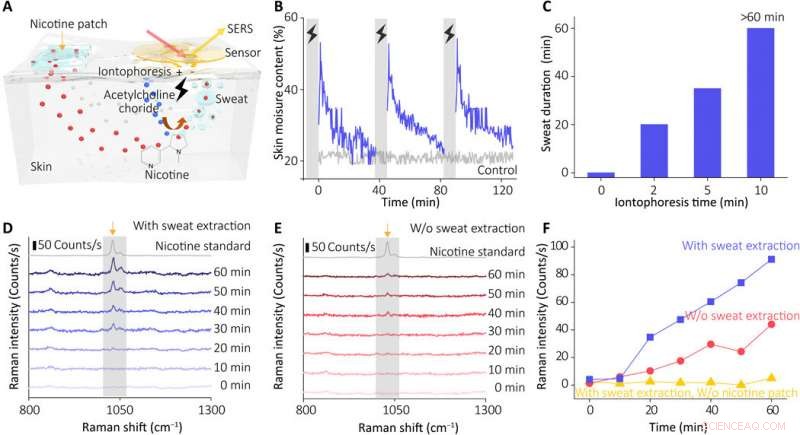
In vivo-avkänningsprestanda för vår sensor. (A) Schematisk illustration som visar arbetsprincipen för svettutvinningssystemet. (B) Variation i hudens fukthalt efter periodisk svettinduktion (med hydrogel som innehåller 10 % acetylkolinklorid, jontoforesström på 0,5 mA under 5 min). (C) Inducerade svettutsöndringsegenskaper som svar på olika jontoforestider (0 till 10 min). Sekretionsvaraktigheten representerar den totala tiden för hudkonduktans över baslinjen (mätningar stoppade vid 60 min). (D) Realtidsövervakning av nikotin i mänsklig hud med hjälp av vår integrerade sensor (med svettextraktion) och (E) kontrollgrupper (utan att slå på jontoforesströmmen för svettextraktion). Spektrana samlades in med hjälp av lasereffekt på 0,33 mW och ett 10× objektiv (insamlingstid, 1 s). (F) Utveckling av den karakteristiska Raman-toppen av nikotin efter svettextraktion av testgruppen och kontrollgruppen (utan att slå på strömmen eller utan att fästa nikotinplåster). Kredit:Science Advances, doi:10.1126/sciadv.abe4553
Biologisk avkänningsapplikation
Wang et al. rekryterade därefter friska frivilliga för in vivo (fysiologiska) mätningar för att visa enhetens svettextraktionsförmåga. Forskarna använde nikotin som modellläkemedel och övervakade den faktiska koncentrationen av läkemedlet i huden i förhållande till läkemedelstillförseln, upptag och ämnesomsättning per individ. Under experimenten använde de en bärbar SERS-sensor kopplad till en kompakt strömförsörjning och trådlös kontrollenhet på underarmen på de frivilliga. Enheten visade SERS-spektrumet av nikotin i svetten för att matcha nikotinstandardens spektrum. Resultaten visade hur sensorn tränade nikotinets metaboliska beteende så att den bärbara sensorns förmåga att övervaka läkemedels dynamiska farmakokinetik och deras metaboliska profil. Sensorn, dock, endast effektivt detekterade mål lagrade i den grunda subepidermis; därför, forskarna kommer att behöva förstå hur detta värde korrelerar med läkemedelskoncentrationer i blod eller interstitiell vätska under fortsatta studier.
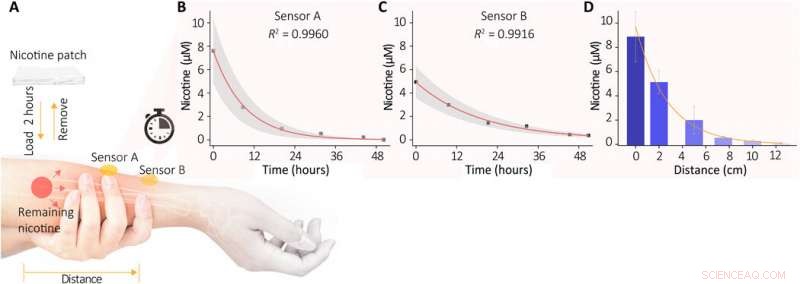
In vivo-övervakning av nikotinmetaboliseringsprocessen i mänsklig hud. (A) Schematisk illustration av experimentet. Ett nikotinplåster innehållande ~10 mg fästes på frivilligas underarm i 2 timmar och togs sedan bort. Efter att huden rengjorts noggrant, det återstående nikotinet i huden extraherades och analyserades av vår sensor. (B och C) Utvecklingen av de återstående nikotinkoncentrationerna mättes från de två platserna (sensor A direkt på det lappade området; sensor B är fäst cirka 2 cm bort). Varje mätning gjordes efter 20 minuters svettextraktion (0,5 mA jontoforesström, 10 % acetylkolinklorid-laddad hydrogel), och sensorsvaren under de följande 10 minuterna samlades kontinuerligt in. De erhållna genomsnittliga nikotinnivåerna visas i figuren. Skuggområdena indikerar ±SD för mätningarna. (D) Avståndsberoende av nikotinkoncentrationerna i den extraherade svetten efter lappning. Sex sensorer placerades längs armen på ett avstånd av 0 till 12,5 cm från lappningsområdet. Kredit:Science Advances, doi:10.1126/sciadv.abe4553
Syn
På det här sättet, Yingli Wang och kollegor visade upp en bärbar plasmonisk-elektronisk integrerad sensor som en nästa generations bärbar enhet. Jämfört med befintliga bärbara elektrokemiska sensorer, denna sensor visade bredare målspecificitet och högre stabilitet. Den integrerade enheten överbryggade det befintliga gapet inom personlig diagnos och precisionsmedicin för att spåra viktiga molekyler inuti kroppen i realtid. Teamet föreslog tillämpningar för att övervaka fysiologiska signaler och läkemedelskoncentrationer i ett återkopplingssystem för återkoppling av läkemedel och förväntar sig att den bärbara sensorn ska inspirera en rad multidisciplinära tillämpningar.
© 2021 Science X Network