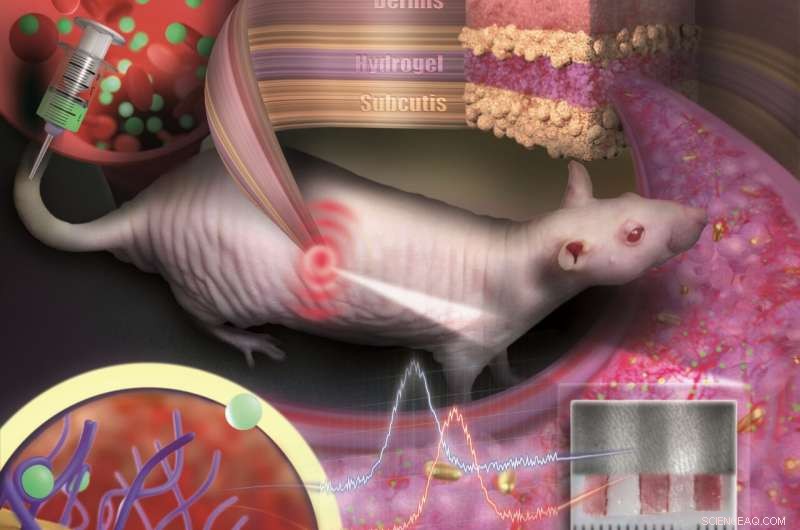
Guldnanopartiklar inbäddade i en porös hydrogel kan implanteras under huden och användas som medicinska sensorer. Sensorn är som en osynlig tatuering som avslöjar koncentrationsförändringar av ämnen i blodet genom färgförändring. Kredit:Nanobiotechnology Group, JGU Institutionen för kemi
Idén om implanterbara sensorer som kontinuerligt överför information om vitala värden och koncentrationer av substanser eller läkemedel i kroppen har fascinerat läkare och forskare under lång tid. Sådana sensorer möjliggör konstant övervakning av sjukdomsprogression och terapeutisk framgång. Dock, tills nu, implanterbara sensorer har inte varit lämpliga att stanna kvar i kroppen permanent och behöver bytas ut efter några dagar eller veckor.
Det finns också problemet med implantatavstötning eftersom immunsystemet känner igen sensorn som ett främmande föremål. Med många tekniker, sensorns färg, som indikerar koncentrationsförändringar, är instabil och bleknar med tiden. Forskare vid Johannes Gutenberg University Mainz (JGU) har utvecklat en ny typ av implanterbar sensor som kan implanteras i kroppen i flera månader. Sensorn är baserad på färgstabila guldnanopartiklar som är modifierade med receptorer för specifika molekyler. Inbäddad i en konstgjord polymervävnad, nanogoldet implanteras under huden, där den rapporterar förändringar i läkemedelskoncentrationer genom att ändra dess färg.
Professor Carsten Soennichsens forskargrupp vid JGU har använt guldnanopartiklar som sensorer för att detektera små mängder proteiner i mikroskopiska flödesceller i många år. Guldnanopartiklar fungerar som små antenner för ljus:de absorberar och sprider det kraftigt, och verkar färgglada. De reagerar på förändringar i sin omgivning genom att ändra färg. Soennichsens team har utnyttjat detta koncept för implanterad medicinsk avkänning.
För att förhindra att de små partiklarna sprids eller bryts ned av immunceller, de är inbäddade i en porös hydrogel med en vävnadsliknande konsistens. När det väl implanterats under huden, små blodkärl och celler växer in i porerna. Sensorn är integrerad i vävnaden och stöts inte bort som en främmande kropp. "Vår sensor är som en osynlig tatuering, inte mycket större än en krona och tunnare än en millimeter, sa professor Carsten Soennichsen, chef för Nanobiotechnology Group på JGU. Eftersom guldnanopartiklarna reflekteras i den infraröda våglängden, de är inte synliga för ögat. Dock, en speciell typ av mätanordning kan upptäcka deras färg icke-invasivt genom huden.
I deras studie publicerad i Nanobokstäver , JGU-forskarna implanterade sina guldnanopartikelsensorer under huden på hårlösa råttor. Färgförändringar i dessa sensorer övervakades efter administrering av olika doser av ett antibiotikum. Läkemedelsmolekylerna transporterades till sensorn via blodomloppet. Genom att binda till specifika receptorer på ytan av guldnanopartiklarna, de inducerar färgförändring som är beroende av läkemedelskoncentrationen. Tack vare de färgstabila guldnanopartiklarna och den vävnadsintegrerande hydrogelen, sensorn visade sig förbli mekaniskt och optiskt stabil under flera månader.
"Vi är vana vid att färgade föremål bleker med tiden. Guldnanopartiklar, dock, blek inte, men behålla sin färg permanent. Eftersom de lätt kan beläggas med olika receptorer, de är en idealisk plattform för implanterbara sensorer, " förklarade Dr Katharina Kaefer, första författare till studien.
Det nya konceptet är generaliserbart och har potential att förlänga livslängden för implanterbara sensorer. I framtiden, guld nanopartikelbaserade implanterbara sensorer kan användas för att observera koncentrationer av biomarkörer eller läkemedel i kroppen samtidigt. Sådana sensorer kan hitta tillämpning i läkemedelsutveckling, medicinsk forskning eller personlig medicin, såsom hantering av kroniska sjukdomar.
Soennichsen hade idén att använda guldnanopartiklar som implanterade sensorer 2004, när han började sin forskning i biofysisk kemi som juniorprofessor i Mainz. Dock, projektet realiserades inte förrän 10 år senare i samarbete med Dr. Thies Schroeder och Dr. Katharina Kaefer, båda forskarna vid JGU. Schroeder hade erfarenhet av biologisk forskning och försöksdjursvetenskap och hade redan genomfört flera års forskningsarbete i USA.
Kaefer letade efter ett spännande ämne för sin doktorsexamen och var särskilt intresserad av projektets komplexa och tvärvetenskapliga karaktär. De första resultaten ledde till ett stipendium som tilldelades Kaefer av Max Planck Graduate Center (MPGC) samt ekonomiskt stöd från Stiftung Rheinland-Pfalz für Innovation. "Ett sådant projekt kräver många människor med olika vetenskaplig bakgrund. Steg för steg, vi kunde övertyga fler och fler människor om vår idé, sade Soennichsen. Till slut, det var tvärvetenskapligt lagarbete som resulterade i den framgångsrika utvecklingen av den första funktionella implanterade sensorn med guldnanopartiklar.