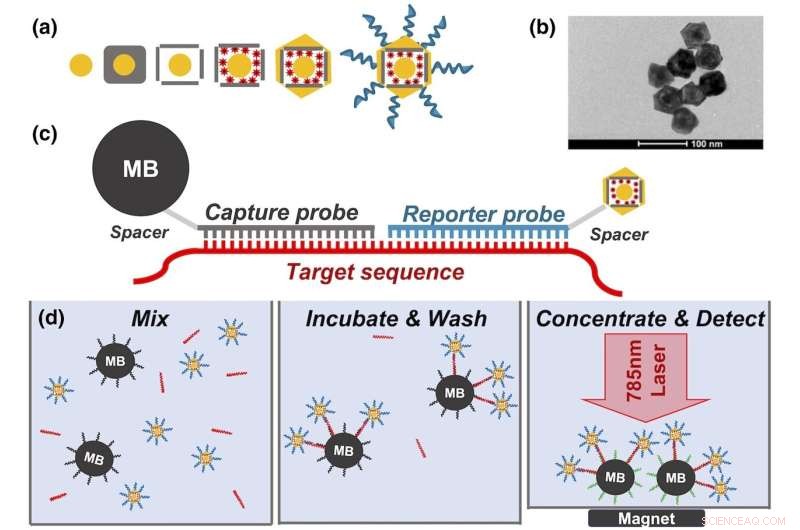
(a) Steg i nanorrattlesyntes:20 nm Au-sfärer, tillväxt av Ag-kub, galvanisk ersättning som resulterar i Au@Ag-bur, färgladdning, slutlig Au-beläggning och funktionalisering av DNA-sond. (b) TEM för nanorrattle. (c) Hybridiseringsschema för hybridiseringsanalys av nanorrattle och magnetiska pärlor. (d) Nanorrattle-analyssteg:blanda magnetiska pärlor, nanorattles och mål; inkubera; koncentrera; och upptäcka. TEM, transmissionselektronmikroskopi. Kredit:Journal of Raman Spectroscopy (2022). DOI:10.1002/jrs.6447
Forskare vid Duke University har utvecklat en unik typ av nanopartikel som kallas en "nanorattle" som avsevärt förbättrar ljuset som emitteras inifrån dess yttre skal.
Tillvägagångssättet är laddat med ljusspridande färgämnen som kallas Raman-reportrar som vanligtvis används för att upptäcka biomarkörer för sjukdomar i organiska prover, och metoden kan förstärka och detektera signaler från separata typer av nanosonder utan att behöva en dyr maskin eller läkare för att läsa resultaten.
I en liten proof-of-concept-studie identifierade nanorattlarna exakt huvud- och halscancer genom en AI-aktiverad point-of-care-enhet som kan revolutionera hur dessa cancerformer och andra sjukdomar upptäcks i områden med låga resurser för att förbättra den globala hälsan.
Resultaten visades online den 2 september i Journal of Raman Spectroscopy .
"Konceptet att fånga Raman-reportrar i dessa så kallade nanorattlar har gjorts tidigare, men de flesta plattformar hade svårt att kontrollera de inre dimensionerna", säger Tuan Vo-Dinh, R. Eugene och Susie E. Goodsons framstående professor i biomedicinsk teknik vid Duke.
"Vår grupp har utvecklat en ny typ av sond med ett exakt inställbart gap mellan den inre kärnan och det yttre skalet, vilket gör att vi kan ladda flera typer av Raman-reportrar och förstärka deras ljusemission som kallas ytförstärkt Raman-spridning," Vo-Dinh sa.
För att göra nanorrattlar börjar forskarna med en solid guldsfär som är cirka 20 nanometer bred. Efter att ha odlat ett lager av silver runt guldkärnan för att göra en större sfär (eller kub), använder de en korrosionsprocess som kallas galvanisk ersättning som hålar ut silvret och skapar ett burliknande skal runt kärnan. Strukturen blötläggs sedan i en lösning som innehåller positivt laddade Raman-reportrar, som dras in i den yttre buren av den negativt laddade guldkärnan. De yttre skroven täcks sedan av ett extremt tunt lager guld för att låsa in Raman-reportrarna.
Resultatet är en nanosfär (eller nanokub) cirka 60 nanometer bred med en arkitektur som liknar en skallra - en guldkärna fångad i ett större yttre silver-guldskal. Gapet mellan de två är bara några få nanometer, vilket är precis tillräckligt stort för att passa Raman-reportrarna.

De första guldnanosfärfröna (till vänster) är omgivna av en ihålig, porös silverbur (mitten) och blir en nanorskalla fylld med ljusspridande färgämnen inuti ett guld yttre skal (höger). Nanorattlarna kan förstärka och upptäcka signaler från olika typer av nanosonder utan att behöva en dyr maskin eller läkare för att läsa resultaten. Kredit:Tuan Vo-Dinh, Duke University
Dessa snäva toleranser är viktiga för att kontrollera Raman-signalförstärkningen som nanorrattlarna producerar.
När en laser lyser på nanorrattlarna, färdas den genom det extremt tunna yttre skalet och träffar Raman-reportrarna inuti, vilket får dem att avge sitt eget ljus. På grund av hur nära ytorna på guldkärnan och det yttre guld/silverskalet är samman, exciterar lasern också grupper av elektroner på metallstrukturerna, så kallade plasmoner. Dessa grupper av elektroner skapar ett extremt kraftfullt elektromagnetiskt fält på grund av plasmonernas interaktion av den metalliska kärnan-skal-arkitekturen, en process som kallas plasmonisk koppling, som förstärker ljuset som sänds ut av Raman-reportrarna miljontals gånger om.
"När vi hade fått nanorrattlarna att fungera ville vi göra bioavkänningsanordningar för att upptäcka infektionssjukdomar eller cancer innan folk ens vet att de är sjuka," sa Vo-Dinh. "Med hur kraftfull signalförstärkningen av nanorattlarna är, trodde vi att vi kunde göra ett enkelt test som lätt kunde läsas av vem som helst vid vårdplatsen."
I den nya tidningen tillämpar Vo-Dinh och hans medarbetare nanorrattle-tekniken på en lab-on-a-stick-enhet som kan upptäcka huvud- och nackcancer, som uppträder var som helst mellan axlarna och hjärnan, vanligtvis i mun, näsa och hals. Överlevnaden för dessa cancerformer har svävat mellan 40 och 60 procent i årtionden. Även om denna statistik har förbättrats under de senaste åren i USA, har den blivit värre i miljöer med låga resurser, där riskfaktorer som rökning, drickande och betelnötstuggning är mycket vanligare.
"I miljöer med låga resurser uppträder dessa cancerformer ofta i avancerade stadier och resulterar i dåliga resultat, delvis på grund av begränsad undersökningsutrustning, brist på utbildad sjukvårdspersonal och i princip obefintliga screeningprogram", säger Walter Lee, professor i huvud- och nacke kirurgi och kommunikationsvetenskap och strålningsonkologi vid Duke, och en samarbetspartner i forskningen.
"Att ha förmågan att upptäcka dessa cancerformer tidigt bör leda till tidigare behandling och förbättring av resultat, både vad gäller överlevnad och livskvalitet", sa Lee. "Det här tillvägagångssättet är spännande eftersom det inte är beroende av en patologgranskning och potentiellt skulle kunna användas vid vårdpunkten."
Prototypenheten använder specifika genetiska sekvenser som fungerar som kardborre för de biomarkörer som forskarna letar efter - i det här fallet ett specifikt mRNA som är alltför rikligt hos personer med cancer i huvud och hals. När mRNA i fråga finns, fungerar det som ett tjuder som binder nanorrattlar till magnetiska pärlor. Dessa pärlor koncentreras sedan och hålls på plats av en annan magnet medan allt annat sköljs bort. Researchers can then use a simple, inexpensive handheld device to look for light emitted from the nanorattles to see if any biomarkers were caught.
In the experiments, the test determined whether or not 20 samples came from patients that had head and neck cancer with 100% accuracy. The experiments also showed that the nanorattle platform is capable of handling multiple types of nanoprobes, thanks to a machine learning algorithm that can tease apart the separate signals, meaning they can target multiple biomarkers at once. This is the goal of the group's current project funded by the National Institutes of Health.
"Many mRNA biomarkers are overly abundant in multiple types of cancers, while other biomarkers can be used to evaluate patient risk and future treatment outcome," Vo-Dinh said. "Detecting multiple biomarkers at once would help us differentiate between cancers, and also look for other prognostic markers such as Human Papillomavirus (HPV), and both positive and negative controls. Combining mRNA detection with novel nanorattle biosensing will result in a paradigm shift in achieving a diagnostic tool that could revolutionize how these cancers and other diseases are detected in low-resource areas." + Utforska vidare