Nyligen designade ett forskarlag under ledning av prof. Wu Zhengyan från Hefei Institutes of Physical Science, Chinese Academy of Sciences, i samarbete Binzhou Medical University, framgångsrikt en nanostruktur som förbättrar upptäckten och behandlingen av tumörer.
Deras arbete, nyligen publicerat i Small , fokuserar på att skapa en mycket specifik metod för att diagnostisera och behandla tumörer med en kombination av magnetisk resonanstomografi och enzymaktivitet.
"Vissa kemiska reaktioner som kallas den metalljonförmedlade Fenton-liknande reaktionen, kan snabbt öka nivåerna av skadliga reaktiva syrearter och bromsa tumörtillväxten", sa prof. Wu, "och enzymer gjorda av koppar, som har hög katalytisk aktivitet och svarar bra på tumörmiljön, är inte särskilt stabila."
Därför möjliggör utveckling av ett tumörmikromiljöreagerande nano-teranostiskt medel tidig tumördiagnos och övervakning av behandlingseffektivitet och skyddar kopparbaserade nanoenzymer från deaktivering på grund av steriskt hinder.
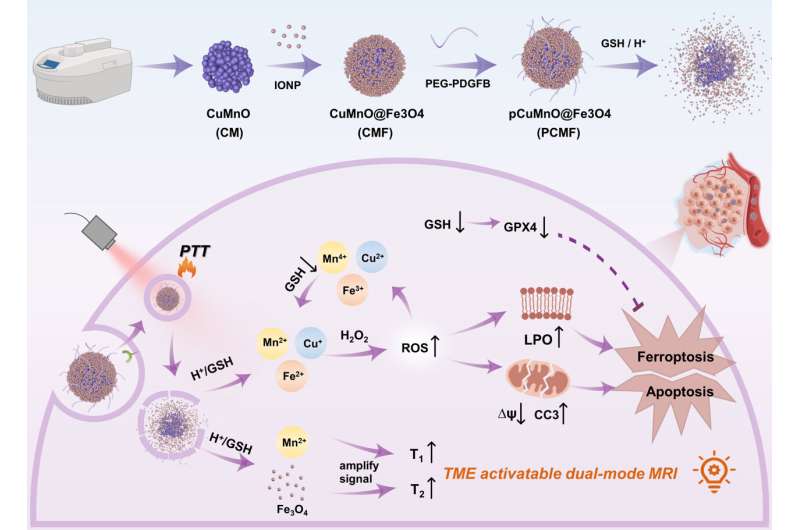
För att lösa detta problem utvecklade forskargruppen ett specialiserat nanoenzym som heter CuMnO@Fe3 O4 (CMF) med en kärna-skalstruktur som svarar på tumörens mikromiljö. De fäste sedan PDGFB-målligander till ytan av CMF, vilket skapade ett specifikt nanoenzym för tumörer som kallas PCMF.
Kärn-skal-designen av PCMF förhindrar interferens från tiolgrupper som finns i stora molekyler under cirkulation i blodomloppet. Detta främjar antitumöraktiviteten hos PCMF.
PCMF uppvisar både T1 och T2 dubbelkontrastavbildningsförmåga när den aktiveras av svag syra och glutation. Detta innebär att den kan ge förbättrad bildkontrast för att diagnostisera tumörer.
Dessutom bryts PCMF ned i tumörens mikromiljö och frigör metalljoner såväl som ultraliten järnoxid. Denna process förbrukar glutation, accelererar Fenton- och Fenton-liknande reaktioner, ökar nivåerna av intracellulära reaktiva syrearter och inducerar apoptos och ferroptos i cancerceller.
PCMF har också fototermisk omvandlingsförmåga och kan därför användas för kombinerad fototermisk och nanokatalytisk terapi, vilket förbättrar anti-canceraktiviteten.
Enligt teamet ger detta arbete insikter i hur man kan uppnå mycket känslig tumörspecifik terapeutisk diagnos.
Mer information: Wenteng Xie et al, Tumor Microenvironment-Activated Nanostructure to Enhance MRI-kapacitet och nanozymaktivitet för mycket tumörspecifika multimodala terapier, Små (2023). DOI:10.1002/smll.202306446
Journalinformation: Liten
Tillhandahålls av Chinese Academy of Sciences