The Beach Boys ikoniska hitsingel "Good Vibrations" får ett helt nytt lager av betydelse tack vare en nyligen upptäckt av forskare och medarbetare från Rice University, som har upptäckt ett sätt att förstöra cancerceller genom att använda förmågan hos vissa molekyler att vibrera kraftigt när det stimuleras av ljus.
Forskarna fann att atomerna i en liten färgämnesmolekyl som används för medicinsk avbildning kan vibrera unisont - och bildar vad som kallas en plasmon - när de stimuleras av nära-infrarött ljus, vilket gör att cancercellernas cellmembran brister. Enligt studien publicerad i Nature Chemistry , hade metoden en effektivitet på 99 % mot labbkulturer av humana melanomceller, och hälften av mössen med melanomtumörer blev cancerfria efter behandling.
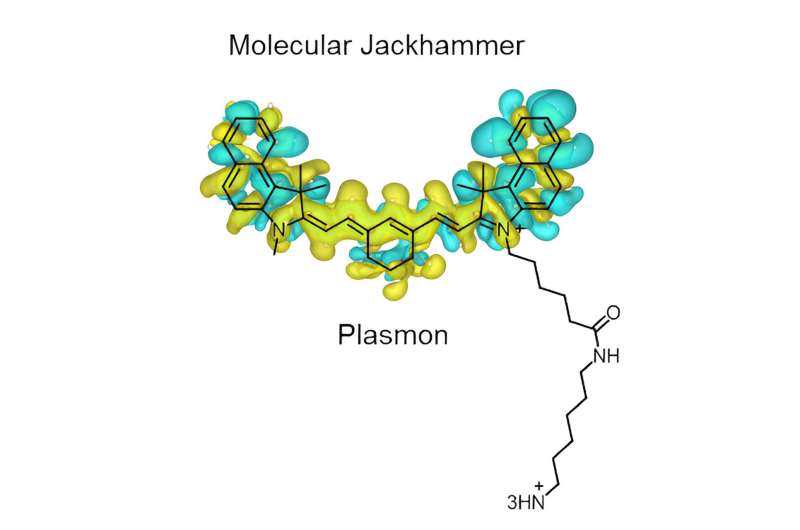
"Det är en helt ny generation av molekylära maskiner som vi kallar molekylära jackhammers", säger riskemist James Tour, vars labb tidigare har använt föreningar i nanoskala utrustade med en ljusaktiverad paddelliknande kedja av atomer som snurrar kontinuerligt i samma riktning för att borra igenom. det yttre membranet av smittsamma bakterier, cancerceller och behandlingsresistenta svampar.
Till skillnad från övningarna i nanoskala baserade på Nobelpristagaren Bernard Feringas molekylära motorer, använder molekylära jackhammare en helt annan – och aldrig tidigare skådad – verkningsmekanism.
"De är mer än en miljon gånger snabbare i sin mekaniska rörelse än de tidigare motorerna av Feringa-typ, och de kan aktiveras med nära-infrarött ljus snarare än synligt ljus," sa Tour.
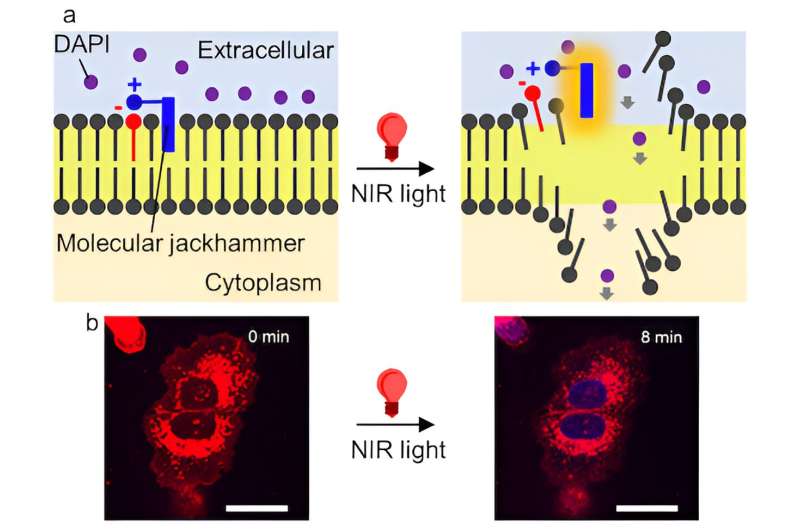
Nära-infrarött ljus kan tränga in mycket djupare in i kroppen än synligt ljus, komma åt organ eller ben utan att skada vävnaden.
"Nära-infrarött ljus kan gå så djupt som 10 centimeter (~ 4 tum) in i människokroppen i motsats till endast en halv centimeter (~ 0,2 tum), penetrationsdjupet för synligt ljus, som vi använde för att aktivera nanoborrarna, " sa Tour, Rice's T. T. och W. F. Chao professor i kemi och professor i materialvetenskap och nanoteknik. "Det är ett stort framsteg."
Hamrarna är aminocyaninmolekyler, en klass av fluorescerande syntetiska färgämnen som används för medicinsk bildbehandling.
"Dessa molekyler är enkla färgämnen som människor har använt under en lång tid", säger Ciceron Ayala-Orozco, en risforskare som är huvudförfattare till studien. "De är biokompatibla, stabila i vatten och mycket bra på att fästa sig på cellernas feta ytterbeklädnad. Men även om de användes för avbildning visste folk inte hur de skulle aktivera dessa som plasmoner."
Ayala-Orozco studerade till en början plasmons som doktorand i forskargruppen ledd av Rices Naomi Halas.

"På grund av deras struktur och kemiska egenskaper kan kärnorna i dessa molekyler oscillera synkront när de utsätts för rätt stimulans," sa Ayala-Orozco. "Jag såg ett behov av att använda egenskaperna hos plasmoner som en behandlingsform och var intresserad av Dr. Tours mekaniska tillvägagångssätt för att hantera cancerceller. Jag kopplade i princip ihop prickarna.
"De molekylära plasmonerna vi identifierade har en nästan symmetrisk struktur med en arm på ena sidan. Armen bidrar inte till den plasmoniska rörelsen, men den hjälper till att förankra molekylen till lipiddubbelskiktet i cellmembranet."
Forskarna var tvungna att bevisa att molekylernas verkningssätt varken kunde kategoriseras som en form av fotodynamisk eller fototermisk terapi.
"Vad som behöver lyftas fram är att vi har upptäckt en annan förklaring till hur dessa molekyler kan fungera," sa Ayala-Orozco. "Detta är första gången en molekylär plasmon används på detta sätt för att excitera hela molekylen och för att faktiskt producera mekanisk verkan som används för att uppnå ett visst mål - i det här fallet att riva isär cancercellers membran. Den här studien handlar om ett annat sätt att behandla cancer med hjälp av mekaniska krafter i molekylär skala."
Forskare vid Texas A&M University under ledning av Jorge Seminario, en kvantkemist och professor i kemiteknik, utförde tidsberoende densitetsfunktionella teorianalyser av de molekylära egenskaperna som är involverade i jackhammering-effekten. Cancerstudierna utfördes på möss vid University of Texas MD Anderson Cancer Center i samarbete med Dr. Jeffrey Myers, professor och ordförande för Department of Head and Neck Surgery och chef för translationell forskning för Division of Surgery.
Mer information: Ciceron Ayala-Orozco et al, Molecular jackhammers utrotar cancerceller genom vibronic-driven verkan, Nature Chemistry (2023). DOI:10.1038/s41557-023-01383-y
Journalinformation: Naturkemi
Tillhandahålls av Rice University