Många sjukdomar kan framgångsrikt behandlas i den enkla miljön i en cellodlingsrätt, men för att framgångsrikt behandla riktiga människor måste läkemedelsagenten ta en resa genom den oändligt mycket mer komplexa miljön i våra kroppar och anlända, intakt, in i de drabbade cellerna. Denna process, som kallas läkemedelsleverans, är en av de viktigaste hindren inom medicin.
Ett samarbete mellan Lawrence Berkeley National Laboratory (Berkeley Lab) och Genentech, en medlem av Roche Group, arbetar för att bryta igenom några av flaskhalsarna för läkemedelsleveransen genom att designa de mest effektiva lipidnanopartiklarna (LNP) – små sfäriska påsar gjorda av fettmolekyler som kapslar in terapeutiska medel tills de dockar med cellmembran och frigör deras innehåll. Det första läkemedlet som använde LNP:er godkändes 2018, men leveransmetoden ökade globalt med Pfizer och Moderna mRNA COVID-vacciner.
"Det är ett ganska smart system, för om du bara levererar RNA självt till människokroppen, bryts RNA ned av nukleaser och kan inte lätt passera cellmembranet på grund av dess storlek och laddning, men LNP:erna levererar det säkert in i cellen, " förklarade medförfattaren Chun-Wan Yen, en senior rektor i Genentechs Small Molecule Pharmaceutical Sciences-grupp.
LNP:er undersöks nu brett som ett leveranssystem för vacciner mot andra infektionssjukdomar eller terapeutiska vacciner mot cancer. Livsdugligheten för dessa nya tillämpningar kommer att vara beroende av hur väl lipidhöljena smälter samman med målceller, hur stabila läkemedels-LNP-formuleringarna är i lagring (så att de har en lång hållbarhetstid) och hur stabila de är i kroppen (så att de kan ge långvarig läkemedelsaktivitet).
Alla dessa egenskaper styrs av blandningen av molekyler som används för att skapa LNP, och den resulterande 3D-strukturen av partikeln. Teamet under Yen och andra medledare Greg Hura och Michal Hammel, båda biofysiker från Berkeley Lab, har under flera år studerat hur man kan ställa in strukturen hos LNP för önskade egenskaper.
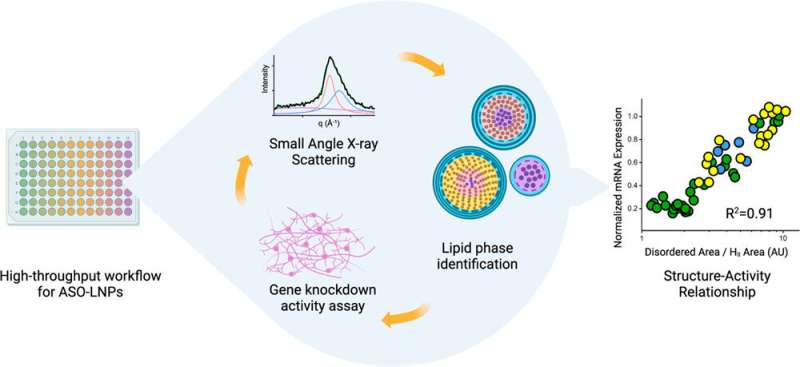
Deras senaste artikel, nyligen publicerad i ACS Nano , dokumenterar hur ett arbetsflöde med hög genomströmning tillåter dem att producera och karakterisera LNP:er i rekordfart. Studien inkluderar också den första demonstrationen någonsin av hur LNP-strukturen korrelerar med aktiviteten av dess innehåll, vilket för denna undersökning var en antisensoligonukleotid (ASO). ASO:er är små bitar av RNA eller DNA-baspar som blockerar genuttryck genom att binda till strängar av mRNA och förhindra dem från att översättas till proteiner. ASO är ett utmärkt sätt att behandla sjukdomar orsakade av felaktiga proteiner eller överflöd av ett protein. Men, liksom mRNA, är de mottagliga för strövande nukleaser – enzymer som bryter ner RNA och DNA – och celler tar inte upp dem så lätt.
Forskarna upptäckte att ASO-bärande LNP med prydligt ordnade, tätt packade inre strukturer ledde till bättre tystnad av en felaktig gen i mänskliga neuroner som är associerad med en degenerativ sjukdom, jämfört med LNP som hade en mer oordnad struktur. Resultaten kom från cellulära aktiviteter, inte från djurstudier, så det återstår fortfarande mer arbete, men teamet är glada att bygga vidare på dessa insikter med hjälp av de kompletterande verktygen från varje institution.

"Vi genererar LNP:er i hög genomströmning och Greg och Michals team kan erbjuda högkapacitetsanalysen," sa Yen. "Om du kollar om publikationen nuförtiden, gör de vanligtvis bara en eller två formuleringar, men för oss är det annorlunda. Vi kan generera stora datamängder, och jag tror att det är anledningen till att vi kan ha detta mycket unika och coola fynd."
"Det här dokumentet anger verkligen metoden som vi kommer att tillämpa på de tusentals andra formuleringar som vi tänker karakterisera," tillade Hura, som är en del av Berkeley Labs biovetenskapsområde. "Vi hoppas att det här kommer att vara en generell metod för människor att optimera sina lipidnanopartiklar. Oavsett om det är vacciner, och igen, har vaccinerna fått störst uppmärksamhet hittills eller längre. Den här typen av terapi har en mycket bred tillämpning utöver det. ."
LNP:s strukturer påverkas av hur du blandar dem, vad du blandar ihop och i vilken ordning. LNP har fyra ingredienser - joniserbara lipider, hjälpfosfolipider, kolesterol och polyetylenglykollipider (PEG-lipider) - och varje ingrediens har olika former. Dessutom kan de kombineras i olika förhållanden, vilket leder till ett exponentiellt antal möjliga formler. Ytterligare komplicerar saken, LNPs förändras med tiden. En formulering som börjar som en snygg, tätpackad sfär kommer så småningom att förvandlas till en mer oordnad struktur.
Forskare vid Genentech utvecklade ett robotdrivet arbetsflöde som kan generera hundratals LNP-formuleringar på bara några timmar. Prover av varje formulering förs sedan till Berkeley Lab för att utföra småvinklar röntgenspridning (SAXS) vid Advanced Light Source, en cirkulär partikelaccelerator som skapar röntgenstrålar med olika energier.
Den biologiska SAXS-strållinjen kan snabbt bearbeta många prover, och till skillnad från andra former av röntgendiffraktion på biologiska material behöver proverna inte frysas eller kristalliseras – vilket kan förändra strukturen på LNP:erna och hindra forskarna från att upptäcka vad LNP:er skulle se ut vid fysiologiska temperaturer i människokroppen. SAXS låter dem också ta ögonblicksbilder av LNP:er vid en specificerad tidpunkt för att bestämma deras strukturella livslängd.
Dessutom använder Genentech-teamet en accelererad process för att studera hur LNP påverkar genuttrycket i sina målceller. Genom att kombinera alla dessa snabba tekniker kan hela samarbetet screena potentiella LNP i en oöverträffad hastighet.
Yen planerar att fortsätta använda SAXS-strållinjen för att studera små detaljer, som hur en 1% förändring i ingredienskoncentrationen eller att använda en ny maskin under produktionen kan påverka LNP:s cellulära aktivitet, såväl som stora frågor, till exempel om LNP:er beter sig annorlunda om de är transportera andra lasttyper och hur de interagerar med olika målceller.
"Vi vet att mRNA LNP fungerar, men det finns fortfarande en enorm kunskapslucka," sa Yen. "Det är därför jag känner att vår tidning är en pionjär inom detta område och förhoppningsvis kan vi också generera mer data och förståelse för framtida tillämpningar."
Mer information: Michal Hammel et al, korrelering av strukturen och gentystnadsaktiviteten hos oligonukleotidladdade lipidnanopartiklar med röntgenspridning med liten vinkel, ACS Nano (2023). DOI:10.1021/acsnano.3c01186
Journalinformation: ACS Nano
Tillhandahålls av Lawrence Berkeley National Laboratory