En ny modelleringsteknik gör det möjligt för forskare att se vad som händer inuti röda blodkroppar som påverkas av sicklecellsjukdom. Upphovsman:Karniadakis lab / Brown University
Datormodeller som utvecklats av matematiker från Brown University visar nya detaljer om vad som händer inuti en röd blodkropp som drabbats av sicklecellsjukdom. Forskarna sa att de hoppas att deras modeller, beskrivs i en artikel i Biofysisk tidskrift , hjälper till att bedöma läkemedelsstrategier för att bekämpa den genetiska blodsjukdomen, som påverkar miljontals människor världen över.
Sickelcellsjukdom påverkar hemoglobin, molekyler i röda blodkroppar som ansvarar för att transportera syre. I normala röda blodkroppar, hemoglobin sprids jämnt i cellen. I säckröda blodkroppar, muterat hemoglobin kan polymerisera när det berövas syre, samlar sig till långa polymerfibrer som trycker mot cellmembranen, tvingar dem ur form. Den stela, dåligt formade celler kan fastna i små kapillärer i hela kroppen, som leder till smärtsamma episoder som kallas sicklecellskris.
"Målet med vårt arbete är att modellera både hur dessa seglhemoglobinfibrer bildas såväl som de mekaniska egenskaperna hos dessa fibrer, "sa Lu Lu, en doktorsexamen student i Brown Division of Applied Mathematics och studiens huvudförfattare. "Det hade funnits separata modeller för var och en av dessa saker som utvecklats individuellt av oss, men detta sammanför dem till en heltäckande modell. "
Modellen använder detaljerade biomekaniska data om hur seglhemoglobinmolekyler beter sig och binder med varandra för att simulera sammansättningen av en polymerfiber. Innan detta arbete, problemet hade varit att när fibern växer, det gör också mängden data modellen måste knäcka. Att modellera en hel polymerfiber i cellulär skala med hjälp av detaljerna i varje molekyl var helt enkelt för beräknande dyrt.
"Även världens snabbaste superdatorer skulle inte klara av det, "sa George Karniadakis, professor i tillämpad matematik vid Brown och tidningens seniorförfattare. "Det händer alldeles för mycket och inget sätt att fånga det hela beräknat. Det var vad vi kunde övervinna med detta arbete."
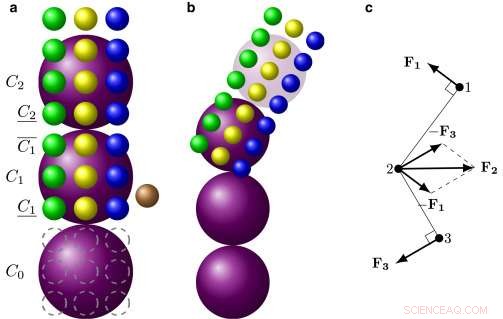
Forskarnas lösning var att tillämpa det de kallar ett mesoskopiskt adaptivt upplösningssystem eller MARS. MARS -modellen beräknar den detaljerade dynamiken för varje enskild hemoglobinmolekyl endast vid varje ände av polymerfibrer, där nya molekyler rekryteras i fibern. När fyra lager av en fiber har etablerats, modellen ringer automatiskt tillbaka upplösningen vid vilken den representerar det avsnittet. Modellen behåller den viktiga informationen om hur fibern beter sig mekaniskt, men glansar över de fina detaljerna för varje bestående molekyl.
"Genom att eliminera de fina detaljerna där vi inte behöver dem, vi utvecklar en modell som kan simulera hela processen och dess effekter på en röd blodkropp, "Sa Karniadakis.
Med hjälp av de nya MARS -simuleringarna, forskarna kunde visa hur olika konfigurationer av växande polymerfibrer kan producera celler med olika former. Även om sjukdomen får sitt namn för att den orsakar att många röda blodkroppar får en sigdliknande form, det finns faktiskt en mängd olika onormala cellformer närvarande. Denna nya modelleringsmetod visade nya detaljer om hur olika fiberstrukturer inuti cellen producerar olika cellformer.
"Vi kan ta fram en polymerisationsprofil för var och en av de celltyper som är associerade med sjukdomen, "Sade Karniadakis." Nu är målet att använda dessa modeller för att leta efter sätt att förebygga sjukdomsdebut. "
Det finns bara ett läkemedel på marknaden som har godkänts av FDA för behandling av sicklecell, Säger Karniadakis. Det läkemedlet, kallas hydroxyurea, antas fungera genom att öka mängden fetalt hemoglobin - den typ av hemoglobin som barn föds med - i patientens blod. Fosterhemoglobin är resistent mot polymerisation och, när den finns i tillräcklig mängd, tros störa polymerisationen av säcellhemoglobin.
Med hjälp av dessa nya modeller, Karniadakis och hans kollegor kan nu köra simuleringar som inkluderar fetalt hemoglobin. Dessa simuleringar kan hjälpa till att bekräfta att fetalt hemoglobin verkligen stör polymerisation, samt hjälp med att fastställa hur mycket fetalt hemoglobin som är nödvändigt. Det kan hjälpa till att upprätta bättre dosriktlinjer eller utveckla nya och mer effektiva läkemedel, säger forskarna.
"Modellerna ger oss ett sätt att göra preliminära tester på nya metoder för att stoppa denna sjukdom, "Karniadakis sa." Nu när vi kan simulera hela polymerisationsprocessen, vi tror att modellerna kommer att vara mycket mer användbara. "