
Credit:Aarhus University Förster resonance energy transfer (FRET) kombinerar laserljus och ultrakänsliga kameror som skickar signaler till en enskild molekyl. Denna signal sprids till den andra färgmolekylen på pumpen, som börjar överföra ljus av en annan färg. Gruppen fokuserar på förhållandet mellan de olika färgerna, som är registrerat i ett specialbyggt ljusmikroskop. Dessa mätningar ger information om pumpens rörelser. Upphovsman:Mateusz Dyla
För första gången, forskare har observerat jonpumparna som aktiverar celltransport och signalsystem. Detta säkerställer funktionen hos biomolekylära mekanismer.
Varje kalciumpump mäter bara några nanometer i varje riktning, och ligger i cellmembranen. Men trots sin ringa storlek, det är avgörande för livet. Denna pump är anledningen till att våra muskler kan dra ihop sig, och att neuroner kan skicka signaler. Om den lilla pumpen slutade fungera, celler skulle sluta kommunicera. Det är därför celler använder så mycket av sin energi - ungefär en fjärdedel av kroppens bränsle, känd som ATP - för att hålla pumparna igång.
Det finns många saker som vi fortfarande inte vet om strukturen och funktionen för denna vitala pump. Kunskap om pumpen är avgörande för att förstå energibalansen och andra viktiga funktioner i kroppen.
En dansk forskargrupp har just publicerat en ny studie som för första gången visar hur pumpen fungerar på nivå med en enda molekyl, och hur det säkerställer att joner pumpas i rätt riktning. Med andra ord, hur pumpen fungerar som en molekylär enkelriktad gata. Upptäckten har just publicerats i den prestigefyllda tidskriften Natur .
"Detta arbete representerar nästa steg i en djupgående och viktig strävan efter att förstå pumpens atomstruktur och funktion. Vi är nu ett steg närmare att förstå hur jonpumparna säkerställer cellernas funktioner. Vi har präglat hur den pumpar ut joner ur cellen på en oöverträffad detaljnivå. Betydelsen av sådan grundläggande kunskap om biofysiska processer kan bara underskattas.Det kommer att ha ett stort inflytande på vår förståelse av livsprocesser och, i tid, om sjukdomsbehandling, "säger professor Poul Nissen. Professor Nissen är en av världens ledande experter på denna pumpfamilj och medförfattare till tidningen.
Den molekylära backstoppen
I viss utsträckning, historien började på 1950 -talet, när professor Jens Christian Skou gjorde sitt banbrytande arbete vid Aarhus universitet, som avslöjade pumpfunktionerna i våra celler. Kalciumpumpen är en nära kusin till natriumkaliumpumpen som Skou arbetade med, och de använder en liknande pumpmekanism. Skous arbete gav honom ett Nobelpris i kemi 1997. Sedan dess har många forskare har studerat mekanismen och funktionen för dessa pumpar, däribland många vid Center for Membrane Pumps in Cells and Disease - PUMPkin - vid Aarhus University.
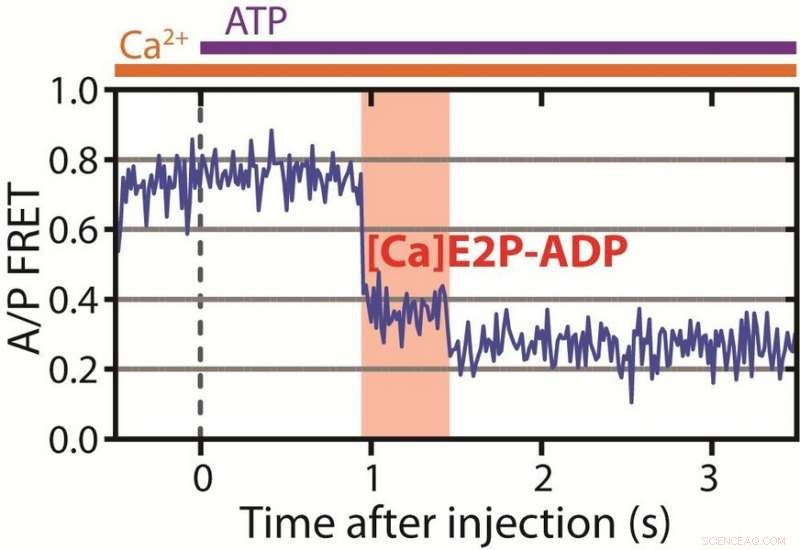
Här visas tidslinjen för pumpfunktionen, som nu avslöjas i hög tidsupplösning. Kurvan visar sambandet mellan de uppmätta fluorescerande färgerna som avges från färgämnen bundna till pumpen. Till vänster, pumpen är öppen mot cellens inre och har bundit kalciumjoner och absorberat ATP -molekylen - med andra ord, det är "laddat". Nästa steg är det nya, nyckelresultat:i det röda fältet, pumpen är i det tidigare okända stängda tillståndet, där den har inneslutit jonerna som ska skickas ut ur cellen. Det sista steget som visas visar att pumpen har öppnat och släppt ut kalciumjoner i omgivningen. Härifrån, den kan inte återgå till det markerade tillståndet. Upphovsman:Daniel Terry/Dyla
En viktig insikt i den nya publikationen gäller jontransportens enkelriktade karaktär. Tidigare, man antog att pumpens enkelriktade natur uppstod vid klyvningen av den energirika molekylen ATP. Hypotesen var att när ATP klyvs, pumpen kunde inte backa och reformera ATP. Det visade sig vara felaktigt.
"Vi har identifierat ett nytt stängt tillstånd i pumpcykeln, som pumpen bara kan komma in om kalciumjonen kommer från de intracellulära vätskorna och pumpen har klyvt ATP. Det kan inte nå detta tillstånd om jonen kommer från cellens omgivning. När kalcium frigörs från detta tillstånd, det är ”point of no return”. Detta är mekanismen som förklarar att pumpen fungerar som en pump och inte bara en passiv kanal. Denna verkligen unika insikt bygger på mycket avancerade experiment. Dessa experiment gör att vi direkt kan se pumpen göra sitt jobb för första gången, "säger postdoktor Mateusz Dyla, den första författaren till den nya artikeln.
Kalciumpumpen behöver energi, som den får genom att klyva en molekyl av ATP. Den frigjorda energin omvandlas till pumpens arbete. Detta förklarar hur stora koncentrationsgradienter byggs upp mellan insidan och utsidan av cellen. Koncentrationsskillnaden kan vara mer än 10, 000-faldigt, och denna stora skillnad är väsentlig för kommunikationen mellan celler, såsom vid nervsignalering.
Rök och speglar
Anledningen till att experimenten är så komplexa är ganska tydlig. Pumpen är så liten att den inte kan avbildas direkt i ett ljusmikroskop. Än så länge, och med stora svårigheter, forskare har skapat molekylära modeller av pumpens stabila tillstånd med hjälp av en teknik som kallas röntgenkristallografi. Detta är analogt med en stop-motion-film. Forskarna har skämtsamt hänvisat till deras visualisering av pumpens rörelse mellan dessa tillstånd som 'Pump Fiction'. Den nya studien, som har varit fem år på gång, flyttar visualiseringen från stopprörelse till levande bilder av pumpens funktionella rörelser. Teknisk förbättring av mikroskopiska tekniker har gjort det möjligt att observera det nya tillståndet.
Tekniken är känd som enmolekylär fluorescensspektroskopi, och använder ett fenomen som kallas Förster resonans energiöverföring, kort sagt FRET. Här, intensivt laserljus och ultrakänsliga kameror kombineras för att möjliggöra direkt observation av en enda molekyl genom den lilla mängd ljus som varje molekyl avger.
Forskargruppen har utnyttjat en kalciumpump från bakterien Listeria, som förbereddes för studierna genom proteinteknik. Konstruktionen av proteinet ensam tog flera år att slutföra.
I FRET -experimenten, två färgämnen är bundna till proteinet, som sedan belyses av laserljus. Ett färgämne, givaren, absorberar laserljuset och avger antingen det med en karakteristisk färg, eller alternativt överför energin till det andra färgämnet, accepteraren. Detta kommer då att avge ljus med en annan färg. Ljus kommer alltså att avges från de två färgämnena, och forskare kan mäta avståndet mellan de två färgämnena genom att mäta hur mycket ljus som avges från varje färg. Eftersom färgämnena försiktigt har införts i två specifika lägen i pumpen, dessa avståndsändringar spårar pumpens rörelser.
Enmolekyltekniken möjliggjorde de nya upptäckterna, som förklaras av stipendiat Magnus Kjærgaard, Aarhus Institute of Advanced Studies (AIAS), som också bidragit till upptäckten.
"Vi har flyttat från" Pump Fiction "till" Pump Live ". Tidigare har vi spelade alltid in signalerna från många molekyler samtidigt, som suddar ut rörelserna. Med hjälp av FRET-tekniker med en molekyl, vi kan fokusera på en molekyl i taget, vilket gör att vi direkt kan observera strukturförändringarna. Detta ger oss en video av pumpen i funktion med färre luckor. Vår Pump Fiction -film fick ursprungligen sitt namn eftersom vi visste att övergångarna mellan de olika tillstånden i cykeln var fiktiva, och att det kan finnas ytterligare insikter som gömmer sig i luckorna mellan de kända staterna. Vi har nu visat detta i överflöd, och avslöjade samtidigt kritiska nya insikter om hur pumpen fungerar, " han säger.
Förutom att öka vår kunskap om livets grundläggande processer, förståelsen av dessa pumpar kan också ha praktiska tillämpningar. Mutationer i pumparna kan orsaka defekter i hjärnceller, och detta kan orsaka neurologiska störningar som migrän, tillfällig förlamning eller neurodegenerativa störningar.
Mekanismerna för dessa jonpumpar är således avgörande för att förstå felen i pumpen, särskilt i syfte att utveckla nya läkemedel riktade mot pumpen.
"Vi har ännu inte nått det stadium där vi kan överföra vår jonpumpforskning till behandling av sjukdomar. Men de nya insikterna har lett till idéer som kan användas för att utveckla behandling av defekter vid neuronal signalering, till exempel. Men det här är arbete för framtiden. Just nu, det finns all anledning att fira avslöjandet av de intima detaljerna i ett av livets viktigaste enzymer. Arbetet har byggt på fantastiska samarbeten här på universitetet, och med forskare i USA. Vi har redan startat nya spännande samarbeten som gör att vi kan ta nästa steg, säger professor Poul Nissen.