En konstnärs uppfattning om kraften i beräkningsdesign för att utforska och belysa strukturerade peptider över det stora energilandskapet. Kredit:Vikram Mulligan/University of Washington Insittute for Protein Design
Nya beräkningsstrategier rapporterade denna vecka i Vetenskap kan hjälpa till att förverkliga löftet om peptidbaserade läkemedel. Peptider liknar proteinmolekyler, men skiljer sig i sin mindre storlek, struktur och funktioner.
Makrocykliska peptider har väckt intresse för läkemedelsindustrin, eftersom de har vissa fysikaliska och kemiska egenskaper som kan bli grunden för en ny generation av mediciner.
Små peptider har fördelarna med småmolekylära läkemedel, som aspirin, och stora antikroppsterapier, som rituximab, med färre nackdelar. De är stabila som små molekyler och potenta och selektiva som antikroppar.
Ett exempel på en framgångshistoria för makrocykliska peptidläkemedel är cyklosporin, ett immunsuppressivt medel för organtransplantationer och vissa autoimmuna sjukdomar.
Innan det arbete som beskrivs i Vetenskap papper, det fanns inget sätt att systematiskt utforma ordnade peptidmakrocykler som cyklosporin.
Naturligt förekommande peptider som kan fungera som pålitliga utgångspunkter, eller byggnadsställningar, är få. Lika frustrerande är att de ofta misslyckas med att prestera som förväntat när de används igen. Istället, forskare hade tillgripit screening av stora, slumpmässigt genererade bibliotek av föreningar i hopp om att hitta det de behövde.
Metoderna som behandlas i rapporten, "Omfattande beräkningsdesign av ordnade peptidmakrocykler" löser nu dessa problem.
Denna konceptuella illustration visar hur peptidheteropolymerer kan programmeras från mindre komponenter för att utforska ett mångsidigt energilandskap. Kredit:Ahmad Hosseinzadeh och Khosro Khosravi
Huvudförfattarna är Parisa Hossienzadeh, Gaurav Bhardwaj och Vikram Mulligan, vid University of Washington School of Medicine Department of Biochemistry och UW Institute of Protein Design. Senior författare är David Baker, professor i biokemi och chef för institutet. Baker är också utredare vid Howard Hughes Medical Institute.
"I vår tidning, " konstaterade forskarna, "vi beskriver beräkningsstrategier för att designa peptider som antar olika former med mycket hög noggrannhet och för att tillhandahålla omfattande täckning av de strukturer som kan bildas av korta peptider."
De påpekade fördelarna med denna nya beräkningsmetod:
Först, de kunde designa och sammanställa ett bibliotek med många nya stabila peptidställningar som kan tillhandahålla de grundläggande plattformarna för läkemedelskandidatarkitektur. Deras metoder kan också användas för att designa ytterligare anpassade peptider med godtyckliga former på begäran.
"Vi tog prov på det olika landskapet av former som peptider kan bilda, som en guide för att utforma nästa generations läkemedel, " sa forskarna.
Nyckeln till kontroll av molekylers geometri och kemi var designen av peptider med naturliga aminosyror, kallas L-aminosyror, och deras spegelmotsatser som innehåller D-aminosyror. (L och D står för latinska ord för att rotera åt vänster eller höger, eftersom vissa molekylära strukturer kan ha vänster- eller högerhänthet eller kiralitet).
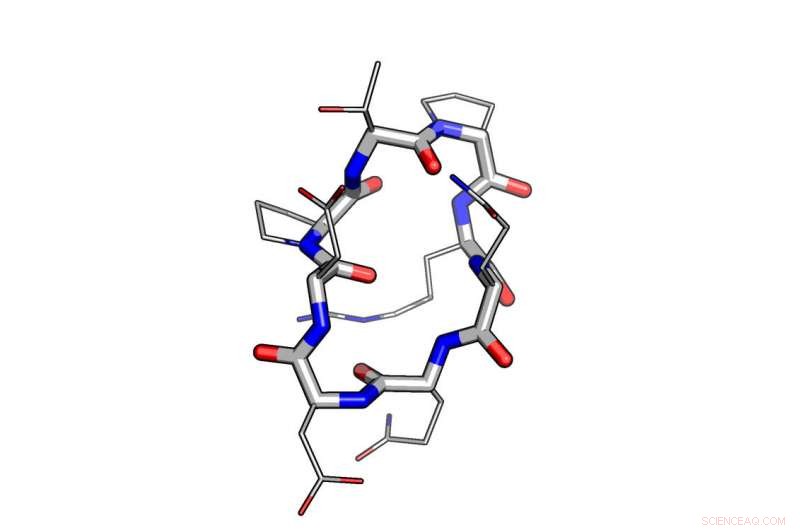
Ett exempel på användningen av beräkningsdesign vid modellering av en peptid. Kredit:University of Washington Institute for Protein Design
D-aminosyrorna förbättrade farmakologiska egenskaper genom att öka resistensen mot naturliga enzymer som bryter ner peptider. Införande av D-aminosyror i design möjliggör också ett mer varierat utbud av former.
Att designa peptider kräver intensiv datorkraft, resulterar i dyra beräkningar. Forskarna krediterade en kader av medborgarforskare och frivilliga som donerade sina extra mobiltelefonminuter och datortid. Hyak Supercomputer vid University of Washington körde också några av programmen.
Forskarna pekade på framtida riktningar för deras peptidberäkningsdesignmetoder. De hoppas kunna designa peptider som kan tränga igenom cellmembran och gå in i levande celler.
I andra aspekter, de planerar att lägga till nya funktioner till peptidstrukturer genom att stabilisera bindningsmotiven vid protein-proteingränssnitt för grundläggande vetenskapliga studier. För kliniska tillämpningar, de räknar med att använda sina metoder och byggnadsställningar för att utveckla peptidbaserade läkemedel.