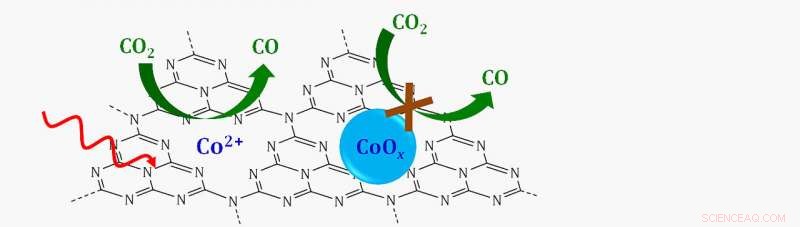
Schematisk beskrivning av en enställskatalysator i vilken enstaka koboltjoner (CO 2 +) stödd på ett grafitiskt kolkväveskikt (C3N4) reducerar koldioxid (CO) 2 ) till kolmonoxid (CO) i närvaro av synligt ljus (röd vågig pil). Om kobolt var bundet med syre för att bilda en koboltoxid (CoOx), reaktionen skulle inte fortsätta. Kredit:Brookhaven National Laboratory
Ett team av forskare har upptäckt en enda plats, synligt ljus-aktiverad katalysator som omvandlar koldioxid (CO 2 ) till "byggsten"-molekyler som kan användas för att skapa användbara kemikalier. Upptäckten öppnar möjligheten att använda solljus för att omvandla en växthusgas till kolvätebränslen.
Forskarna använde National Synchrotron Light Source II, en användaranläggning för US Department of Energy (DOE) Office of Science vid Brookhaven National Laboratory, för att avslöja detaljer om den effektiva reaktionen, som använde en enda jon av kobolt för att hjälpa till att sänka energibarriären för att bryta ner CO 2 . Teamet beskriver denna enstaka katalysator i en tidning som just publicerats i Journal of the American Chemical Society .
Konvertera CO 2 i enklare delar – kolmonoxid (CO) och syre – har värdefulla tillämpningar i den verkliga världen. "Genom att bryta CO 2 , vi kan slå två flugor i en smäll – ta bort CO2 från atmosfären och göra byggstenar för att göra bränsle, sa Anatoly Frenkel, en kemist med en gemensam utnämning vid Brookhaven Lab och Stony Brook University. Frenkel ledde försöket att förstå katalysatorns aktivitet, som gjordes av Gonghu Li, en fysikalisk kemist vid University of New Hampshire.
"Vi har nu bevis på att vi har gjort en katalysator på en plats. Inget tidigare arbete har rapporterat solenergi 2 reduktion med en enda jon, sa Frenkel.
Att bryta bindningarna som håller CO 2 tillsammans tar mycket energi och lång tid. Så, Li satte sig för att utveckla en katalysator för att sänka energibarriären och påskynda processen.
"Frågan är, mellan flera möjliga katalysatorer, som är effektiva och praktiska att implementera i industrin?" sa Frenkel.
En nyckelingrediens som krävs för att bryta bindningarna av CO 2 är ett förråd av elektroner. Dessa elektroner kan genereras när ett material som kallas en halvledare aktiveras av energi i form av ljus. Ljuset "sparkar" ut elektroner, så att säga, gör dem tillgängliga för katalysatorn för kemiska reaktioner. Solljus kan vara en naturlig källa till sådant ljus. Men många halvledare kan bara aktiveras av ultraviolett ljus, som utgör mindre än fem procent av solspektrumet.
"Utmaningen är att hitta ett annat halvledarmaterial där energin från naturligt solljus kommer att göra en perfekt match för att sparka ut elektronerna, sa Frenkel.
Forskarna behövde också att halvledaren skulle vara bunden till en katalysator gjord av material som kunde finnas rikligt i naturen, snarare än sällsynt, dyra metaller som platina. Och de ville att katalysatorn skulle vara tillräckligt selektiv för att bara driva reaktionen som omvandlar CO 2 till CO.
"Vi vill inte att elektronerna ska användas för andra reaktioner än att reducera CO 2 , sa Frenkel.
Koboltjoner bundna till grafitkolnitrid (C3N4), en halvledare gjord av kol, kväve, och väteatomer, kryssat i alla rutor för dessa krav.
"Det har funnits ett stort intresse för att använda C3N4 som en metallfri halvledare för att skörda synligt ljus och driva kemiska reaktioner, " sa Li. "Elektroner som genereras av C3N4 under ljusbestrålning har tillräckligt hög energi för att minska CO 2 . Sådana elektroner har ofta inte tillräckligt långa livstider för att de ska kunna resa till halvledarytan för användning i kemiska reaktioner. I vår studie, vi antog en gemensam och effektiv strategi för att bygga upp tillräckligt med energiska elektroner för katalysatorn genom att använda en offerelektrondonator. Denna strategi gjorde det möjligt för oss att fokusera på katalysen för CO 2 minskning. I sista hand, vi vill använda vattenmolekyler som elektrondonator för vår katalys, " han lade till.
Peipei Huang, en postdoktor i Lis labb, tillverkade katalysatorn genom att helt enkelt avsätta koboltjoner på ett C3N4-material tillverkat av kommersiellt tillgänglig urea. Teamet undersökte sedan omfattande den syntetiserade katalysatorn med en mängd olika tekniker i samarbete med Christine Caputo vid University of New Hampshire och Ronald Grimm vid Worcester Polytechnic Institute.
Katalysatorn arbetade i CO 2 minskning under synligt ljus.
"Denna katalysator gjorde vad den var tänkt att göra - bryta ner CO 2 och gör CO med mycket god selektivitet i synligt ljus, ", sa Frenkel. "Men nästa mål var att se varför det fungerade. Om du kan förstå varför det fungerar kan du göra nya och bättre material baserat på dessa principer."
Så Frenkel och Li brainstormade experiment som skulle visa katalysatorns struktur med precision. Strukturella studier skulle ge forskarna information om antalet koboltatomer, deras placering i förhållande till kol- och kväveatomerna, och andra egenskaper som forskarna eventuellt skulle kunna anpassa för att försöka förbättra katalysatorn ytterligare.
De vände sig till Quick X-ray Absorption and Scattering (QAS) strållinjen vid NSLS-II för att använda röntgenabsorptionsspektroskopi. Med hjälp av den ledande strållinjeforskaren Steven Ehrlich, Frenkels elev Jiahao Huang tog data och analyserade spektra.
I denna teknik, röntgenstrålar från NSLS-II absorberas av atomer i provet, som sedan skjuter ut vågor av elektroner. Spektran visar hur dessa elektronvågor interagerar med omgivande atomer, liknar hur krusningar på ytan av en sjö störs när de möter stenar.
"För att kunna göra röntgenabsorptionsspektroskopi (XAS), vi måste ställa in och skanna energin från röntgenstrålen som träffar provet, ", sade Ehrlich. "Varje element kan absorbera röntgenstrålar vid olika energier, kallas absorptionskanter. Vid den nya QAS-strållinjen kan vi skanna energin från röntgenstrålningen över absorptionskantenergin hos olika element, som kobolt i det här fallet. Vi mäter sedan antalet fotoner som absorberas av provet för varje värde på röntgenenergin."
Dessutom, Frenkel förklarade, "varje typ av atom producerar en annan typ av elektronisk krusning, när de upphetsas av röntgenstrålar, eller när den träffas av andra krusningar, så röntgenabsorptionsspektrumet talar om för dig vad de omgivande atomerna är samt hur långt ifrån varandra och hur många det finns."
Analysen visade att katalysatorn bryter ner CO 2 var gjord av enstaka joner av kobolt omgiven på alla sidor av kväveatomer.
"Det fanns inga kobolt-kobolt-par. Så, detta var bevis på att de i själva verket var enstaka atomer av kobolt spridda på ytan, sa Frenkel.
"Denna data begränsar också de möjliga strukturella arrangemangen, som ger information för teoretiker att till fullo utvärdera och förstå reaktionerna, " tillade Frenkel.
Även om vetenskapen som beskrivs i tidningen ännu inte är i praktisk användning, det finns gott om applikationsmöjligheter, sa Frenkel. I framtiden, sådana single-site katalysatorer skulle kunna användas i storskaliga områden med rikligt solljus för att bryta ner överskott av CO 2 i atmosfären, liknande sättet som växter bryter ner CO 2 och återanvända dess byggstenar för att bygga sockerarter i processen för fotosyntes. Men istället för att göra socker, forskare kan använda CO-byggstenarna för att generera syntetiska bränslen eller andra användbara kemikalier.