Rapadocin -molekyl. Kredit:Liu laboratorium
I en strategisk sökning, Johns Hopkins forskare skapade och screenade ett bibliotek med 45, 000 nya föreningar som innehåller kemiska element i allmänt använda immunförsvarssänkande medel, och säga att de hittade en som kan förhindra reperfusionsskada, en vävnadsskadande och vanlig komplikation av operationen, hjärtinfarkt och stroke.
Johns Hopkins -teamet kallade sitt nyupptäckta förening rapadocin och har inlämnat patent på det och dess familj på 45, 000 kemiska kusiner. Det har också licensierat läkemedlet till Baltimore-baserade bioteknikföretag Rapafusyn Pharmaceuticals, som grundades av studiens ledare, Jun O. Liu, Ph.D., professor i farmakologi och onkologi vid Johns Hopkins University School of Medicine. Forskarna varnar för att kommersialisering eller klinisk användning av läkemedlet måste vänta på betydande ytterligare säkerhets- och nyttostudier hos människor.
En rapport om metoden som används för att skapa och identifiera rapadocin, liksom laboratorietester av det hos möss med reperfusionsskador i njurarna dök upp den 10 december Naturkemi .
"Reperfusionsskador är en vanlig komplikation efter operationen, särskilt hos äldre, "säger Liu som övervakar ett bibliotek med tusentals av världens någonsin använda mediciner som bankas på Johns Hopkins Drug Library.
Skadan uppstår när, efter operationen, läkare släpper klämmor på blodkärl och en ökning av syresatt blod rinner tillbaka till vävnader som tillfälligt svälts av det. Blodvågen kan chocka vävnaderna som orsakar inflammation och organskador. Tillståndet kan också hända när tilltäppta artärer öppnas efter hjärtinfarkt och stroke. För närvarande, det finns ett antal läkemedel som studeras för att behandla reperfusionsskador, och några behandlingar, såsom blodförtunnande medel och antiinflammatoriska läkemedel, kan vara milt effektivt för vissa typer av tillståndet.
För att hitta det nya läkemedlet, Liu, som meddirigerar Cancer Chemical and Structural Biology Program på Johns Hopkins Kimmel Cancer Center, återkallade hans postdoktorala utbildningsår för att studera hur ett läkemedel som kallas rapamycin fungerar. Väsentligen, det undertrycker immunsystemet och ordineras ofta till njurtransplanterade patienter för att förhindra avstötning av deras nya organ.
"Jag har alltid trott att rapamycin hade intressanta egenskaper, "säger Liu." Det är väldigt stabilt och celler kan absorbera stora mängder av det, särskilt på grund av dess kemiska struktur. "
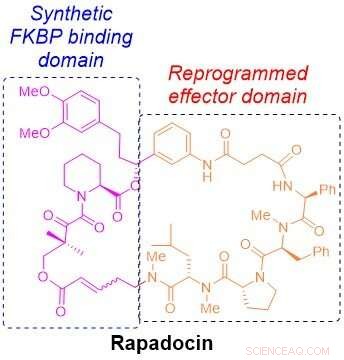
Molekylstrukturen för rapadocin. Kredit:Liu laboratorium
Kemiskt, rapamycin och ett annat immunsuppressivt läkemedel, kallas FK506, innehåller en unik ställning som utgör nästan hälften av en ring. Den där halvan av ringen, kallad FKBP-bindande domän, är nästan identisk mellan de två drogerna, och den andra halvan, den så kallade effektordomänen, är unik för var och en av dem. Läkemedlets FKBP-bindande domän ger ett antal fördelar, inklusive stabilitet och större fördelning i hela kroppen. Effektordomänen är det som gör att varje läkemedel riktar sig mot ett annat protein för att undertrycka immunsystemet eller hämma tillväxten av cancerceller.
Inspirerad av de unika kemiska arkitekturerna för rapamycin och FK506, Liu undrade om det var möjligt att bygga liknande ringformade molekyler genom att byta ut effektordomänen för rapamycin och ersätta det med nya byggstenar för att rikta in sig på andra proteiner som är involverade i mänskliga sjukdomar.
Att göra så, Liu och hans team gjorde 45, 000 kombinationer av föreningar med en FKBP-bindande domän och olika effektordomäner. "Vi kunde ha gjort många fler kombinationer, men bara hade en viss mängd resurser att arbeta med, "minns Liu.
Liu och hans team delade den massiva poolen på 45, 000 föreningar till 3, 000 mindre grupper och testade varje grupp för dem som blockerade en kemisk väg i samband med reperfusionsskada.
Den vägen är ett pumpsystem som kallas ekvilibrativ nukleosidtransportör, eller ENT, som transporterar en molekyl som kallas adenosin, en viktig biologisk budbärare, in i cellen. Vävnader som svälts för syre producerar stora mängder adenosin. Adenosin skyddar celler från skador genom att ansluta till receptorer på cellens yta. För att kontrollera hur mycket och hur länge adenosin ansluter till dess receptor, celler kan dämpa aktiviteten av adenosin genom att svälja den in i cellen genom ENT -transportören. "Så målet är att hålla adenosin utanför cellen längre för att behandla reperfusionsskador, säger Liu.
För att hålla adenosin utanför cellen, forskarna letade efter föreningarna som blockerade ENT-aktivitet och höll mest adenosin utanför cellerna för att ha sin vävnadsskyddande effekt så länge som möjligt. En förening steg till toppen av deras experiment, och de kallade det rapadocin.
I laboratoriestudier av 25 möss, forskarna injicerade dem med rapadocin, tog bort en av deras njurar och klämde fast den andra i 45 minuter; 24 timmar senare, de provade sitt blod för nivåer av kreatinin och kväve, som är markörer för reperfusionsskada.
Djuren som fick rapadocin hade en tredjedel mindre kreatinin (0,4 milligram per deciliter jämfört med 0,6 milligram per deciliter i genomsnitt) och mindre än hälften av kvävehalterna (40 milligram per deciliter jämfört med 90 milligram per deciliter i genomsnitt) än kontrollmöss som var fått ett läkemedel för att avbryta effekterna av rapadocin.