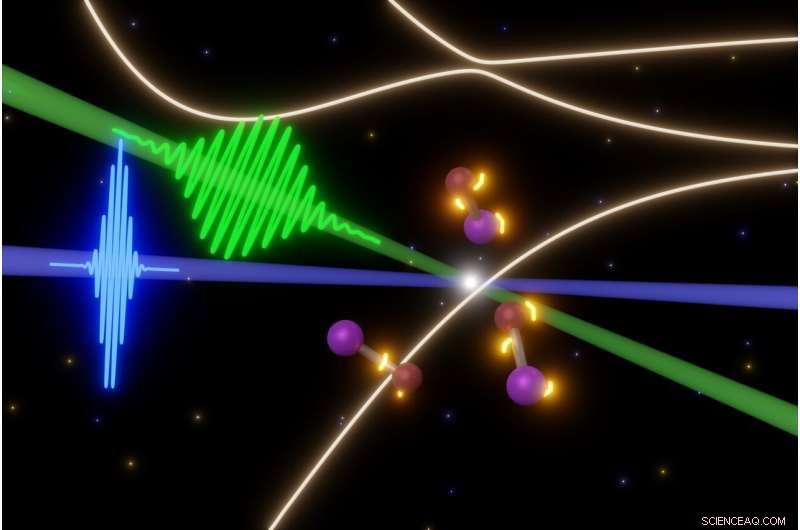
UC Berkeleys forskare undersöker de flyktiga stegen i snabba fotokemiska reaktioner med några av de kortaste laserpulserna som är möjliga idag. I detta fall, en femtosekundspuls av synligt ljus (grönt) utlöser sönderdelningen av jodmonobromidmolekyler (mitten), medan attosecond XUV-laserpulser (blå) tar ögonblicksbilder av molekylerna. Detta gör att de kan göra en film av utvecklingen av elektroniska tillstånd (gula lampor runt molekyler) innan molekylerna blåser isär. Kredit:Yuki Kobayashi, UC Berkeley
Under ljusa sommardagar, solljuset runt omkring oss bryter dåligt genom att bryta band. Kemiska bindningar.
Ultraviolett ljus krossar kopplingarna mellan atomer i våra hudcellers DNA, potentiellt orsaka cancer. UV-ljus bryter också syrebindningar, så småningom skapa ozon, och klyver väte från andra molekyler för att lämna efter sig fria radikaler som kan skada vävnad.
University of California, Berkeley, kemister som använder några av de kortaste tillgängliga laserpulserna – en kvintiljondels sekund – har nu kunnat lösa den steg-för-steg-process som leder till att en kemisk bindning exploderar, i huvudsak göra en film av händelsen. De kan följa elektroner som obeslutsamt studsar runt i olika tillstånd i molekylen innan bindningen bryts, och atomerna går skilda vägar.
Tekniken, rapporterade förra veckan i tidningen Vetenskap , kommer att hjälpa kemister att förstå och potentiellt manipulera kemiska reaktioner stimulerade av ljus, så kallade fotokemiska reaktioner. Kemister och biologer, särskilt, är intresserade av att förstå hur stora molekyler lyckas absorbera ljusenergi utan att bryta några bindningar, som händer när molekyler i ögat absorberar ljus, ger oss visioner, eller molekyler i växter absorberar ljus för fotosyntes.
"Tänk på en molekyl, rhodopsin, i ögat, " sa första författaren Yuki Kobayashi, en doktorand vid UC Berkeley. "När ljus träffar näthinnan, rhodopsin absorberar det synliga ljuset, och vi kan se saker eftersom rhodopsins bindnings konformation förändras."
Faktiskt, när ljusenergin absorberas, en bindning i rhodopsin twists, istället för raster, utlöser andra reaktioner som resulterar i uppfattningen av ljus. Tekniken Kobayashi och hans UC Berkeley-kollegor, professorerna Stephen Leone och Daniel Neumark, utvecklat skulle kunna användas för att studera i detalj hur denna ljusabsorption leder till vridning efter att molekylen passerar genom ett exciterat tillstånd som kallas en undvikad korsning eller konisk skärning.
För att förhindra att en bindning i DNA bryts, "du vill omdirigera energin från dissociation till att bara vara vibrationsvarm. För rhodopsin, du vill omdirigera energin från att vibrera till en cis-trans-isomerisering, en tvist, " sade Kobayashi. "Dessa omdirigeringar av kemiska reaktioner sker allestädes runt omkring oss, men vi har inte sett det verkliga ögonblicket för dem tidigare."

Yuki Kobayashi gör justeringar av ett experiment i källaren i Hildebrand Hall. Han och forskare i Stephen Leones och Daniel Neumarks labb riktar in sig på molekyler i en vakuumkammare med både femtosekund- och attosekundslasrar för att ta reda på hur molekyler absorberar ljus. Kredit:UC Berkeley foto med tillstånd av Robert Sanders
Snabba laserpulser
Attosecond-lasrar – en attosecond är en miljarddels miljarddels sekund – har funnits i ungefär ett decennium och används av forskare för att undersöka mycket snabba reaktioner. Eftersom de flesta kemiska reaktioner sker snabbt, dessa snabbpulslasrar är nyckeln till att "se" hur elektronerna som bildar den kemiska bindningen beter sig när bindningen bryts och/eller reformeras.
Leone, professor i kemi och fysik, är en experimentalist som också använder teoretiska verktyg och är en pionjär när det gäller att använda attosecond-lasrar för att undersöka kemiska reaktioner. Han har sex av dessa röntgen och extrem ultraviolett (tillsammans, XUV)-lasrar i hans UC Berkeley-laboratorium.
Att arbeta med en av de enklaste molekylerna, jodmonobromid (IBr) – som är en jodatom kopplad till en bromatom – UC Berkeley-teamet träffade molekylerna med en 8 femtosekunders puls av synligt ljus för att excitera en av deras yttersta elektroner, sedan sonderade dem med attosecond laserpulser.
Att pulsera attosecond XUV-lasern med tidsintervall på 1,5 femtosekund (en femtosekund är 1, 000 attosekunder), ungefär som att använda ett blixtljus, forskarna kunde upptäcka stegen som leder till att molekylerna splittras. Den högenergiska XUV-lasern kunde utforska de exciterade energitillstånden i förhållande till molekylens inre elektroner, som normalt inte deltar i kemiska reaktioner.
"Du gör typ en film av elektronens vägar när den närmar sig korsningen och sannolikheten att den går längs en väg eller längs en annan, " sa Leone. "De här verktygen vi utvecklar låter dig titta på fasta ämnen, gaser och vätskor, men du behöver de kortare tidsskalorna (som tillhandahålls av en attosecond-laser). Annat, du ser bara början och slutet, och du vet inte vad mer som hände däremellan."
Experimentet visade tydligt att de yttre elektronerna i Ibr, en gång upphetsad, plötsligt se en mängd olika stater eller platser de kan vara och utforska många av dem innan du bestämmer dig för vilken väg du ska ta. I denna enkla molekyl, dock, alla vägar leder till att elektronen sätter sig på antingen jod eller brom och de två atomerna flyger isär.
I större molekyler, som teamet snart hoppas kunna utforska, exciterade elektroner skulle ha fler valmöjligheter, vissa där energin går i en twist, som med rhodopsin, eller till molekylär vibration utan att molekylerna går sönder.
"Inom biologi, det visar sig att evolutionen har valt ut saker som är extremt effektiva för att absorbera energin och inte bryta ett band, " sa Leone. "När något går fel i din kemi är när du ser sjukdomar dyka upp."