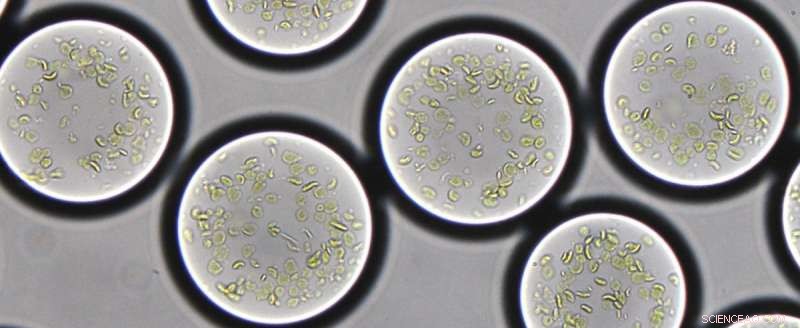
Växttylakoider är inkapslade i mikrodroppar på cirka 90 mikrometer i diameter. Utrustad med en uppsättning enzymer, de halvsyntetiska kloroplasterna fixerar koldioxid med hjälp av solenergi, efter naturens exempel. Kredit:Max Planck Institute for terrestrial Microbiology/Erb
Under miljarder år, mikroorganismer och växter utvecklade den anmärkningsvärda process vi känner som fotosyntes. Fotosyntes omvandlar solenergi till kemisk energi, på så sätt förse allt liv på jorden med mat och syre. Cellfacken som rymmer molekylära maskiner, kloroplasterna, är förmodligen de viktigaste naturliga motorerna på jorden. Många forskare anser att artificiellt återuppbygga och kontrollera fotosyntesprocessen är "vår tids Apollo-projekt." Det skulle innebära förmågan att producera ren energi – rent bränsle, rena kolföreningar som antibiotika, och andra produkter helt enkelt från ljus och koldioxid.
Men hur man bygger ett levande, fotosyntetisk cell från grunden? Nyckeln till att efterlikna processerna i en levande cell är att få dess komponenter att samarbeta vid rätt tid och plats. På Max Planck Society, detta ambitiösa mål eftersträvas i ett tvärvetenskapligt multilabbinitiativ, MaxSynBio -nätverket. Nu har Marburg-forskargruppen under ledning av regissören Tobias Erb framgångsrikt skapat en plattform för automatiserad konstruktion av cellstora fotosyntetiskt aktiva fack, "konstgjorda kloroplaster, " som kan fånga upp och omvandla växthusgasen koldioxid med ljus.
Mikrofluidik möter syntetisk biologi
Max Planck -forskarna använde sig av två senaste tekniska utvecklingar:den första syntetiska biologin för design och konstruktion av nya biologiska system, såsom reaktionsnätverk för avskiljning och omvandling av koldioxid, och andra mikrofluidik, för montering av mjuka material, såsom cellstora droppar.
"Vi behövde först en energimodul som skulle tillåta oss att driva kemiska reaktioner på ett hållbart sätt. Inom fotosyntes, kloroplastmembran ger energin för koldioxidfixering, och vi planerade att utnyttja denna förmåga ", Tobias Erb förklarar.
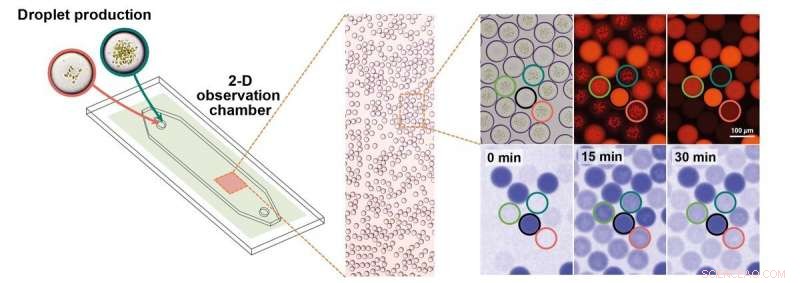
Mikrodroppproduktion och realtidsobservation på en mikrofluidisk plattform. Mikro-droppar samlas i en kammare där deras aktivitet kan mikroskopiskt övervakas i realtid, inklusive kvantifiering av den enzymatiska aktiviteten genom att mäta NADPH-fluorescens. Med hjälp av det ljusa fältet lokaliseras dropparna och de fotosyntetiskt aktiva membranen kan ses. Dessa membran är fluorescerande när de exciteras. Dropppopulationerna särskiljs med hjälp av ett kodande färgämne, vilket är observerbart när dropparna exciteras av en specifik våglängd (550 nm). NADPH-produktionen av dropparna observeras med NADPH-fluorescens (med hjälp av, 365 nm). Kredit:Planck Institute for terrestrial Microbiology/Erb
Fotosyntesapparaten isolerad från spenatväxten visade sig vara tillräckligt robust för att kunna användas för att driva enstaka reaktioner och mer komplexa reaktionsnätverk med ljus. För den mörka reaktionen, forskarna använde sin egen artificiella metaboliska modul, CETCH-cykeln. Den består av 18 biokatalysatorer som omvandlar koldioxid mer effektivt än kolmetabolismen som naturligt förekommer i växter. Efter flera optimeringsrundor, teamet lyckades med ljusstyrd fixering av växthusgasen CO 2 in vitro.
Den andra utmaningen var monteringen av systemet i ett definierat fack i mikroskala. Med tanke på framtida ansökningar, det ska också vara enkelt att automatisera produktionen. I samarbete med Jean-Christophe Barets laboratorium vid Centre de Recherché Paul Pascal (CRPP) i Frankrike, forskare utvecklade en plattform för att kapsla in de semisyntetiska membranen i cellliknande droppar.
Mer effektiv än naturens fotosyntes
Den resulterande mikrofluidiska plattformen kan producera tusentals standardiserade droppar som kan utrustas individuellt enligt önskad metabolisk förmåga. "Vi kan producera tusentals identiskt utrustade droppar eller så kan vi ge specifika egenskaper till enskilda droppar, sa Tarryn Miller, huvudförfattare till studien. "Dessa kan styras i tid och rum med ljus."
I motsats till traditionell genteknik för levande organismer, bottom-up-metoden erbjuder avgörande fördelar:Den fokuserar på minimal design, och det är inte nödvändigtvis bundet till gränserna för naturlig biologi. "Plattformen tillåter oss att realisera nya lösningar som naturen inte har utforskat under evolutionen, " förklarar Tobias Erb. Enligt hans åsikt, resultaten har stor potential för framtiden. I deras publicering i tidningen Vetenskap , författarna kunde visa att att utrusta den "konstgjorda kloroplasten" med de nya enzymerna och reaktionerna resulterade i en bindningshastighet för koldioxid som är 100 gånger snabbare än tidigare syntetisk-biologiska tillvägagångssätt. "I längden, livslika system kan tillämpas på praktiskt taget alla tekniska områden, inklusive materialvetenskap, bioteknik och medicin - vi är bara i början av denna spännande utveckling. "Dessutom, resultaten är ytterligare ett steg mot att övervinna en av framtidens största utmaningar:de ständigt ökande koncentrationerna av atmosfärisk koldioxid.