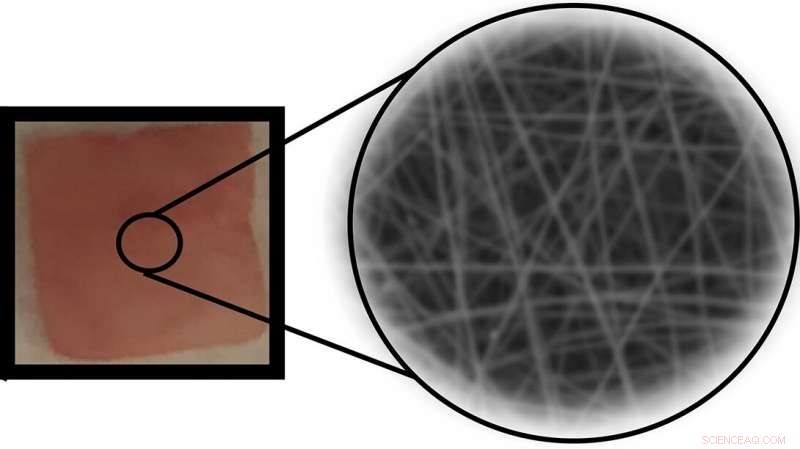
En implanterbar piezoelektrisk polymer nanofiberenhet som frigör kontrollerade mängder av ett läkemedel under mekanisk kraft. Upphovsman:Jin Nam/UCR
Ett membran tillverkat av trådar av en polymer som vanligtvis används i vaskulära suturer kan laddas med terapeutiska läkemedel och implanteras i kroppen, där mekaniska krafter aktiverar polymerens elektriska potential och långsamt släpper ut läkemedlen.
Det nya systemet, utvecklad av en grupp ledd av bioingenjörer vid UC Riverside och publicerad i ACS Applied Bio Materials , övervinner de största begränsningarna av konventionell läkemedelsadministrering och vissa metoder för kontrollerad frisättning, och skulle kunna förbättra behandlingen av cancer och andra kroniska sjukdomar.
Nackdelarna med konventionell läkemedelsadministrering inkluderar upprepad administrering, ospecifik biodistribution i kroppens system, den långsiktiga ohållbarheten hos läkemedelsmolekyler, och hög cytotoxicitet, utgör en utmaning för effektiv behandling av kroniska sjukdomar som kräver varierande läkemedelsdoser över tid för optimal terapeutisk effekt. De flesta metoder för kontrollerad frisättning kapslar in läkemedelspartiklar i biologiskt nedbrytbara, bubbelliknande behållare som löses upp med tiden för att frigöra läkemedlet, vilket gör det svårt att leverera droger enligt ett schema. Andra involverar en batteridriven enhet som inte är biokompatibel.
Jin Nam, docent i bioteknik vid UC Riversides Marlan och Rosemary Bourns College of Engineering, driver ett labb som arbetar med biokompatibla polymerer för att bygga ramverk som kallas byggnadsställningar som hjälper stamceller att reparera vävnader och organ. En av dessa polymerer, poly(vinylidenfluorid-trifluoreten), eller P(VDF-TrFE), kan producera en elektrisk laddning under mekanisk påfrestning. Nam insåg denna fastighet, känd som piezoelektricitet, gjorde polymeren till en potentiellt livskraftig kandidat för ett läkemedelsfrisättningssystem.
Hans team använde en teknik som kallas elektrospinning för att producera P(VDF-TrFE) nanofibrer skiktade i en tunn matta. Strukturering av materialet i nanoskala genom elektrospinning optimerade känsligheten hos de resulterande nanofibrerna så att läkemedelsleveranssystemet skulle svara på fysiologiskt säkra kraftstorlekar samtidigt som det förblir okänsligt för dagliga aktiviteter. Nanofibrernas stora yta gjorde att de kunde adsorbera en relativt stor mängd läkemedelsmolekyler.
Efter att ha bäddat in filmen i en hydrogel som efterliknar levande vävnad, en serie tester med terapeutiska stötvågor genererade tillräckligt med elektrisk laddning för att frigöra en elektrostatiskt fäst modellläkemedelsmolekyl i den omgivande gelen. Forskarna kunde justera mängden läkemedelsfrisättning genom att variera det applicerade trycket och varaktigheten.
"Detta piezoelektriska nanofiberbaserade läkemedelsleveranssystem möjliggör lokal leverans av läkemedelsmolekyler på begäran, som skulle vara användbar för sjukdomar eller tillstånd som kräver långvarig, upprepad läkemedelsadministration, såsom cancerbehandlingar, ", sade Nam. "Det stora förhållandet mellan yta och volym av nanofibrös struktur möjliggör en större läkemedelsbelastning, vilket leder till en enda injektion eller implantation som varar längre än konventionell läkemedelsleverans. "
Jämfört med traditionella läkemedelstillförselsystem baserade på nedbrytning eller diffusionsfrisättning som vanligtvis visar en initial burstfrisättning följt av olika frisättningshastigheter, den linjära profilen för läkemedelsfrisättning från det piezoelektriska systemet möjliggör exakt administrering av läkemedelsmolekyler oavsett implantationstiden. Upprepade läkemedelsfrisättningstester på begäran visade en liknande mängd läkemedelsfrisättning per aktivering, bekräftar den robusta kontrollen av frisättningshastigheten.
Känsligheten hos läkemedelsfrisättningskinetiken kan ställas in genom att kontrollera nanofiberstorleken till ett intervall som aktiveras av terapeutiska stötvågor, används ofta för behandling av muskuloskeletal smärta med en handhållen enhet. Mindre, känsligare nanofiberstorlekar kan användas för implantation i djupa vävnader, såsom nära ett ben under musklerna, medan mindre känsliga större nanofibrer kan användas i subkutana applikationer för att undvika falsk aktivering vid oavsiktlig påverkan.