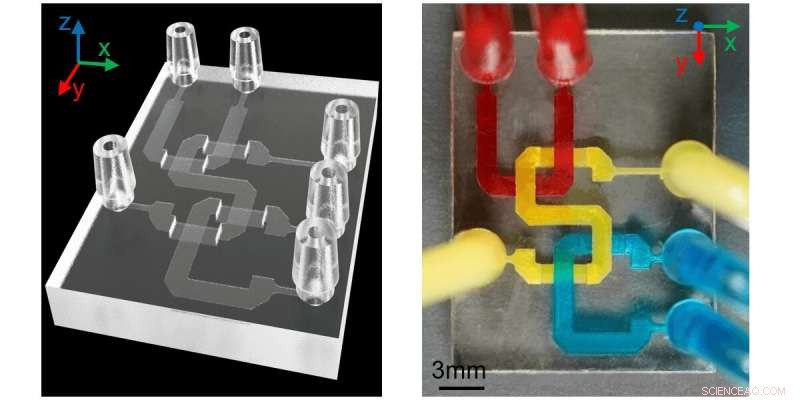
Ett exempel på ett mikrofluidchip skapat av forskargruppen. Kredit:Yang Xu
Mikrofluidiska enheter är kompakta testverktyg som består av små kanaler snidade på ett chip, som gör att biomedicinska forskare kan testa egenskaperna hos vätskor, partiklar och celler i mikroskala. De är avgörande för läkemedelsutveckling, diagnostiska tester och medicinsk forskning inom områden som cancer, diabetes och nu covid-19. Produktionen av dessa enheter är dock mycket arbetskrävande, med små kanaler och brunnar som ofta behöver etsas manuellt eller gjutas till ett transparent hartschip för testning. Medan 3D-utskrift har erbjudit många fördelar för tillverkning av biomedicinska enheter, var dess tekniker tidigare inte tillräckligt känsliga för att bygga lager med den minsta detalj som krävs för mikrofluidiska enheter. Tills nu.
Forskare vid USC Viterbi School of Engineering har nu utvecklat en mycket specialiserad 3D-utskriftsteknik som gör att mikrofluidkanaler kan tillverkas på chips i en exakt mikroskala som inte tidigare uppnåtts. Forskningen, ledd av Daniel J. Epstein Institutionen för industri- och systemteknik Ph.D. examen Yang Xu och professor i rymd- och maskinteknik samt industri- och systemteknik Yong Chen, i samarbete med professor i kemiteknik och materialvetenskap Noah Malmstadt och professor Huachao Mao vid Purdue University, publicerades i Nature Communications .
Forskargruppen använde en typ av 3D-utskriftsteknik känd som vat-fotopolymerisation, som utnyttjar ljus för att kontrollera omvandlingen av flytande hartsmaterial till dess fasta sluttillstånd.
"Efter ljusprojektion kan vi i princip bestämma var vi ska bygga delarna (av chipet), och eftersom vi använder ljus kan upplösningen vara ganska hög inom ett lager. Däremot är upplösningen mycket sämre mellan lagren, vilket är en kritisk utmaning i att bygga mikroskaliga kanaler," sa Chen.
"Det här är första gången vi har kunnat skriva ut något där kanalhöjden är på 10 mikron-nivån; och vi kan kontrollera det riktigt exakt, till ett fel på plus eller minus en mikron. Detta är något som aldrig har varit gjort tidigare, så det här är ett genombrott i 3D-utskrift av små kanaler", sa han.
Karfotopolymerisation använder sig av ett kar fyllt med flytande fotopolymerharts, ur vilket ett tryckt föremål konstrueras lager för lager. Ultraviolett ljus blinkar sedan på föremålet, härdar och härdar hartset på varje lagernivå. När detta händer flyttar en byggplattform det utskrivna objektet uppåt eller nedåt så att ytterligare lager kan byggas på det.
Men när det kommer till mikrofluidiska enheter har karfotopolymerisering vissa nackdelar i skapandet av de små brunnar och kanaler som krävs på chipet. UV-ljuskällan tränger ofta djupt in i kvarvarande flytande harts, härdande och stelnar material inom väggarna i enhetens kanaler, vilket skulle täppa till den färdiga enheten.
"När du projicerar ljuset vill du helst bara härda ett lager av kanalväggen och lämna det flytande hartset inuti kanalen orört, men det är svårt att kontrollera härdningsdjupet, eftersom vi försöker rikta in oss på något som bara är en 10 mikron gap," sa Chen.
Han sa att nuvarande kommersiella processer endast tillåter skapandet av en kanalhöjd på 100 mikron nivå med dålig noggrannhetskontroll, på grund av det faktum att ljuset penetrerar ett härdat lager för djupt, såvida du inte använder en ogenomskinlig harts som t tillåta så mycket ljus penetration.
"Men med en mikrofluidkanal vill du vanligtvis observera något under mikroskop, och om det är ogenomskinligt kan du inte se materialet inuti, så vi måste använda ett genomskinligt harts," sa Chen.
För att exakt skapa kanaler i klar harts på en mikroskalanivå som är lämplig för mikrofluidiska enheter, utvecklade teamet en unik hjälpplattform som rör sig mellan ljuskällan och den tryckta enheten, vilket blockerar ljuset från att stelna vätskan inom väggarna i en kanal, så att kanaltaket sedan kan läggas separat till toppen av enheten. Det resterande hartset som finns kvar i kanalen skulle fortfarande vara i flytande tillstånd och kan sedan spolas ut efter tryckprocessen för att bilda kanalutrymmet.
Mikrofluidiska enheter har allt viktigare tillämpningar inom medicinsk forskning, läkemedelsutveckling och diagnostik.
"Det finns så många tillämpningar för mikrofluidkanaler. Du kan flöda ett blodprov genom kanalen, blanda det med andra kemikalier så att du till exempel kan upptäcka om du har covid eller höga blodsockernivåer," sa Chen.
Han sa att den nya 3D-utskriftsplattformen, med sina mikroskaliga kanaler, möjliggjorde andra applikationer, såsom partikelsortering. En partikelsorterare är en typ av mikrofluidchip som använder sig av kammare av olika storlek som kan separera partiklar av olika storlek. Detta skulle kunna erbjuda betydande fördelar för upptäckt och forskning om cancer.
"Tumörceller är något större än normala celler, som är runt 20 mikron. Tumörceller kan vara över 100 mikron," sade Chen. "Just nu använder vi biopsier för att kontrollera om det finns cancerceller; skär av organ eller vävnad från en patient för att avslöja en blandning av friska celler och tumörceller. Istället kan vi använda enkla mikrofluidiska enheter för att flöda (provet) genom kanaler med exakt tryckta höjder för att separera celler i olika storlekar så att vi inte tillåter de friska cellerna att störa vår upptäckt."
Chen sa att forskargruppen nu var i färd med att lämna in en patentansökan för den nya 3D-utskriftsmetoden och att de söker samarbete för att kommersialisera tillverkningstekniken för medicinska testanordningar. + Utforska vidare