Helicener är organiska molekyler som vunnit stor popularitet på grund av deras unika spiralformade π-konjugerade molekylstruktur, där bensenringarna är orto-fuserade, vilket resulterar i utmärkta kirotiska egenskaper som cirkulärt polariserad luminescens (CPL). Möjligheten att fungera som en CPL-sändare gör helicener idealiska för ett brett utbud av nästa generations optoelektroniska applikationer, såsom optiska informationskommunikationssystem och 3D-displaysystem.
Högre ordningens 3D π-förlängda karbohelicener - en typ av helicin - förväntas ge utmärkta CPL-sändare på grund av deras höga cirkulära polarisation, ljusstyrka och stabilitet. Dessa exceptionella egenskaper hos karbohelicener kan dock inte utnyttjas fullständigt på grund av deras mycket förvrängda struktur, vilket hindrar både deras syntes och enantiokontroll - kontrollen av den enantiomera sammansättningen eller mängden vänsterhänta eller högerhänta versioner av en molekyl som produceras i en molekyl. reaktion.
För att säkerställa att hela utbudet av egenskaper hos karbohelicener är tillgängligt för tillämpning, tog ett team av forskare under ledning av professor Ken Tanaka från Tokyo Institute of Technology nyligen fram en ny strategi som underlättade den enantioselektiva syntesen av 3D π-förlängd karbo[11] och [ 13]helicener för CPL-sändare och deras enantioselektiva syntes med minskade distorsioner.
I sin studie från 2022 rapporterade teamet den Rh-katalyserade enantioselektiva syntesen av en hexabensokoronen-baserad karbo[6]helicen via intramolekylär [2+2+2] cykloaddition av en triyn följt av en π-förlängning av Scholl-reaktionen.
"Vi observerade att även om den här processen övervann nackdelarna med konventionella syntesprocesser, såsom oönskade omarrangeringsreaktioner och låg regioselektivitet, var den molekylära distorsionen tyvärr fortfarande ganska hög. Genom att lära av dessa observationer utformade vi en strategi för att övervinna de höga distorsionerna och förbättra CPL-emissionen", förklarar Tanaka.
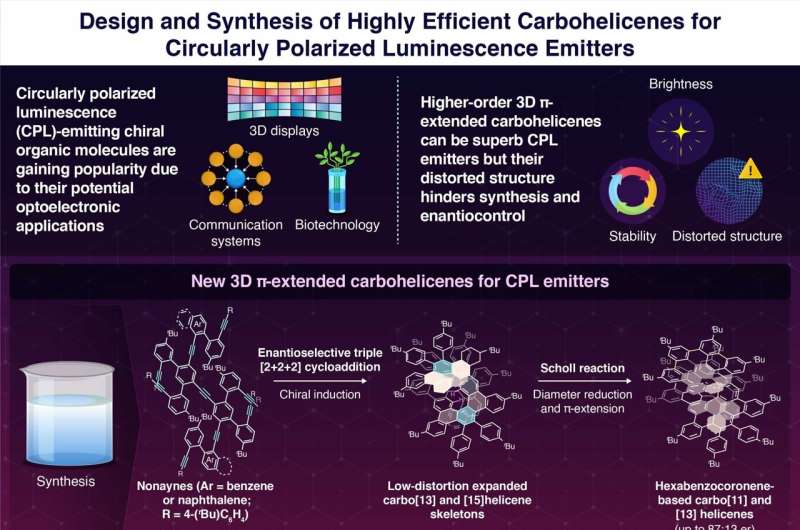
För denna Natursyntes studien genomförde teamet enantioselektiv syntes av karbo[11] och [13]helicener med ett enantiomert förhållande på 87:13 och övervann höga distorsioner genom att kombinera den enantioselektiva syntesen av karbo[5] och [6]helicener med trippel [2+ 2+2] cykloaddition, som följdes av π-förlängningen/helixdiameterreduktionen genom Scholl-reaktionen.
Den stora fördelen med den stegvisa konstruktionsprocessen av en helt orto-fuserad 3D π-förlängd karbohelicen-ryggrad är att den övervinner nackdelarna som är förknippade med både enantioselektiv [2+2+2] cykloaddition och Scholl-reaktion.
För att utforska materialegenskaperna hos det syntetiserade materialet genomförde teamet röntgenkristallografiska analyser, som avslöjade att de 3D π-förlängda karbo[11] och [13]helicenerna med stela molekylära ryggrader var konglomerat som gynnade preferentiell kristallisering. Dessutom var de vanligaste molekylära krafterna bland karbohelicenskikten van der Waals-interaktioner.
Efter att testa de fotofysiska egenskaperna hos de syntetiserade π-förlängda karbo[11]- och [13]-helicenerna upptäckte teamet att CPL-ljusstyrkan nådde maximalt 513 M –1 cm –1 , ett av de högsta värdena bland helicenderivat som rapporterats i litteraturen.
Sammantaget kan detta nya tillvägagångssätt för molekylär design och enantioselektiv syntes utgöra en solid grund för vidare forskning och utveckling av högpresterande karbohelicener för framtidens CPL-utsändare.
"Vår studie har öppnat nya vägar för produktion och användning av kirala organiska molekylbaserade CPL-sändare, med tillämpningar som sträcker sig från toppmoderna digitala displayer till effektiva kommunikationsnätverk och viktiga biotekniska framsteg", avslutar Tanaka.
Mer information: Futo Morita et al, Design och enantioselektiv syntes av 3D π-förlängda karbohelicener för cirkulärt polariserad luminescens, Nature Synthesis (2024). DOI:10.1038/s44160-024-00527-3
Journalinformation: Natursyntes
Tillhandahålls av Tokyo Institute of Technology