Paklitaxel är världens mest sålda växtbaserade anticancerläkemedel och ett av de mest effektiva anticancerläkemedlen under de senaste 30 åren. Det används i stor utsträckning vid behandling av olika typer av cancer, inklusive bröstcancer, lungcancer och äggstockscancer.
I slutet av 1990-talet och början av 2000-talet översteg den årliga försäljningen av paklitaxel 1,5 miljarder USD och nådde 2,0 miljarder USD 2001, vilket gjorde det till det mest sålda läkemedlet 2001. 2019 var marknaden för paklitaxel och dess derivat cirka 15 miljarder USD, och den förväntas uppgå till 20 miljarder dollar 2025.
Som ett anticancerläkemedel är paklitaxelns molekylära struktur extremt komplex, med starkt oxiderade, komplicerade bryggade ringar och 11 stereocentra, vilket gör det allmänt erkänt som en av de mest utmanande naturliga produkterna att syntetisera kemiskt. Sedan den första totalsyntesen av paklitaxel rapporterades av forskargrupperna Holton och Nicolaou 1994, har mer än 40 forskarlag varit engagerade i den totala syntesen av paklitaxel.
Men även i den kortaste kemiska syntesvägen hittills är det totala utbytet av paklitaxel endast 0,118 %, vilket inte klarar av att möta efterfrågan på industriell produktion. För närvarande använder den industriella produktionen av paklitaxel en semisyntetisk strategi:isolering av prekursorer för paklitaxel (såsom baccatin III) från växtcellkulturer eller Taxus-blad och omvandla dem sedan till paklitaxel genom kemiska metoder. Den semisyntetiska strategin är dock starkt beroende av naturresurser och begränsas av den långsamma tillväxten av Taxus-celler eller löv, och kan därför inte möta den växande efterfrågan på marknaden.
Med den snabba utvecklingen av bioteknik har syntetiska biologistrategier för mikrobiell biosyntes av växtnaturprodukter vuxit fram som ett kraftfullt tillvägagångssätt för att effektivt producera komplexa växtnaturprodukter.
Att uppnå effektiv, miljövänlig och hållbar produktion av paklitaxel genom syntetisk biologi har därför väckt stor uppmärksamhet. För att realisera de novo-syntesen av paklitaxel i ett heterologt system krävs dock att nyckelenzymer som saknas i paklitaxels biosyntesväg identifieras och att en komplett biosyntesväg för paklitaxel etableras.
För att ta itu med den långvariga utmaningen med paklitaxelbiosyntes i Taxus har två forskarlag ledda av prof. Jianbin Yan (Agricultural Genomics Institute i Shenzhen, AGIS) och prof. Xiaoguang Lei (Peking University, PKU), samt andra forskarlag från fem andra olika institutioner inklusive Tsinghua University och UCLA har samarbetat för att framgångsrikt identifiera de saknade enzymerna och uppnå rekonstitutionen av de biosyntetiska enzymerna som leder till baccatin III.
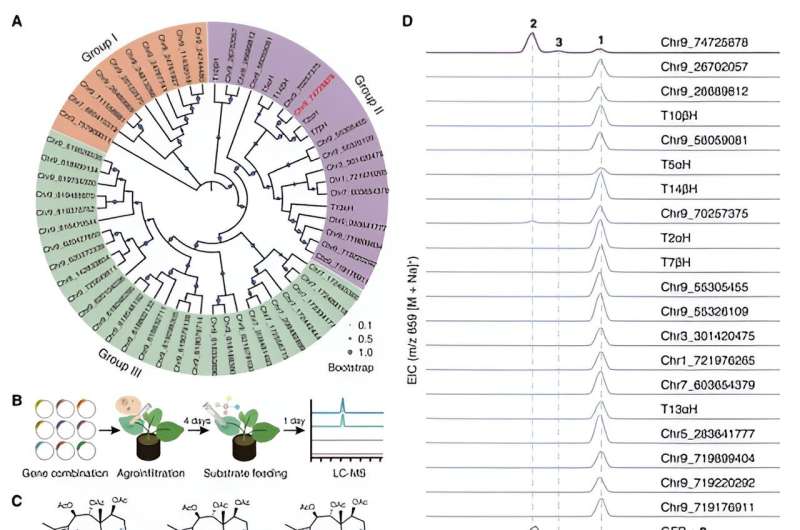
Forskarna använde ett heterologt uttryckssystem för tobak för att utföra aktivitetsscreening av CYP725A-genfamiljen som finns specifikt i Taxus via saminjektion av substrat. De har framgångsrikt identifierat ett biosyntetiskt enzym vid namn Taxane oxetanas (TOT) som katalyserar bildandet av oxetanringen under taxolbiosyntesvägen.
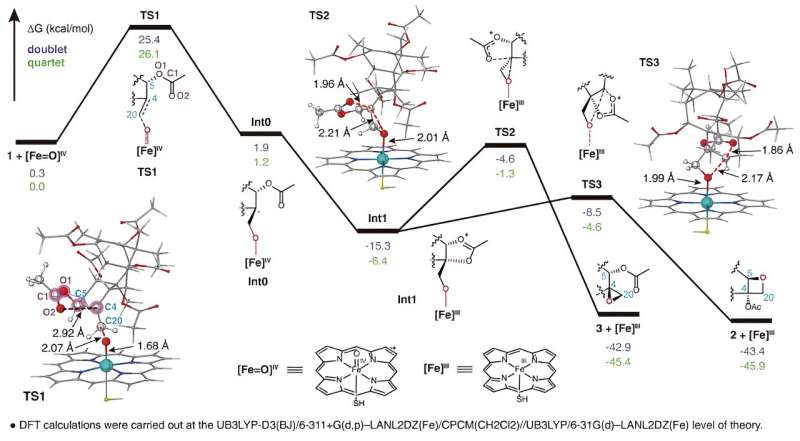
TOT katalyserar bildningen av den unika oxetanringen genom oxidation av C4,20-dubbelbindningen och efterföljande omarrangemang av den intilliggande acetylgruppen vid C5-positionen, som visas i. Denna nya reaktionsmekanism för oxetanringbildning bryter den konventionella förståelsen att oxetanringen bildning i taxolbiosyntesvägen uppnås genom en omlagringsreaktion av motsvarande epoxid.
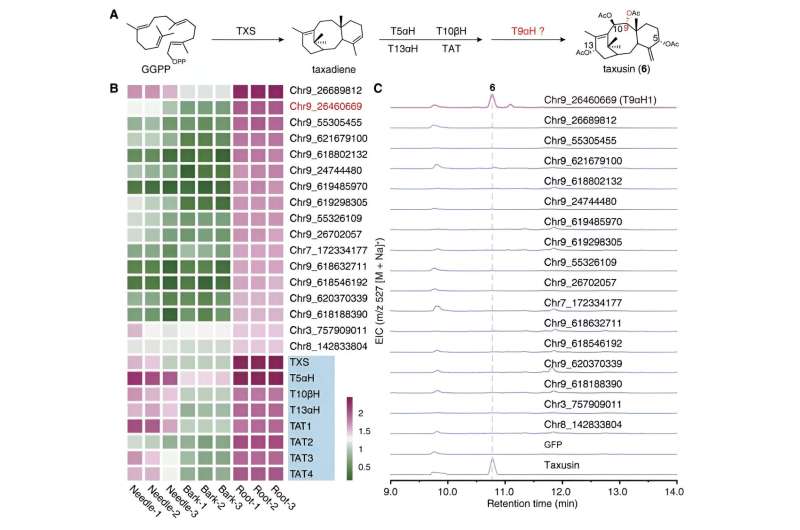
Under tiden, genom att fokusera på den strukturellt enklare föreningen, taxusin, identifierade forskarna 17 kandidatgener som kodar för enzymer som är ansvariga för C9-oxidationen av taxaner med hjälp av samuttrycksanalys och metabolismanalys. Dessa kandidatgener utsattes ytterligare för aktivitetsscreening genom att rekonstruera taxusinbiosyntesvägen i tobak, vilket ledde till upptäckten av enzymet som ansvarar för C9-oxidation i taxaner, som fick namnet Taxane 9α-hydroxylas (T9αH).
Med dessa två nyligen identifierade enzymer TOT och T9αH i händerna försökte forskare uppnå den totala biosyntesen av baccatin III i tobak genom att samuttrycka dem med andra kända biosyntetiska gener av taxol. De upptäckte framgångsrikt produktionen av baccatin III i tobak när TOT och T9αH samuttrycktes med andra 7 kända biosyntetiska gener (TXS, T5αH, T13αH, T2αH, T7βH, TAT och TBT). Dessutom har de visat att dessa nio gener är kärngenerna för baccatin III-biosyntes eftersom varje gen är oumbärlig för biosyntesen av baccatin III i tobak.
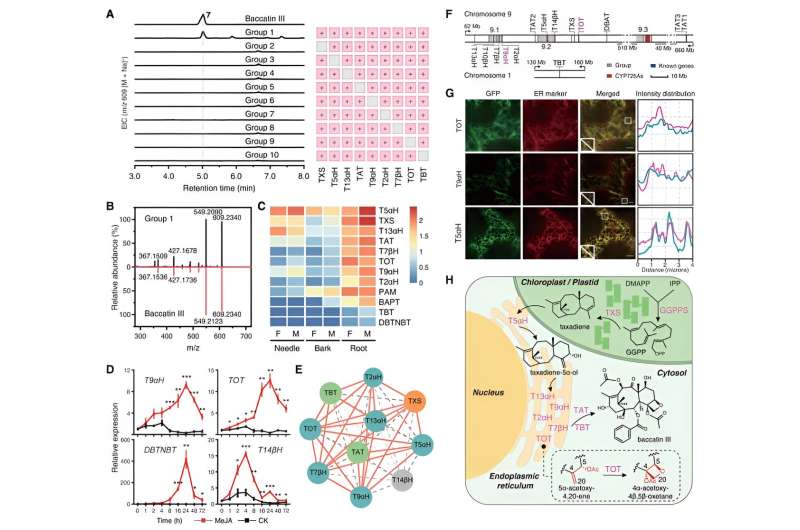
Ytterligare biokemiska studier visade att dessa kärngener uppvisar nära funktionell synergi och samregleras av växthormonet jasmonat, vilket visar liknande induktionsuttrycksmönster och stark uttryckskorrelation. Genom att kombinera subcellulär lokaliseringsanalys och andra experimentella resultat ger forskarna en fullständig översikt över den biosyntetiska processen för baccatin III.
Utgångssubstratet GGPP katalyseras av TXS för att bilda taxadien i kloroplaster. Därefter överförs taxadien till cytoplasman genom kontaktställena av plastid-endoplasmatiskt retikulum och genomgår samordnad katalys av sex membranbundna oxidaser (T2αH, T5αH, T7βH, T9αH, T13αH och TOT) förankrade i den endoplasmatiska och två cytoplasmiska retikulen. transferaser (TAT och TBT), vilket slutligen resulterar i bildningen av baccatin III.
Sammanfattningsvis denna studie, som har publicerats i Science nyligen, kombinerar multipel omics-analys och omfattande funktionell validering för att framgångsrikt identifiera viktiga saknade enzymer i den biosyntetiska vägen för paklitaxel. Den avslöjar en ny mekanism genom vilken växtceller katalyserar bildandet av oxetanringar och upptäcker den kortaste vägen för heterolog biosyntes av paklitaxel.
Genom att samuttrycka 9 kärnenzymer i tobak uppnår forskarna bioproduktionen av paklitaxelprekursorn baccatin III, vilket lägger grunden för storskalig produktion av paklitaxel och ger också teoretisk vägledning för biosyntetiska studier på hundratals andra naturliga taxanprodukter.
Mer information: Bin Jiang et al, Karakterisering och heterolog rekonstitution av Taxus biosyntetiska enzymer som leder till baccatin III, Science (2024). DOI:10.1126/science.adj3484
Journalinformation: Vetenskap
Tillhandahålls av Peking University