Forskare vid TUS har utvecklat en ätbar växtbaserad nanopartikel som kan bli nästa potenta anticancerläkemedel. Kredit:Makiya Nishikawa från Tokyo University of Science
Nanomaterial har revolutionerat världen av cancerterapi, och växtbaserade nanopartiklar har den extra fördelen att de är kostnadseffektiva och lätta att massproducera. Forskare från Tokyo University of Science har nyligen utvecklat nya majs-härledda bionanopartiklar för att rikta cancerceller direkt, via en immunmekanism. Resultaten är uppmuntrande, och tekniken har visat sig vara effektiv vid behandling av tumörbärande laboratoriemöss. Dessutom har inga allvarliga biverkningar rapporterats hos möss hittills.
Nanopartiklar, eller partiklar vars storlek varierar mellan 1 och 100 nanometer, har visat en enorm potential inom många områden av vetenskap och teknik, inklusive terapi. Konventionella, syntetiska nanopartiklar är dock komplicerade och dyra att tillverka. Extracellulära vesiklar (EV), som har dykt upp som ett alternativ till syntetiska nanopartiklar, visar utmaningar för massproduktion.
Ett annat nyligen framväxande alternativ är växtbaserade nanopartiklar (NP), som lätt kan produceras i höga nivåer till relativt lägre kostnader. Liksom elbilar innehåller dessa nanopartikelbaserade system även bioaktiva molekyler, inklusive polyfenoler (som är kända antioxidanter) och mikroRNA, och de kan leverera läkemedel till målorgan i våra kroppar.
Med hjälp av denna kunskap utvecklade forskare från Tokyo University of Science (TUS) nyligen bionanopartiklar med anticanceraktivitet, med majs (majs) som råvara.
Prof. Makiya Nishikawa från Tokyo University of Science, Japan, som ledde forskargruppen i denna strävan, förklarar, "Genom att kontrollera de fysikalisk-kemiska egenskaperna hos nanopartiklar kan vi kontrollera deras farmakokinetik i kroppen; så vi ville utforska nanopartiklarnas ätliga växter. Majs, eller majs, produceras i stora mängder över hela världen i sin ursprungliga form såväl som i sina genetiskt modifierade former. Det är därför vi valde det för vår studie." Resultaten av denna studie publicerades online den 24 november 2021 i Scientific Reports .
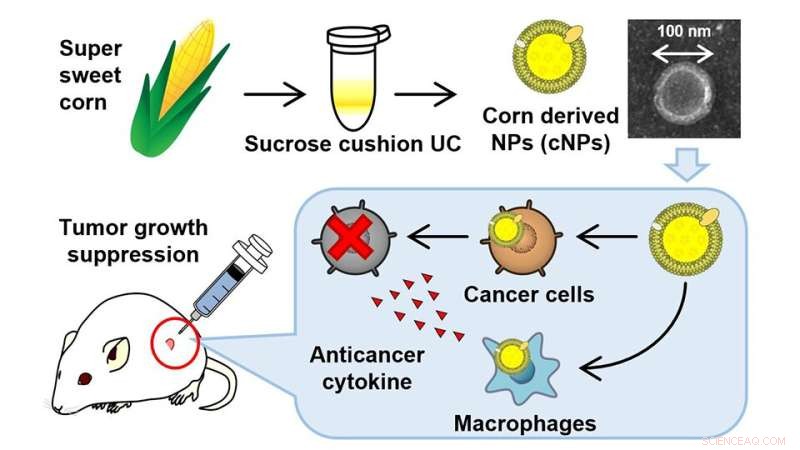
Teamet skapade en homogen blandning av supersötmajs i vatten, centrifugerade sedan denna majsjuice i hög hastighet och filtrerade den sedan genom ett sprutfilter med en porstorlek på 0,45 μm. De filtrerade proverna ultracentrifugerades sedan för att erhålla NP härrörande från majs. De majshärledda NP:erna (cNPs) var cirka 80 nm i diameter. Ganska intressant nog bar dessa cNP också en liten negativ nettoladdning på -17 mV.
Forskargruppen satte sedan upp experiment för att se om dessa cNP togs upp av olika typer av celler. I en serie lovande resultat togs cNP:erna upp av flera typer av celler, inklusive de kliniskt relevanta colon26-tumörcellerna (cancerceller härledda från möss), RAW264.7 makrofagliknande celler och normala NIH3T3-celler. RAW264.7-celler används ofta som in vitro-screening för immunmodulatorer – läkemedel som främst riktar sig mot olika cancervägar.
Resultaten var häpnadsväckande:av de tre typerna av celler hämmade cNP endast signifikant tillväxten av colon26-celler, vilket indikerar deras selektivitet för cancerframkallande cellinjer. Dessutom kunde cNP framgångsrikt inducera frisättningen av tumörnekrosfaktor-a (TNF-α) från RAW264.7-celler. Det är ett väldokumenterat faktum att TNFα i första hand utsöndras av makrofager, naturliga mördarceller och lymfocyter - tre nyckelingredienser i vårt högt utvecklade immunsystem och som hjälper till att skapa ett anticancersvar. "Det starka TNFα-svaret var uppmuntrande och indikerade rollen av cNP vid behandling av olika typer av cancer", förklarar Dr Daisuke Sasaki, första författare till studien och instruktör och forskare vid TUS.
Forskargruppen genomförde sedan en reporteranalys med enzymet "luciferas" (som härrör från eldflugor), som är en känslig reporter för att studera olika biologiska reaktioner. Denna luciferasbaserade analys avslöjade att den potenta kombinationen av cNPs och RAW264.7-celler signifikant undertryckte proliferationen av colon26-celler. Slutligen studerade forskargruppen effekten av cNP på laboratoriemöss som bär subkutana tumörer. Återigen var resultaten häpnadsväckande:att dagligen injicera cNPs i colon26-tumörer undertryckte tumörtillväxten avsevärt, utan att orsaka allvarliga biverkningar eller viktminskning.
"Genom att optimera nanopartikelegenskaper och genom att kombinera dem med anticancerläkemedel hoppas vi kunna ta fram säkra och effektiva läkemedel för olika cancerformer", konstaterar en optimistisk professor Nishikawa.
Dr. Kosuke Kusamori, medförfattare och biträdande professor vid TUS sammanfattar dessa effektfulla resultat, säger:"Dessa cNP:er uppvisar utmärkta antitumöregenskaper, är lätta att utveckla och är ekonomiskt lönsamma. Dessutom uppvisar de inga allvarliga negativa effekter. , åtminstone i möss hittills." + Utforska vidare