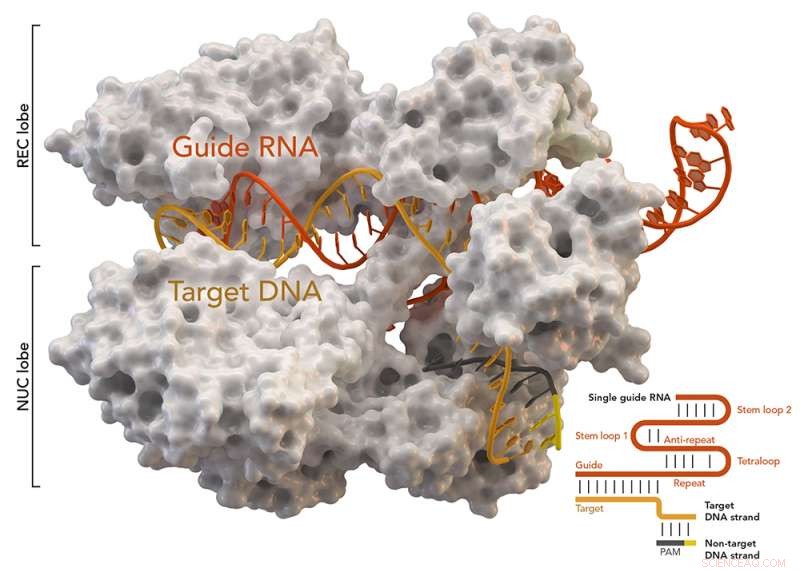
CRISPR-associerat protein Cas9 (vitt) från Staphylococcus aureus baserat på proteindatabas-ID 5AXW. Upphovsman:Thomas Splettstoesser (Wikipedia, CC BY-SA 4.0)
(Phys.org) - Ett team av forskare från University of California och University of Tokyo har hittat ett sätt att använda CRISPR -genredigeringsmetoden som inte är beroende av ett virus för leverans. I deras tidning publicerad i tidningen Natur Biomedicinsk teknik , gruppen beskriver den nya tekniken, hur bra det fungerar och förbättringar som behöver göras för att göra det till ett livskraftigt genredigeringsverktyg.
CRISPR-Cas9 har varit mycket i nyheterna den senaste tiden eftersom det gör det möjligt för forskare att redigera gener direkt-antingen inaktivera oönskade delar eller ersätta dem helt och hållet. Men trots många framgångshistorier, tekniken lider fortfarande av ett stort underskott som hindrar den från att användas som ett riktigt medicinskt verktyg - det gör ibland misstag. Dessa misstag kan orsaka små eller stora problem för en värd beroende på vad som går fel. Tidigare forskning har antytt att majoriteten av misstagen beror på leveransproblem, vilket innebär att en ersättning för virusdelen av tekniken krävs. I denna nya insats, forskarna rapporterar att de har upptäckt just en sådan ersättare, och det fungerade så bra att det kunde reparera en genmutation i en Duchenne muskeldystrofi -musmodell. Teamet har döpt den nya tekniken till CRISPR-Gold, eftersom en guldnanopartikel användes för att leverera genredigeringsmolekylerna istället för ett virus.
Det nya paketet skapades genom att modifiera lite DNA så att det fastnar på en guld -nanopartikel och sedan ett Cas9 -protein och även en RNA -guide. Förpackningen belades sedan med en polymer som fungerade som ett inneslutande hölje - en som också utlöste endocytos (en form av celltransport) och hjälpte molekylerna att undkomma endosomer en gång inne i målcellerna. Molekylerna satte sedan igång - Cas9 skar av mål -DNA -strängen, guiden RNA visade vad som behövde göras och en DNA -sträng placerades där en mutation hade existerat. Resultatet var en gen fri från en mutation som orsakar Duchenne muskeldystrofi.
Det finns fortfarande ett stort problem att övervinna med tekniken, det fungerar dock bara i lokaliserade applikationer. Helst, en massa förpackningar skulle injiceras i blodomloppet vilket möjliggör reparation av alla celltyper, såsom muskler försämrade av en mutant gen.
© 2017 Phys.org