Mikrokontakt utskrift. Upphovsman:Okinawa Institute of Science and Technology Graduate University (OIST)
Medicinområdet är alltid på jakt efter bättre verktyg för diagnostik av sjukdomar – enklare, snabbare, och billigare teknologier för att förbättra patientbehandling och resultat. För närvarande, mikrofluidiska bioanalysanordningar är de föredragna diagnostiska verktygen som gör det möjligt för läkare att mäta koncentrationen av sjukdomsbiomarkörer i en patients biologiska prov, såsom blod. De kan indikera sannolikheten för en sjukdom baserat på en jämförelse av biomarkörkoncentrationen i provet i förhållande till den normala nivån. För att upptäcka denna koncentration, patientens prov passerar över en yta som innehåller immobiliserade bioreceptorer, eller "biomarkörfångande" molekyler som har fästs på denna yta. En forskare kan sedan registrera mängden biomarkörer, avgöra om nivån är normal, och nå en diagnos. Eftersom effektiviteten hos dessa enheter beror på hur intakta och funktionella de bifogade bioreceptorerna är, immobilisering av dessa bioreceptorer utan att orsaka skada har visat sig skrämmande.
Under de senaste två decennierna har mikrokontaktutskrift, som använder en gummistämpel för att immobilisera bioreceptorerna, har etablerats som en robust metod för att skapa en mängd olika analyser med flera applikationer. Men denna metod har också sina brister, speciellt när det används på nanoskala - skalan där proteiner och DNA härskar. I denna skala, de hårda och utarbetade teknikerna som används för närvarande äventyrar enhetens upplösning, antingen genom att deformera stämpeln eller skada bioreceptorerna, vilket ger data något ohanterligt för användning i diagnostik eller andra applikationer. Dock, i en nyligen publicerad artikel i tidskriften Analytiker , forskare vid Okinawa Institute of Science and Technology Graduate University (OIST) beskriver en ny sekvens av utskriftssteg som har åtgärdat dessa problem.
För mikrokontaktutskrift, "du behöver en stämpel, ett bläck, och en yta, och sedan skapar du ditt mönster på din yta. Så enkelt är det, " förklarar Shivani Sathish, OIST doktorand vid Micro/Bio/Nanofluidics Unit, och första författare på tidningen.
Stämpeln är gjord av polydimetylsiloxan, som är ett flexibelt fast ämne som liknar det gummi som används i vardagsfrimärken. Bläcket är en lösning som består av kisel- och oxidhaltiga molekyler som kallas APTES, och ytan är glas. Efter att ha belagt stämpeln med bläcket, stämpeln trycks på glaset, och avlägsnades sedan efter en kort inkubation. Resultatet är ett mönstrat lager av APTES på glaset - ett rutbord med områden med eller utan APTES. Nästa, en mikrofluidanordning, som innehåller en eller flera mikrokanaler konfigurerade för att leda vätska genom angivna vägar, är förseglad över det mönstrade glaset. Till sist, bioreceptorerna är kemiskt kopplade till APTES-regionerna inom mikrofluidkanalerna. Enheten som helhet är ungefär lika stor som ett frimärke.
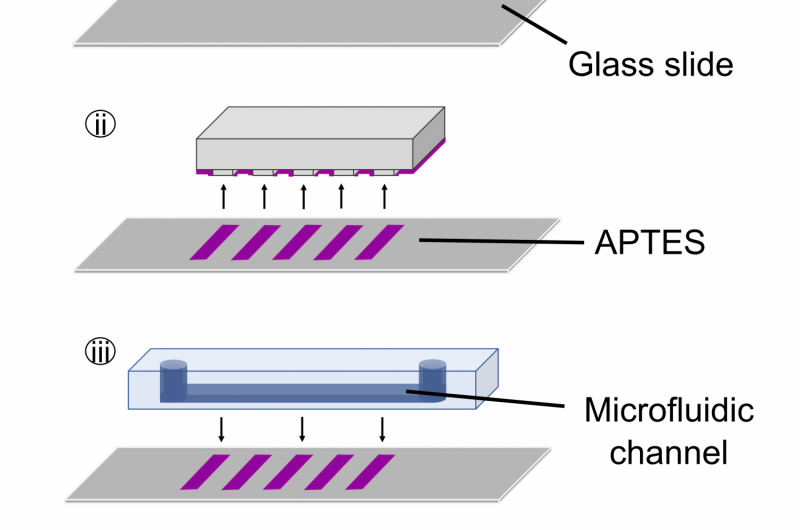
Först, en flexibel stämpel är färgad med APTES-lösningen (i). Stämpeln pressas sedan på glasytan (ii). En mikrofluidkanal placeras över APTES-mönstret på glaset (iii), och enheten är redo att användas för att immobilisera bioreceptorer och, så småningom, för att hjälpa till att ställa en diagnos (iv). Kredit:Okinawa Institute of Science and Technology Graduate University (OIST)
Systemet är nu redo att användas som en diagnostisk analys. För att utföra analysen, ett vätskeprov från en patient levereras genom mikrofluidanordningen fäst vid glaset. Om den relevanta sjukdomsbiomarkören finns, molekylen kommer att "hålla fast" på de områden som innehåller bioreceptorerna.
Det som är viktigt med APTES -lösningen är dess praktiska kemi. "Beroende på din bioreceptor av intresse, du behöver bara välja lämplig kemi för att länka molekylen med APTES, " förklarar Ms Sathish. Eller med andra ord, en stämpel kan användas för att förbereda en analys med förmågan att immobilisera en mängd olika bioreceptorer – en stämpel tillåter flera tester och diagnoser på en enda yta. Denna funktion skulle vara fördelaktig för att diagnostisera komplexa sjukdomar som cancer, som förlitar sig på tester som kan upptäcka flera markörer för att förbättra diagnosen.
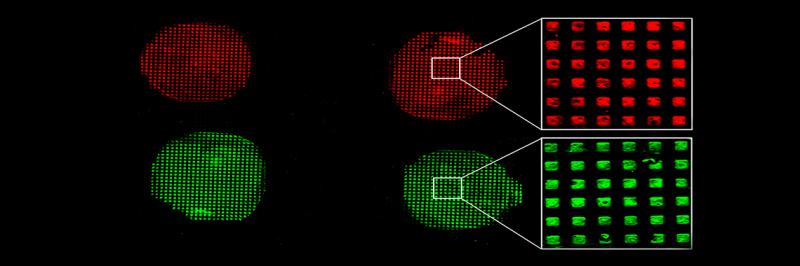
I sin forskning, Ms. Sathish och kollegor utvecklade en förbättrad teknik för att skapa den mest optimala sjukdomsdiagnostiska enheten för användning i nanoskala. Här, de mönstrade först nanoskaliga egenskaper hos APTES med ett bläck gjort av APTES i vatten, i motsats till starka kemikalier, vilket eliminerade problemet med stämpelsvällning. Sedan, de immobiliserade bioreceptorerna på ytan som det allra sista steget i processen, efter att ha mönstrat APTES och fäst mikrofluidanordningen. Genom att fästa bioreceptorerna som det sista steget, forskarna undvek att utsätta dem för extrema och skadliga förhållanden. De visade sedan effekten av den slutliga enheten genom att köra en analys för att fånga biomarkörerna interleukin 6 och humant c-reaktivt protein, två ämnen som ofta förhöjs i kroppen under inflammation.
"Det slutliga målet är att skapa en vårdcentral, "förklarar OIST -professor Amy Shen, som ledde forskningen.
"Om du får dina bioreceptorer förimmobiliserade i mikrofluidiska enheter kan du sedan använda dem som diagnostiska verktyg vid behov, " Ms. Sathish fortsätter. "[Så småningom] istället för att ha ett helt kliniskt team som behandlar ditt prov... hoppas vi att patienterna kan göra det själva hemma."