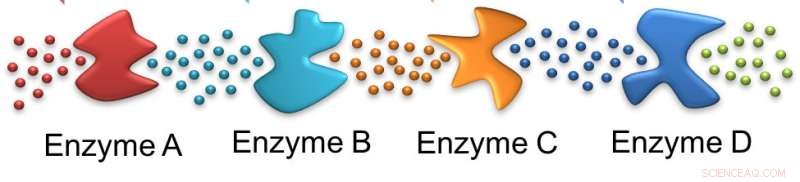
Som myror, ett enzym följer spåret som det föregående efterlämnade. I detta fall, det initiala substratet påverkas av enzym A, lämnar ett substrat lämpligt för enzym B och på linjen. Upphovsman:Ayusman Sen, Penn State
En sked socker kan få medicinen att gå ner, men att förstå vad som händer med det sockret i cellen är mycket mer komplicerat än enkel matsmältning, enligt forskare. För att socker ska metabolisera och ge energi till cellerna, en serie enzymer - biologiska katalysatorer - måste var, i tur och ordning, bryta ner en reaktant. I detta fall, forskarna använde glukos, sockret som finns i majssirap och ett av de två sockerarterna som uppstår när bordsocker - sackaros - bryts ner i kroppen.
I denna kaskad, det första enzymet verkar på glukosen som tillförs cellen och de efterföljande enzymerna fungerar på successiva produkter. I processen, två adenosintrifosfatmolekyler - ATP - förbrukas men fyra produceras. Hydrolysen av ATP driver många cellulära processer för att bibehålla cellens livskraft. Liknande enzymkaskader är ansvariga för många metaboliska processer i kroppen.
Enzymer som deltar i sådana reaktionsvägar har i vissa fall visat sig bilda intracellulära, reversibla komplex som kallas metaboloner av Paul Srere (avliden), University of Texas Southwestern Medical School. Att ha enzymerna i närheten av varandra underlättar serien av reaktioner de katalyserar. Ett sådant exempel är purinosomen som upptäcktes i Evan Pugh University Professor och Eberly Chair i kemi Stephan J. Benkovic's Lab i Penn State som består av sex enzymer som är involverade i biosyntesen av puriner.
Forskarna frågade om en av de faktorer som bidrar till metabolonbildningen kan vara en gradient av kemikalier som genereras av de deltagande enzymerna. De rapporterar sina resultat i dagens (18 december) nummer av Naturkemi .
"Vi upptäckte för en tid sedan att enkla katalysatormolekyler som enzymer också kommer att kemotaxa upp en reaktants gradient, "sade Ayusman Sen, framstående professor i kemi, Penn State. "De rör sig mot högre och högre koncentrationer av reaktant."
Rörelsen kallas kemotaxi, där enskilda molekyler migrerar längs en koncentrationsgradient av andra molekyler.
"Alla levande saker kemotaxar, "sa sen." Om du är hungrig och plötsligt luktar pommes frites, du kommer att försöka gå mot pommes fritesen. Om lukten minskar, du kommer slumpmässigt att vända dig för att försöka hitta den högre koncentrationen av fransk-stek luktmolekyler tills du är vid fransstegsdisken. "
I deras studie, forskarna använde endast de fyra första enzymerna i den glykolytiska vägen - hexokinas, fosfoglukosisomeras, fosfofruktokinas och aldolas. Dessa fyra steg förbrukar faktiskt ATP. För att studera rörelsen av enzymerna, forskarna använde fluorescerande märkning av hexokinas och aldolas, de första och fjärde enzymerna i vägen. Var och en märktes med ett annat fluorescerande färgämne så att rörelsen av båda enzymerna kunde följas.
De tittade på tre fall - den normala reaktionen där hexokinas fosforylerar glukos; reaktionen av hexokinas med mannos, ett socker som binder starkare men har en långsammare reaktionshastighet; och slutligen med L-glukos, en form av glukos som inte används av hexokinas. Fosforyleringen kräver ATP. I närvaro av fosfoglukosisomeras - det andra enzymet - och fosfofruktokinas - det tredje enzymet - produceras reaktanten för aldolas.
Forskarna observerade att aldolasen rör sig mot hexokinaset i sitt flödesexperiment, avslöjar att aldolas kemotaxar upp reaktantgradienten som produceras av funktionen av de tre första enzymerna i vägen. Kemotaxin var störst med D-glukos, mindre med mannos och observerades inte med L-glukos.
Teoretisk modellering av enzymrörelsen förutspådde kvalitativt omfattningen av enzymrörelsen.
Forskarna tittade också på om kemotaxi av enzymer skulle inträffa i en modell av den exceptionellt trånga intracellulära miljön. De tillsatte en substans med stor molekylvikt för att simulera sådan trängsel. Kemotaxi förekom fortfarande, men i en långsammare takt.
"Chemotaxis längs en kemisk gradient kan vara en faktor vid montering av enzymkluster, såsom metaboloner, "sa Benkovic." Andra faktorer, såsom icke -kovalenta interaktioner förväntas fortfarande bidra. "
Forskningsinstrumentets upplösning, dock, var otillräcklig för att i detta fall visa att de fyra enzymerna samlades till ett metabolon. Forskarna observerade bildandet av stora aggregat av enzymer, men kunde inte visa att de fungerade metaboloner.