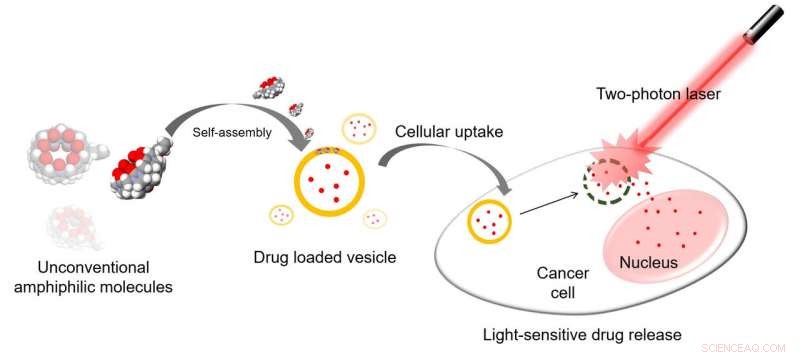
Översikt över experimentet. Ihåliga pumpaformade molekyler med allyloxisvansar sätts ihop till vesiklar som kan transportera läkemedel in i cancerceller. Sedan bryter en laser vesiklarna vilket underlättar frisättningen av läkemedlet på ett lämpligt och platsspecifikt sätt. Kredit:Institutet för grundvetenskap
Med målet att minimera biverkningarna av kemoterapi på friska vävnader, ett team av forskare vid Centrum för självmontering och komplexitet, inom Institutet för grundvetenskap (IBS) har utvecklat nya nanobehållare som kan leverera läkemedel mot cancer vid exakt tidpunkt och plats. Publicerad i Angewandte Chemie International Edition , studien kombinerar unikt designade molekyler och ljusberoende läkemedelsfrisättning, som kan ge en ny plattform för att förbättra effekten av cancerläkemedel.
Tack vare en serendipital observation, IBS-forskare vid POSTECH fick reda på att svansade pumpaformade molekyler, mono-allyloxylerad gurka[7]uril (AO1CB[7]), fungera som ytaktivt ämne i vatten. De flesta ytaktiva ämnen, som tvålmolekyler i bubblor och fosfolipider i cellmembran, har små vattenälskande (hydrofila) huvuden och långa fettälskande (hydrofoba) svansar som avgör hur de ordnar sig i rymden. I kontrast, AO1CB[7] är ganska okonventionell eftersom den bildar vesikler i vatten trots sin korta hydrofoba allyloxisvans. Detaljerad analys visade att svansarna förenar AO1CB[7]-molekyler till kolloidala partiklar.
"Att se AO1CB[7] bilda en grumlig lösning när den skakas i vatten var en oväntad överraskning för laget, " förklarar PARK Kyeng Min, studiens första och motsvarande författare. "Vi tänkte dra nytta av denna nyupptäckta egenskap och använda dessa vesikler som vehiklar för att bära läkemedel mot cancer. Sedan, genom att kontrollera när och var vesiklarna är trasiga, drogerna kunde släppas på begäran."
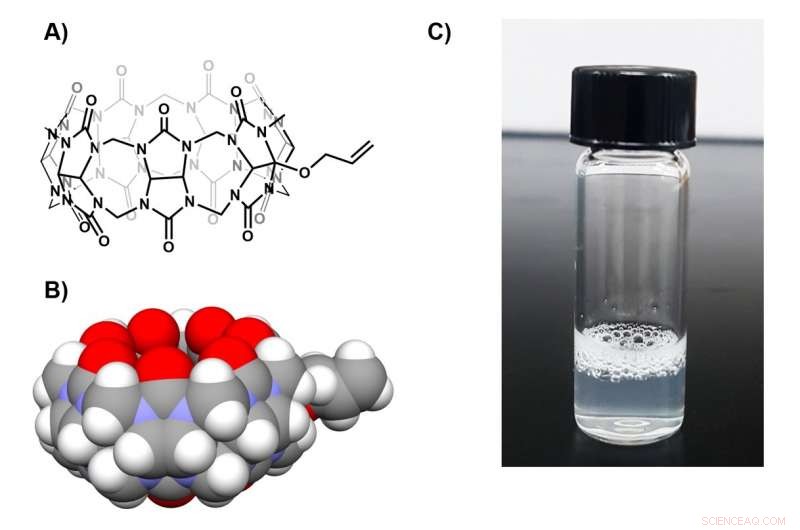
Kemisk struktur och ytaktiva egenskaper hos monoallyloxylerad gurkbit[7]uril (AO1CB[7]). A) och B) visar den kemiska strukturen hos AO1CB[7]-molekylen. C) Efter kraftig skakning av AO1CB[7] i vatten, lösningen blir grumlig och skum bildas ovanpå, vilket betyder att AO1CB[7] beter sig som ett ytaktivt ämne. Kredit:Institutet för grundvetenskap
Förutom att hjälpa AO1CB[7] att självmontera, allyloxisvansen är också ljuskänslig:den kan reagera med molekyler som glutation som normalt finns i celler när den bestrålas av UV-ljus (365 nanometer våglängd). På samma sätt som en såpbubbla som poppar, reaktionen mellan svansarna och glutationmolekylerna bryter isär AO1CB[7]-vesiklarna.
Istället för att använda UV-enkelfotonlaser för att främja glutation-allyloxisvansreaktionen, IBS-forskare använde en nära infraröd tvåfotonlaser, som har förmågan att penetrera djupare in i vävnader med ökad noggrannhet. I enkla termer, tvåfotonlasern (våglängd 720 nanometer) är ett bättre verktyg att använda än en enfotonlaser (365 nanometer) eftersom den kan nå djupare in i köttet med mindre spridning. Eftersom det bestrålade området är mindre, läkemedelstillförseln är begränsad till målområdet, vilket resulterar i mindre skada på frisk vävnad som omger tumören.
Forskargruppen tillämpade denna teknik för att leverera det kemoterapeutiska läkemedlet Doxorubicin till livmoderhalscancerceller (HeLa-celler) i laboratoriet. De observerade att drogen kunde lämna vesiklarna, nå kärnan i cancercellerna, och så småningom döda dem.
"Dessa studier på cellnivå representerar en proof-of-concept-demonstration. Nu vill vi utöka den här tekniken till djurmodeller, som cancerbärande möss, för att verifiera dess praktiska användning i olika typer av tumörer, " förklarar Park.
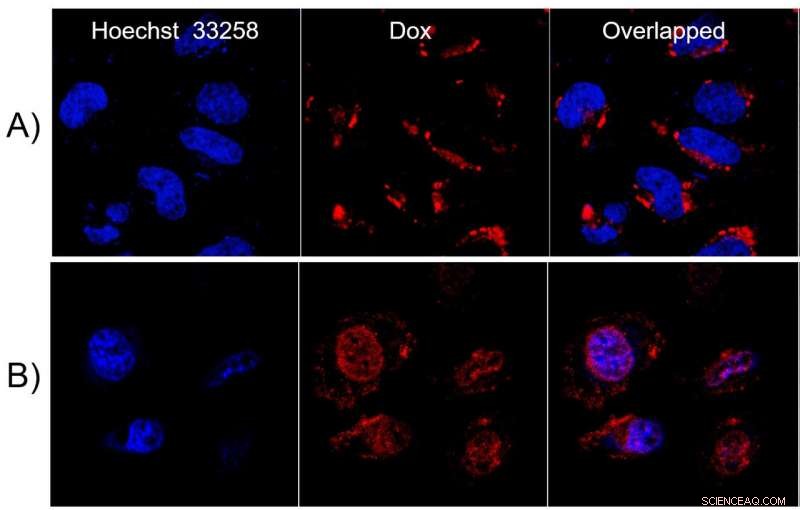
Fluorescerande mikroskopibilder av tillförsel av läkemedel mot cancer via AO1CB[7] vesiklar och tvåfoton nära infraröd laser. Det kemoterapeutiska läkemedlet Doxorubicin (Dox, i rött) fångades i AO1CB[7]-vesiklar och levererades till livmoderhalscancerceller (HeLa-celler). Bilden jämför platsen för Dox i frånvaro A) och närvaro B) av infraröd tvåfotonlaserbestrålning. I B) är läkemedlet synligt inuti kärnan (färgad i blått), vilket betyder att vesiklarna stördes och läkemedlet kunde nå kärnan, där den bekämpar cancertumören med ökad effektivitet. Kredit:Institutet för grundvetenskap