Ett schema av en bakteriecell med ett fragment av en metabolisk kedja som fungerar inuti den omgiven av glycerol eller sackaros som imiterar den intracellulära miljön. Kredit:Oleg Sutormin.
Ett team från Institute of Fundamental Biology and Biotechnology of SFU använde glycerol och sackaros för att simulera den intracellulära miljön av självlysande bakterier och utförde ett antal enzymatiska reaktioner. De hoppas kunna utveckla fragment av metaboliska kedjor med olika längd och studera fermentativa reaktioner under tillstånd nära intracellulära. Forskningen publicerades i Molekylär katalys tidning.
Hundratals reaktioner som involverar enzymer inträffar ständigt i celler. För att studera dem mer i detalj, forskare försöker skapa omfattande experimentella modeller av den intracellulära miljön. En intressant egenskap hos sådana artificiella miljömodeller är möjligheten att justera sina parametrar för att förstå hur en viss enzymreaktion skulle reagera och skillnaderna mellan enzymreaktioner i en cell och de i rörförhållanden.
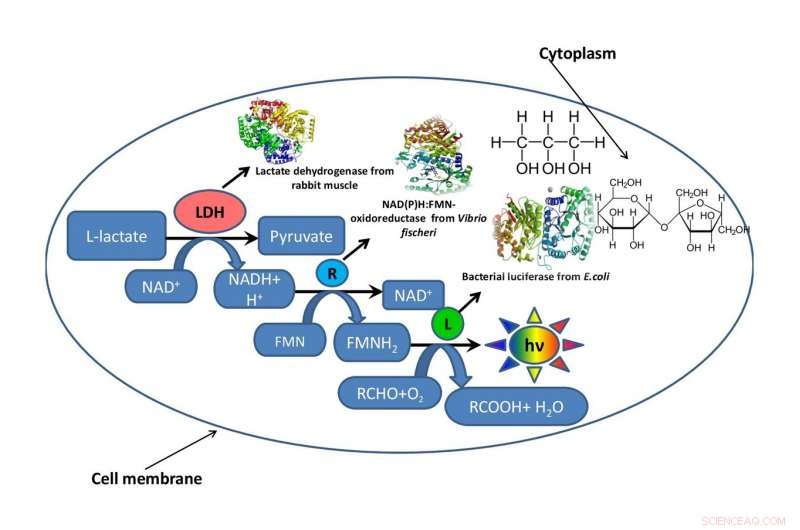
För att förstå hur reaktionsblandningens viskositet påverkar hastigheten för enzymatiska processer, ett team från Institute of Fundamental Biology and Biotechnology of SFU simulerade den intracellulära miljön med hjälp av två organiska lösningsmedel - glycerol och sackaros. För att testa effekten av reaktionsblandningens viskositet, forskarna använde ett fragment av en bioluminiscent metabolisk kedja.
Arbetet bestod av tre steg. På första etappen, biofysikerna utvecklade flera konstgjorda modellsystem gjorda av glycerol och sackaros med olika koncentrationer av komponenter, men samma viskositetsnivåer för reaktionsmediet. På andra etappen, de bestämde hur reaktionsblandningens viskositet påverkade hastigheten på en enzymatisk reaktion i det kopplade systemet av tre enzymer:LDH, NAD(P)H:FMN-oxidoreduktas, och luciferas. På tredje etappen, forskarna utvärderade den termiska stabiliteten hos trippelenzymsystemet vid temperaturintervallet från 15 till 80 grader.
Som ett resultat av studien, forskarna drog slutsatsen att sackaros begränsade enzymernas rörlighet mer effektivt än glycerol. Rörlighetsbegränsning kan leda till förändringar i reaktionshastigheten eller till och med mekanismen. Forskarna rekommenderar ytterligare studier av den ökande termiska stabiliteten hos enzymer i viskösa reaktionsblandningsmiljöer och ökande temperatur. De föreslår också ett tillvägagångssätt för att konstruera de cellulära multienzymmetaboliska kedjorna inuti den lysande bakteriecellen.
"På grund av det enorma antalet enzymreaktioner inuti en riktig cell, för att metabolismprocessen ska fortgå snabbt och kontinuerligt inom den, enzymer bör ha hög kooperativitet. Därför, desto mer förändring av den termiska stabiliteten hos enzymer i närvaro av viskogener, ju bättre samarbete mellan studerade enzymsystem inuti de verkliga cellförhållandena, och desto större är möjligheten att ett artificiellt fragment av en metabolisk kedja skulle vara naturligt för en bakteriecell. Det är extremt viktigt att studera inverkan av viskösa organiska lösningsmedel på hastigheten och termisk stabilitet hos enzymatiska reaktioner. Det unika med vår studie är att vi använder naturliga föreningar - glycerol och sackaros som faktiskt finns i den verkliga cellen, i motsats till trängselmedel som används i liknande studier av andra forskare, " säger Oleg Sutormin, en medförfattare till studien, och juniorforskare vid Laboratory of Bioluminescent Biotechnologies of SFU.