
Väte i sitt plasmatillstånd. Upphovsman:Alchemist-hp
Ett vanligt antagande inom kemi är att koordinatornumret för en katalysatoryta bestämmer reaktiviteten för reaktionen som den katalyserar. Slående, kemister från universitetet i Leiden har nu bevisat att detta inte är sant för naturens enklaste kemiska reaktion:dissociering av väte. Forskarna lyckades mäta den så kallade absoluta reaktiviteten i denna reaktion, en första i vetenskap. De publicerade sina fynd i Angewandte Chemie .
Hemligt vapen
Katalysatorer används ofta i våra dagliga liv, t.ex. platinakatalysatorn i din bilavgas. Dock, det är ofta inte förstått hur de exakt fungerar. Professor Ludo Juurlink och hans grupp försöker ändra på detta och har ett hemligt vapen för att göra det:en böjd platinayta. Förra året, denna utrustning gav dem två publikationer i ledande tidskrifter:in Vetenskap de bevisade slutligen vilken teoretisk modell för reaktion av väte på platina som är korrekt och in PNAS de visade hur syre reagerar på platina. Nu, kemisterna använde denna speciella platina för att skaka om en viktig etablerad idé inom kemi:samordning.
Zooma in på en katalysator
För att förklara detta, vi måste först titta på ytan på en katalysator, där kemiska reaktioner äger rum. Denna yta består av atomer - platinaatomer i denna studie - som är inriktade på ett specifikt sätt. Varje atom har ett annat koordinationsnummer, som anger hur många andra atomer som omger just denna atom. Om vi tar reaktionen av väte på platina som ett exempel, den allmänna idén var följande:koordinationsnumret för atomerna på ytan av platina bestämmer reaktiviteten mot molekylärt väte.
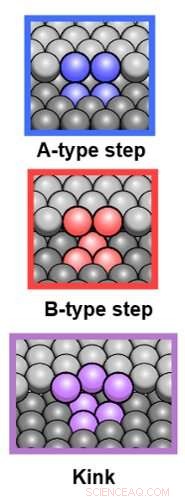
De tre typerna av oegentligheter. Kredit:Leiden University
Leiden -teamet använde två krökta platina -kristaller för att testa denna hypotes. "Eftersom platinaytan är krökt, atomstrukturen förändras mycket gradvis längs ytan, "förklarar gruppledaren Juurlink." Du kan jämföra denna struktur med en trappa, vars steg mot kanterna blir smalare och smalare. I mitten, det ser mer ut som en balsal. "Men varför är det viktigt? En katalysators yta är inte plan och slät, men oregelbunden, med steg och knäck. Och precis vid dessa oegentligheter, kemiska reaktioner äger rum. Med den böjda platina, forskarna efterliknar denna effekt, samtidigt som man vet exakt hur många steg eller knän varje del av kristallen har. Detta gjorde det möjligt för kemisterna att mäta reaktiviteten av väte jämfört med densiteten av steg eller knäckar på platina.
Steg och knäck
"Vi identifierade tre typer av oegentligheter, "säger doktorandkandidaten Sabine Auras, första författaren till studien. "Det finns A-typ, B-typen, och den böjda typen. "För varje typ, hon mätte reaktiviteterna. Om ytan har fler steg eller fler knäckar, reaktiviteten ökar. Än så länge, inget nytt under solen. "Men vi fann också att denna ökning är olika för varje typ av oegentligheter. Och denna skillnad motsvarar inte vad man kan förvänta sig när det gäller samordning." Istället, laget definierade tvärsnitt för växelverkan och steg eller knäckar, som är ett viktigt landmärke för andra forskare inom området.
Långsiktighet
Grunden för denna publikation i Angewandte Chemie lades för fem år sedan när tidigare doktorand kandidaten Dima Bashlakov upptäckte något speciellt när han studerade en krökt platinakristall. "Jag tror att vår forskning stöder idén att vetenskaplig finansiering aldrig ska fokuseras på kortsiktiga visioner eller kortsiktiga resultat, "säger Juurlink." Tyvärr nog, det är båda aspekter som verkar så vanliga i forskningsapplikationer nuförtiden. "
Auras tillägger:"Jag förstår att vi har ett ansvar för samhället. Men med en viss grad av frihet, som långsiktig finansiering kan ge, vi kan få riktigt unika resultat. Du kan inte alltid styra vetenskapen. "