
Ny MIT-forskning beskriver hur marina mikroorganismer bidrar till ett lager av nitrit strax under havets solbelysta zon. Kredit:Massachusetts Institute of Technology
Kväve är en het råvara i ythavet. Primärproducenter inklusive växtplankton och andra mikroorganismer konsumerar och omvandlar det till organiska molekyler för att bygga biomassa, medan andra omvandlar oorganiska former för att komma åt deras kemiska energiförråd. Alla dessa steg är en del av den komplexa kvävecykeln i den övre vattenpelaren.
Cirka 200 meter ner, strax under havets solbelysta zon, ligger ett lager av nitrit, en mellanliggande förening i kvävecykeln. Forskare har hittat denna robusta funktion, kallas det primära nitritmaximum, i hela världens syresatta hav. Medan flera individuella hypoteser har lagts fram, ingen har övertygande förklarat denna marina signatur förrän nu.
En nyligen Naturkommunikation studie ledd av forskare inom programmet i atmosfärer, Oceans and Climate (PAOC) inom MIT:s Department of Earth, Atmospheric and Planetary Sciences (EAPS) använder teori, modellering, och observationsdata för att undersöka de ekologiska mekanismerna som producerar den observerade nitritansamlingen och dikterar dess placering i vattenpelaren. Huvudförfattaren Emily Zakem – en före detta doktorand i EAPS som nu är postdoc vid University of Southern California – tillsammans med EAPS:s huvudforskare Stephanie Dutkiewicz och professor Mick Follows visar att fysiologiska begränsningar och resurskonkurrens mellan växtplankton och nitrifierande mikroorganismer i det solbelysta lagret kan ge detta havsdrag.
Reglering av den biologiska pumpen
Trots sin låga havskoncentration, nitrit (NO2-) spelar en nyckelroll i globala kol- och kvävekretslopp. Det mesta av kvävet i havet finns i den oorganiska formen av nitrat (NO3-), vilka primärproducenter och mikroorganismer kemiskt reducerar det för att bygga organiska molekyler. Remineralisering sker när den omvända processen äger rum:Växtplankton och andra heterotrofa bakterier bryter ner dessa organiska föreningar till ammonium (NH4+), en form av oorganiskt kväve. Ammonium kan sedan konsumeras igen av primärproducenter, som får sin energi från ljus. Andra mikroorganismer som kallas kemoautotrofer använder också ammonium både för att tillverka ny biomassa och som energikälla. Att göra detta, de utvinner syre från havsvatten och omvandlar det, en process som kallas nitrifikation, som sker i två steg. Först, mikroberna omvandlar ammonium till nitrit och sedan till nitrat.
Någonstans längs linjen, nitrit har ansamlats vid basen av den solbelysta zonen, vilket har konsekvenser för havets biogeokemi. "Brett, vi försöker förstå vad som styr remineraliseringen av organiskt material i havet. Det är den där remineraliseringen som är ansvarig för att bilda den biologiska pumpen, vilket är den extra lagringen av kol i havet på grund av biologisk aktivitet, " säger Zakem. Det är detta starka inflytande som kvävet har på den globala kolcykeln som fångar Follows intresse. "Tillväxt av växtplankton på nitrat kallas "nyproduktion" och det balanserar mängden som sjunker ut från ytan och styr hur mycket kol lagras i havet. Tillväxt av växtplankton på ammonium kallas återvunnen produktion, som inte ökar lagringen av kol i havet, ", säger Follows. "Så vi vill förstå vad som styr utbudet och den relativa konsumtionen av dessa olika kvävearter."
Kampen om kvävet
Det primära nitritmaximumet ligger mellan två grupper av mikroorganismer i de flesta av världens hav. Ovanför den i den solbelysta zonen finns växtplankton, och i det primära nitritmaximumet och något under det vilar ett överflöd av nitrifierande mikrober i ett område med höga nitrifikationshastigheter. Forskare klassificerar dessa mikrober i två grupper baserat på deras föredragna kvävekälla:de ammoniumoxiderande organismerna (AOO) och nitritoxiderande organismer (NOO). På höga breddgrader som jordens subpolära områden, nitrit ansamlas i den solbelysta ytan såväl som djupare.
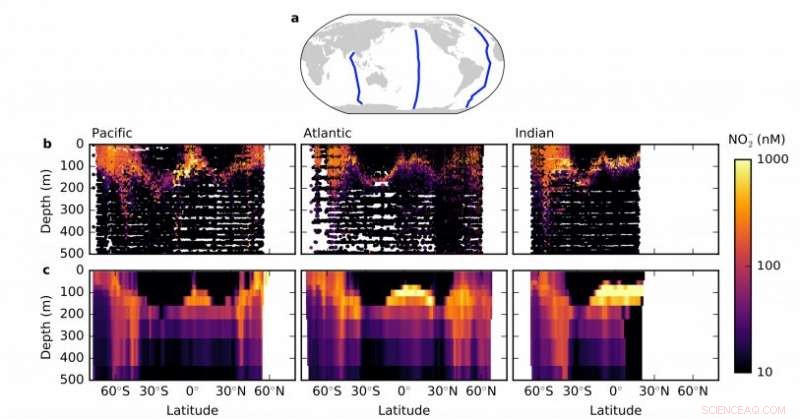
En ekosystemmodell visar koncentrationerna av nitrit efter djup (vertikal profil) över tre havstransekter. Kredit:Massachusetts Institute of Technology
Forskare har antagit att det kan finnas två inte ömsesidigt uteslutande orsaker till uppbyggnaden av nitrit:Nitrifikation genom kemoautotrofiska mikrober, och när man är stressad, växtplankton kan reducera nitrat till nitrit. Eftersom isotopiska bevis inte stöder det senare, gruppen tittade på det förra.
"Den långvariga hypotesen var att platserna för nitrifikation kontrollerades av hämningen av ljuset från dessa [nitrifierande] mikroorganismer, så mikroorganismerna som utför denna process var begränsade från ytan, " Zakem säger, antyder att dessa nitrifierande kemoautotrofer blev solbrända. Men istället för att anta att det var sant, gruppen undersökte de ekologiska interaktionerna mellan dessa och andra organismer i ythavet, låta dynamiken falla ut naturligt. För att göra detta samlade de mikrobiella prover från det subtropiska norra Stilla havet och utvärderade dem för ämnesomsättningshastigheter, effektivitet och överflöd, och bedömde de fysiologiska behoven och begränsningarna hos de olika nitrifierande mikroberna genom att minska deras metabolismers biologiska komplexitet till dess underliggande kemi och därmed hypotisera några av de mer grundläggande begränsningarna. De använde denna information för att informera om dynamiken hos de nitrifierande mikroberna i både en endimensionell och tredimensionell biogeokemisk modell.
Gruppen fann att genom att använda detta ramverk, de skulle kunna lösa interaktionerna mellan dessa nitrifierande kemoautotrofer och växtplankton och därför simulera ackumuleringen av nitrit vid det primära nitritmaximumet på lämpliga platser. I ythavet när oorganiskt kväve är en begränsande faktor, växtplankton och ammoniumoxiderande mikrober har liknande förmåga att förvärva ammonium, men eftersom växtplankton behöver mindre kväve för att växa och ha en snabbare tillväxt, de kan konkurrera ut nitrifierarna, exkludera dem från den solbelysta zonen. På det här sättet, de kunde ge en ekologisk förklaring till var nitrifikation sker utan att behöva förlita sig på ljusinhibering som dikterar platsen.
Jämförelse av nitrifiernas grundläggande fysiologier avslöjade att skillnader i metabolism och cellstorlek skulle kunna stå för nitrituppbyggnaden. Forskarna fann att det andra steget i nitrifikationsprocessen som utförs av nitritoxiderarna kräver mer kväve för samma mängd biomassa som skapas av dessa organismer, vilket innebär att ammoniakoxidationsmedel kan göra mer med mindre, och att det finns färre nitritoxiderare än ammoniakoxidanterna. De nitritoxiderande mikroberna har också en högre yta-till-volymbegränsning än de mindre och allestädes närvarande ammoniumoxiderande mikroberna, försvårar kväveupptaget. "Detta är en alternativ förklaring till varför nitrit bör ackumuleras, " säger Zakem. "Vi har två skäl som pekar i samma riktning. Vi kan inte skilja på vilken det är, men alla observationer överensstämmer med att någon av dessa två eller någon kombination av båda är kontrollen."
Forskarna kunde också använda en global klimatmodell för att reproducera en ansamling av nitrit i den solbelysta zonen av platser som subpolära regioner, där växtplankton begränsas av en annan resurs än kväve som ljus eller järn. Här, nitrifier kan samexistera med växtplankton eftersom det finns mer kväve tillgängligt för dem. Dessutom, det djupa blandade lagret i vattnet kan dra resurser bort från växtplanktonet, ger nitrifierarna en bättre chans att överleva i ytan.
"Det finns en långvarig hypotes att nitrifierarna hämmades av ljus och att det är därför de bara existerar under ytan, " säger Zakem. "Vi säger att vi kanske har en mer grundläggande förklaring:att denna ljusinhibition existerar för att vi har observerat den, men det är en konsekvens av långvarig uteslutning från ytan."
Tänker större
"Denna studie drog ihop teori, numeriska simuleringar, och observationer för att reta isär och ge en enkel kvantitativ och mekanistisk beskrivning av några fenomen som var mystiska i havet, ", säger Follows. "Det hjälper oss att reta isär kvävekretsloppet, som har en inverkan på kolets kretslopp. Det har också öppnat lådan för att använda den här typen av verktyg för att ta itu med andra frågor inom den mikrobiella oceanografin. "Han noterar att det faktum att dessa mikrober skiftar ammonium till nitrat nära den solbelysta zonen komplicerar historien om kollagring i havet.
Två forskare som inte var involverade i studien, Karen Casciotti, docent vid Stanford University Department of Earth System Science, och Angela Landolfi, en forskare vid avdelningen för marin biogeokemisk modellering vid GEOMAR Helmholtz Center for Ocean Research Kiel, hålla med. "Denna studie är av stor betydelse eftersom den ger bevis på hur organismers individuella egenskaper påverkar konkurrenskraftiga interaktioner mellan mikrobiella populationer och ger en direkt kontroll över näringsämnenas distribution i havet, " säger Landolfi. "I huvudsak Zakem et al., ge en bättre förståelse för kopplingen mellan olika nivåer av komplexitet från individ till samhälle upp till miljönivå, tillhandahålla en mekanistisk ram för att förutsäga förändringar i samhällets sammansättning och deras biogeokemiska påverkan under klimatförändringar, säger Landolfi.
Den här historien återpubliceras med tillstånd av MIT News (web.mit.edu/newsoffice/), en populär webbplats som täcker nyheter om MIT-forskning, innovation och undervisning.