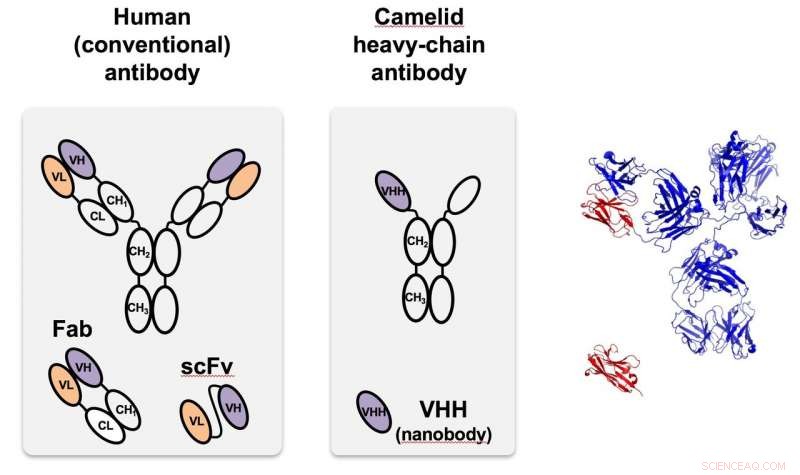
Den kameliska nanokroppen (mitten), först identifierad i kameler, är en antikropp med tung kedja som är mycket mindre och lättare att programmera än antikroppar som finns i de flesta organismer, inklusive människor, så till vänster. Till höger, den monomera kameliden (röd) jämförs med strukturen hos den humana antikroppen i full storlek. VHH är en nanobody designad för att rikta in sig på gröna fluorescerande proteiner som används i proof-of-principe-tester på Rice. Kredit:Segatori Research Group/Rice University
En antikropp i nanoskala som först hittades i kameler i kombination med en proteinnedbrytande molekyl är en effektiv ny plattform för att kontrollera proteinnivåer i celler, enligt forskare från Rice University. Tekniken kan hjälpa till med grundläggande forskning om cellulär dynamik såväl som designen av syntetiska genkretsar.
Riskemi och biomolekylär ingenjör Laura Segatori, före detta doktorand Wenting Zhao och tidigare doktorand Lara Pferdehirt uppfann ett bifunktionellt igenkänningssystem som de kallar NanoDeg. Det tillåter dem att rikta in sig på specifika proteiner i en cell och strikt reglera deras nedbrytning.
Plug-and-play-systemet kommer att tillåta syntetiska biologer att studera funktionen av ett specifikt protein i den cellulära miljön genom att bedöma hur proteinuttrycksnivån påverkar en cells liv, sa Segatori.
Forskningen visas i tidskriften American Chemical Society ACS syntetisk biologi .
NanoDeg accelererar proteolysen – den enzymatiska nedbrytningen av proteiner – för att kontrollera nivåerna av målproteiner efter translation.
En funktion kommer från den enkelkedjiga antikroppen från kamelider, som kan anpassas för att rikta specifika proteiner. När antikropparna upptäcktes i kameler (och senare hajar), forskare upptäckte snabbt deras unika egenskaper, inklusive deras ringa storlek, hög löslighet och förmåga att känna igen även mål som är dolda eller i mellanliggande tillstånd. De är mycket mindre än de antikroppar som finns naturligt i människor och de flesta andra organismer men kan lätt tillverkas och modifieras i bakterier och andra celler.
Den andra funktionen är beroende av degroner, korta sekvenser i proteiner som är ansvariga för att reglera hastigheten för ett proteins nedbrytning. Dessa kan också anpassas för att justera utarmningen av ett målprotein till önskade nivåer.
I kombination med NanoDegs, de blir en mäktig, universell plattform för att modulera cellulära proteinnivåer, Segatori sa.
"Väsentligen, det tillåter oss att kontrollera den specifika mängden proteiner i celler, " sa hon. "Vi kan skräddarsy det för att rikta in sig på vilket protein som helst i en cell, och när den degronmärkta nanokroppen binder till den partnern, hela komplexet försämras.
"Fördelen med detta system är att det riktar sig till uttryck på proteinnivå, " sa Segatori. "Typiskt, när människor vill modulera mängden proteiner i celler, de verkar på DNA eller RNA - den genetiska - nivån. Men genom att agera på proteinnivå, vi kan rikta in oss på olika modifieringar efter reglering, och mycket viktigare, vi har mycket mer kontroll över hastigheten och graden av utarmning av proteinet."
Som ett principbevis, forskarna designade en syntetisk genkrets som uttryckte både grönt fluorescerande protein (GFP), som forskare använder för att rapportera om cellulära processer, och en NanoDeg som riktar sig mot det. "Vi använde GFP eftersom det är en vanlig reporter och fluorescens är lätt att mäta, " Sa Segatori. "När nanobody känner igen GFP, hela komplexet tas för nedbrytning."
Det kommer också att vara användbart för dem som vill ha renare information om aktiviteten hos proteiner i celler.
"Säg att du utformar en genetisk krets där GFP -uttryck aktiveras när cellen är under stress, som näringssvält eller värme, till exempel, " sade Segatori. "När cellen utsätts för stimulans, GFP uttrycks och du kan upptäcka en ökning av cellfluorescens.
"Men när du tar bort stimulansen, sönderfallet av signalen återspeglar inte nödvändigtvis sönderfallet av stimulansen; det återspeglar stabiliteten hos GFP-reportern, " sa hon. "Vad vi har gjort är att skapa en genkrets där GFP-uttryck aktiveras under stimulans, men när stimulansen stängs av, NanoDeg försämrar GFP mycket snabbt. Det ökar känsligheten och dynamiska upplösningen för en syntetisk genkrets. "