Kärnan i var och en av dina celler innehåller all genetisk information (genomet) som behövs för att bygga upp alla typer av celler och protein i hela din kropp. Som ett komplext bibliotek i ett litet utrymme som är 50 gånger mindre än ett mänskligt hårstrå, är gener organiserade i exakta områden i tre dimensioner.
Förutom genomet innehåller kärnan strukturer som kallas kärnkroppar som innehåller höga koncentrationer av specifika proteiner och nukleinsyror. Nukleära kroppars roll har dock varit ett mysterium i nästan ett sekel. En ny studie från laboratoriet av Caltechs Mitch Guttman, professor i biologi, visar att dessa kärnkroppar kan fungera som miniatyrfabriker för att möjliggöra effektiv produktion av mRNA.
mRNA-splitsning är en grundläggande del av processen som sker när kodade DNA-instruktioner omvandlas till ett funktionellt protein. Efter att en gen har transkriberats från DNA till RNA måste främmande sektioner (kallade introner) skäras ut, en process som underlättas av splitsning av enzymer.
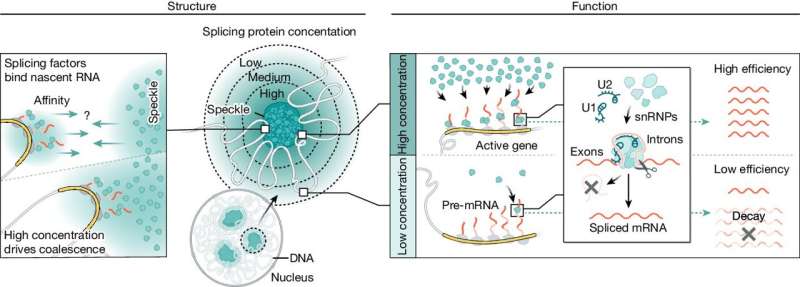
I den nya studien undersökte Caltech-forskarna en viss typ av kärnkropp, kallad kärnfläcken, som innehåller höga koncentrationer av splitsningsenzymer. Guttmans team upptäckte att genomet fysiskt förskjuter sig själv så att mycket transkriberade gener är i närheten av fläckar, vilket möjliggör effektivare splitsning.
Fynden har implikationer för både grundläggande vetenskaplig förståelse av sambandet mellan kärnstruktur och cellulär funktion och, i slutändan, för framtida terapeutisk utveckling för sjukdomar där mRNA-skarvning påverkas, inklusive för neurodegenerativa tillstånd som ALS.
Uppsatsen som beskriver resultaten publicerades i tidskriften Nature den 8 maj. Den har titeln "Genomorganisation kring kärnfläckar driver mRNA-splitsningseffektivitet."
Under ett decennium har forskare i Guttman-laboratoriet studerat hur kärnan är rymdligt organiserad – layouten på biblioteket, med andra ord. 3D-strukturerna som DNA beställs i gör vissa gener mer eller mindre tillgängliga för maskineriet som omvandlar DNA till mRNA, och den nya studien visar att genomets fysiska struktur kopplar transkription till splitsningsprocessen.
En muskelcell, till exempel, kommer att flytta runt sitt genom så att starkt transkriberade gener för muskelaktivitet är i fysisk närhet till nukleära prickar, där höga koncentrationer av splitsningsenzymer gör RNA-skarvningen särskilt effektiv. En neuronal cell, å andra sidan, kommer att omorientera sitt genom i rymden så att de gener som är nödvändiga för att producera celler som är specialiserade för neurologisk funktion är närmare prickarna.
"Vi vet att splitsning är beroende av enzymer, och varje mutation som stör koncentrationen av enzymer har dramatiska effekter", säger Prashant Bhat, en forskarassistent inom biologi och biologisk teknik och studiens första författare.
"Tidigare tenderade vi att tänka på splitsning som en konstant – du gör ett pre-mRNA; du splitsar det. Nu vet vi att kärnans fysiska organisation gör stor skillnad i effektiviteten av splitsning och, i förlängningen, andra processer ."
Många sjukdomar, inklusive neurodegenerativa störningar och cancer, har en gemensam egenskap:dysfunktionell RNA-skarvning. Även om det inte är känt om felaktig skarvning är en primär orsak till sjukdom eller en effekt, är skarvningsprocessen i slutändan ett lovande mål för behandlingar.
Till exempel kan sjukdomar där ett otillräckligt antal proteiner tillverkas (känd som haploinsufficienssjukdomar) behandlas genom att flytta den normala kopian av genen för det proteinet nära nukleära prickar för att öka splitsningen och återställa hälsosamma proteinnivåer.
Mer information: Prashant Bhat et al, Genomorganisation kring kärnfläckar driver mRNA splitsningseffektivitet, Nature (2024). DOI:10.1038/s41586-024-07429-6
Journalinformation: Natur
Tillhandahålls av California Institute of Technology