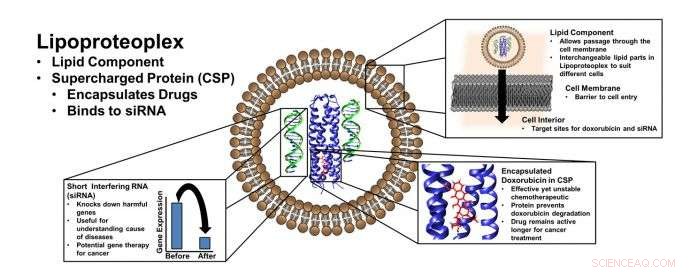
Lipoproteoplex använder en "lipidbehållare" för transfektion - transport av material förbi ett cellmembran - och en lätttillverkad proteinkapsel som kan binda både småmolekylära kemoterapeutiska läkemedel och genetisk teknologi, såsom kort interfererande RNA (siRNA), som kan "tysta" gener som sprider sjukdomstillstånd. Kredit:NYU Tandon School of Engineering
Kliniker har idag en arsenal på mer än 200 läkemedel till sitt förfogande för att behandla en rad cancerformer – 68 läkemedel godkändes bara mellan 2011 och 2016. Men många kemoterapeutiska medel utgör envisa utmaningar:de orsakar allvarliga biverkningar eftersom de dödar friska celler förutom cancerceller; vissa former av cancer utvecklar resistens mot läkemedel; och många sådana kemoterapier, är dåligt vattenlöslig, visa låg biotillgänglighet vilket resulterar i suboptimal läkemedelsleverans till cancerceller.
En potentiell lösning ligger i den synergistiska kombinationen av ett kemoterapeutiskt läkemedel med konstruerat genetiskt material utformat för att neutralisera de illvilliga generna som ger resistens mot det läkemedlet, bland andra funktioner.
Även om det finns många exempel på syntetiska vehiklar för dubbla gener och läkemedelstillförsel, nya hybridmaterial som utvecklats i labbet vid NYU Tandon School of Engineering använder lätt modifierbara proteiner för att leverera en kemisk en-två-stämpel:de kombinerar en lipid-"behållare" för transfektion - transport av last förbi ett cellmembran - och en enkel- för att göra proteinkapsel som kan binda både små kemoterapeutiska molekyler och nukleinsyror.
Utvecklat av ett team ledd av NYU Tandon docent i kemi- och biomolekylär teknik Jin Kim Montclare - som också fungerar som en affiliate professor i kemi vid NYU:s College of Arts and Sciences, och en affiliate professor i biomaterial vid NYU College of Dentistry, samt att vara ansluten till SUNY Downstate som professor i biokemi – det hybrida lipid-proteinmaterialet, kallas ett lipoproteoplex, består av både en lindad överladdad proteinmakromolekyl och ett kommersiellt tillgängligt transfektionsmedel som kallas Lipofectamine 2000.
Eftersom forskarna konstruerade proteinmakromolekylen med omfattande positiva laddningar på ytan och en hydrofob kärna, det kan lätt prydas med negativt laddat kort interfererande RNA (siRNA) – ett kraftfullt verktyg för att undertrycka gener som framkallar läkemedelsresistens och sprider sjukdomstillstånd – samtidigt som det fungerar som ett effektivt, och toxicitetsreducerande, carryall för det hydrofoba kemoterapeutiska medlet doxorubicin.
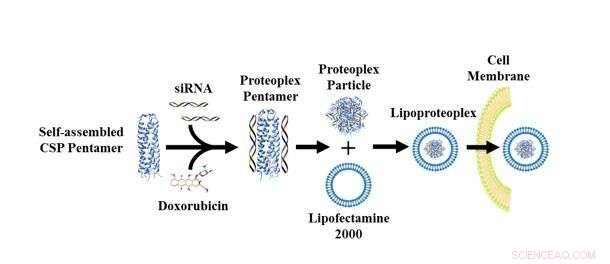
Lipoproteoplex tillåter forskare att byta ut ett överladdat protein eller lipidkomponent och valfritt antal siRNA för att adressera en specifik cellinje och typ av läkemedel. Kredit:NYU Tandon School of Engineering
I forskning publicerad i Biomakromolekyler , en tidskrift från American Chemical Society, Teamet beskriver hur lipoproteoplexet som exponerats för prover av bröstcancercellinjen MCF-7 levererade mer doxorubicin till målceller än Lipofectamine 2000 enbart, vilket resulterar i en avsevärd minskning av MCF-7-cellviabiliteten. De visade också att hybridmakromolekylen var mycket framgångsrik vid siRNA-transfektion, tystar genen med 60 procent.
Montclare sa att en viktig fördel med det nya lipoproteoplexet är att det är lätt att modifiera, en tillgång för forskare som studerar celler vars genetiskt anropade beteende förändras över tiden och skiljer sig åt beroende på cellinje och patient. Snarare som ett system av mix-and-match-komponenter, lipoproteoplexet tillåter forskare att byta ut ett överladdat protein eller lipidkomponent och valfritt antal siRNA för att adressera en specifik cellinje och typ av läkemedel.
"Till skillnad från andra sysselsättningar med att producera dubbla gen- och läkemedelstillförselsystem, detta tillvägagångssätt kräver inte tråkiga kemiska syntesförfaranden; snarare kan vi biosyntetisera vilken variant som helst av det överladdade proteinet, ", sa hon. "Detta gör det möjligt att ersätta olika siRNA-molekyler och kemoterapeutiska läkemedel för att passa laboratoriets behov."
I det senaste arbetet med proteinbaserade hybridmaterial, Montclare och hennes medarbetare kombinerade ett konstruerat överladdat protein med transfektionsreagenset Fugene. Kombinationen uppvisade en åttafaldig förbättring av transfektionseffektiviteten för DNA jämfört med Fugene enbart, med försumbar cytotoxicitet.
Montclare undersöker mekanismerna som gör det möjligt för dessa lipoproteoplexer att effektivt leverera gener och läkemedel över olika cellinjer.