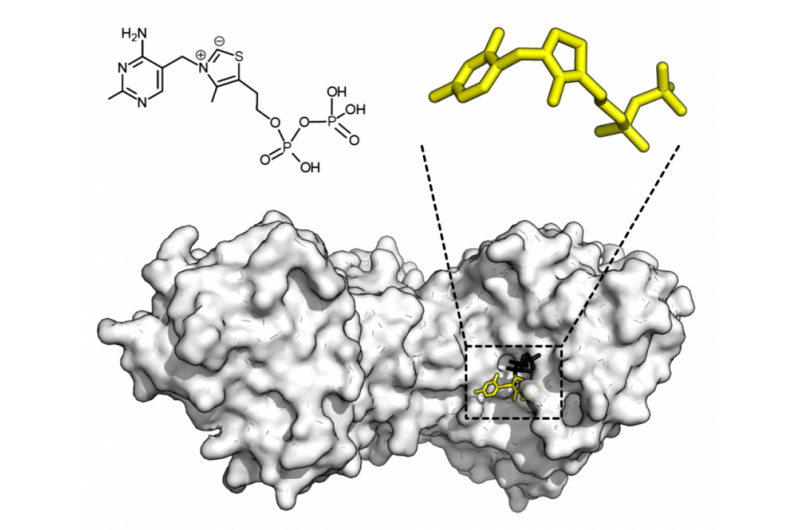
Kemisk struktur för tiaminpyrofosfat och proteinstruktur av transketolas. Tiaminpyrofosfatkofaktor i gult och xylulosa 5-fosfatsubstrat i svart. Upphovsman:Thomas Shafee/Wikipedia
Forskare vid McGill University har uppfunnit en ny teknik för att mäta hur snabbt läkemedel interagerar med deras molekylära mål. Upptäckten ger forskare ett nytt sätt att undersöka effektiviteten av läkemedelskandidater som annars skulle ha förbisetts.
Den nya metoden fokuserar på principen om enzymhämning. Otaliga läkemedel, allt från antibiotika till kemoterapiläkemedel, fungerar genom att blockera verkan av enzymer, och sökandet efter nya enzymhämmande ämnen är fortfarande ett stort fokus för läkemedelsutvecklingen.
I en tidning publicerad i Naturkommunikation , McGill-teamet, ledd av kemiprofessorerna Nicolas Moitessier och Anthony Mittermaier, demonstrera användningen av isotermisk titreringskalorimetri (ITC) för att mäta värmen som genereras av enzymaktivitet och därigenom de hastigheter med vilka inhibitorsubstanser blockerade denna aktivitet.
"En viktig skillnad mellan ITC och andra metoder är att ITC mäter reaktionshastigheten direkt, "Förklarar Mittermaier.
Befintliga metoder för att mäta enzymaktivitet ser indirekt på den aktiviteten. genom att mäta förändringar i koncentration orsakade av enzymatisk katalys som en funktion av tiden. Dessa mätningar beror ofta på speciella reagenser som ändrar färg eller fluorescens när de påverkas av enzymet, och kräver att ett unikt test utvecklas för varje enzym som studeras.
Eftersom ITC mäter produktionen av värme - ett nästan universellt inslag i kemiska reaktioner - kan det appliceras på nästan vilket enzym som helst.
"ITC är så nära du kan komma till ett universellt enzymtest, " säger Mittermaier.
Förutom dess allmänhet, ITC-metoden ger en direkt avläsning av enzymaktivitet eftersom den detekterar värmeflöde i realtid. Genom att ge ett direkt fönster om reaktionen, ITC ger forskare en bättre inblick i de mekanismer genom vilka enzymhämning fortskrider. Det är vanligtvis mycket utmanande, och ibland nästan omöjligt, för att få denna information från konventionella analyser.
ITC:s realtid är särskilt lovande för forskare som undersöker kovalenta hämmare. Dessa starkt bindande molekyler har potential som långverkande läkemedel men hade tidigare fallit i unåde i läkemedelsutvecklingen på grund av toxicitetsproblem. Den insikt ITC erbjuder om förhållandet mellan en hämmares molekylära struktur och hur den reagerar med sitt mål kommer att stödja förnyat intresse för kovalenta hämmare och underlätta arbetet med att utveckla dem till läkemedel som är både mycket effektiva och säkra.