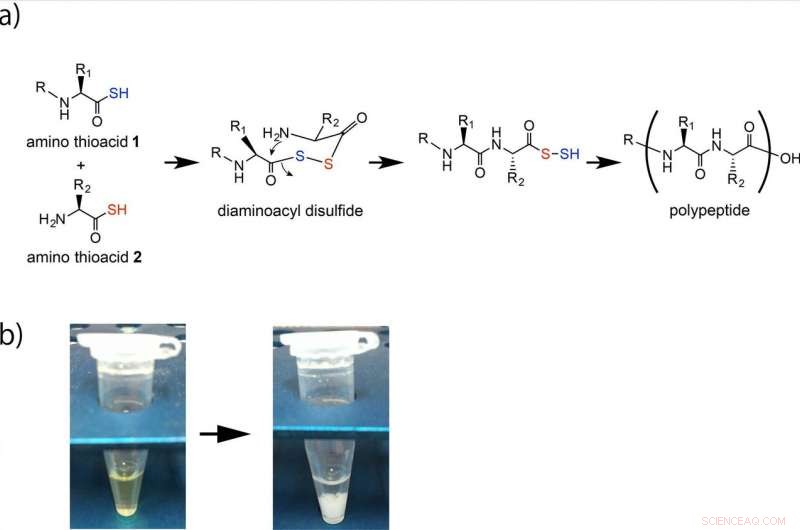
Polypeptidbildning genom den oxidativa reaktionen mellan aminosyror. (a) Amino tiosyror 1 och 2 kopplas via en diaminoacyldisulfidmellanprodukt och efterföljande intramolekylär amidbildning genererar en alfa-amidbindning. Järnmalm eller Fe2O3 i sur lösning påskyndar denna polypeptidbildning. Denna reaktions upprepade prestanda ger polypeptiden. (b) Polypeptiden bildas som en vit fällning. Upphovsman:Osaka University
De viktigaste beståndsdelarna i celler, vävnad, organ, och hela organismer är proteiner, som byggs genom tillsats av aminosyror efter varandra för att bilda långa proteinkedjor som kallas polypeptider. Även om levande celler har avancerade maskiner som kan uppnå denna kedjeförlängning med häpnadsväckande hastighet och noggrannhet, ansträngningar att efterlikna denna reaktion i laboratoriet för att skapa naturliga peptidprodukter eller peptidläkemedel har förblivit råa och mödosamma i jämförelse.
Med hjälp av varianter av aminosyror som kallas aminosyrasyror, ett team vid Osaka University har övervunnit dessa svårigheter för att uppnå en exakt och enkel förlängning av peptidkedjor i en snabb reaktion. Deras arbete, publicerad i tidningen Biokemi , föreslår också att för miljarder år sedan, denna speciella kemiska mekanism kunde ha möjliggjort ett överflöd av större mer komplexa molekyler att dyka upp, möjligen ger de förutsättningar som liv så småningom uppstod ur.
I den här studien, laget fokuserade på att förbättra tidigare ansträngningar att artificiellt syntetisera polypeptider, där ett stort hinder var behovet av att inkludera skyddsgrupper. Sådana skyddsgrupper läggs till funktionella grupper i en molekyl för att säkerställa att en efterföljande reaktion är specifik. Dock, de kräver att flera reaktionssteg utförs, vilket gör proceduren ineffektiv.
"I våra ansträngningar att förbättra artificiell peptidbindningsbildning, istället för att fokusera på aminosyror, vi tittade istället på aminotioacider, som inkluderar en svavelatom, "Säger Yasuhiro Kajihara." Vi började med aminotiosyraversionen av fenylalanin som en monomer, och under en reaktion som varade bara fem minuter fann man att peptidkedjor innehållande två till fem fenylalaniner bildades. En alternativ analys avslöjade kedjor så länge som 12 fenylalaniner. "
En bild av polypeptidbildning av aminosyror på ytan av järnmalm i sur lösning. Upphovsman:Osaka University
Teamet visade sedan att förlängningen av peptidkedjan inträffade med blandningar av aminotiosyror och även endast under sura förhållanden, som föreslog att oxidation var nyckeln till den inblandade mekanismen. Teamet bekräftade detta genom att karakterisera reaktionen, och visade också att det involverade en unik reaktionsmellanprodukt, vilket säkerställde att den avsedda produkten genererades korrekt.
"Med tanke på att förlängningen av vanliga aminosyror till kedjor är en nyckelfaktor för livet, vi undrade om, för miljarder år sedan, aminosyratsyror kunde ha fungerat som en föregångare till den mer komplexa kemin som ledde till utvecklingen av ett levande liv, med tanke på deras snabba och enkla införlivning i kedjor, "säger huvudförfattaren Ryo Okamoto." Vi fann att oligomeriseringsreaktionen också fortsatte under kemiska förhållanden som liknade dem på jorden innan livet uppstod, använda reaktionskomponenter som järnmalm och svavelsyra, som kunde ha genererats från vulkanisk gas. "
Teamets arbete ger således inte bara ett effektivt laboratorieverktyg för en rad praktiska tillämpningar, men också en potentiell inblick i kemin från vilken livet började.